肿瘤代谢重编程是癌症研究领域的核心方向之一,缺氧微环境引发的还原应激与能量应激平衡调控,是癌细胞存活与增殖的关键瓶颈。《Nature Cell Biology》(IF=19.5)近期发表的一项机制研究《AMPK-regulated glycerol excretion maintains metabolic crosstalk between reductive and energetic stress》(DOI:https://www.nature.com/articles/s41556-024-01549-x),从代谢网络调控视角出发,系统解析了AMPK(腺苷酸活化蛋白激酶)通过调控甘油排泄通路平衡肿瘤细胞双重应激的分子机制,为肿瘤代谢研究提供了全新的理论框架与技术范式。本文将从科研设计、核心机制、技术方法等维度,基于科研视角展开深度解析。
一、 研究背景与科学问题的精准定位
1. 领域研究现状与缺口
代谢重编程是癌症的标志性特征,缺氧条件下癌细胞通过重塑电子传递链(ETC)、糖酵解等通路维持氧化还原平衡与能量供给已成为共识。此前研究已建立"电子传递潜力"理论及电子平衡模型,但葡萄糖衍生的排泄性甘油在缺氧代谢中的功能尚未明确:
- 还原应激(NADH积累)与能量应激(ATP不足)的协同调控机制不明;
- 甘油代谢通路与肿瘤细胞缺氧适应的功能关联缺乏直接证据;
- 代谢网络中"应激平衡"的调控节点尚未被鉴定。
2. 核心科学问题
本研究聚焦三大关键科学问题:
- 缺氧环境下癌细胞是否通过甘油代谢通路调控NADH稳态?
- 甘油生物合成与排泄的分子调控网络如何构成?
- AMPK作为能量感知分子,是否参与甘油代谢与应激平衡的协同调控?
二、 研究设计与技术方法的科研严谨性
1. 多维度实验体系构建
为系统性验证科学假设,研究建立了"细胞-分子-动物-临床"四级实验体系:
- 细胞模型:覆盖HeLa、A549、HepG2等15种肿瘤细胞系及HUVEC、HAEC内皮细胞,设置常氧(20% O₂)、梯度缺氧(0%-5% O₂)及ETC抑制(抗霉素A处理)等多组学条件;
- 基因操作体系:利用CRISPR-Cas9技术构建GPD1、GPD1L、PGP等关键基因敲除(KO)细胞系,通过慢病毒载体实现目标基因过表达与shRNA介导的敲低,确保基因功能验证的特异性;
- 动物模型:采用裸鼠皮下移植瘤模型,评估关键基因对肿瘤生长、缺氧区域分布及细胞增殖凋亡的影响;
- 临床关联分析:整合TCGA数据库及宫颈癌、肺癌、肝癌患者血清样本,验证甘油代谢基因与临床预后的相关性。
2. 核心技术方法的创新性应用
研究整合多种前沿技术,确保机制解析的精准性与可靠性:
- 代谢分析技术:结合¹³C₆-葡萄糖同位素示踪、靶向代谢组学及GC-MS(气相色谱-质谱联用),明确甘油的葡萄糖来源及代谢流向;
- 分子互作技术:通过Co-IP、GST pull-down及内源性IP实验,验证ALDOB与GPD1/GPD1L的复合物形成;
- 磷酸化修饰分析:利用体外激酶实验、质谱鉴定及特异性磷酸化抗体,精准定位AMPK对ALDOB的磷酸化位点(T245);
- 功能验证技术:通过NADH/NAD⁺比率检测、ATP/AMP定量、细胞活力及集落形成实验,多维度评估代谢通路对细胞应激状态的影响。
三、 核心机制的科研解析:从通路激活到稳态调控
1. 缺氧诱导甘油排泄的分子通路解析
研究通过代谢流分析首次证实:缺氧条件下,葡萄糖经糖酵解生成DHAP(二羟丙酮磷酸),ALDOB与GPD1/GPD1L形成复合物,介导DHAP向甘油3-磷酸转化,再经PGP催化生成游离甘油,最终通过AQP3转运至细胞外。该通路的核心功能是持续消耗NADH,缓解缺氧诱导的还原应激——GPD1/GPD1L双敲除可显著升高NADH/NAD⁺比率,加剧细胞死亡,而补充α-酮丁酸(NADH氧化底物)可逆转这一表型。 从科研视角看,该发现填补了"葡萄糖代谢-还原应激调控"的机制缺口,明确了甘油排泄作为NADH耗散途径的全新功能,拓展了缺氧代谢通路的认知边界。
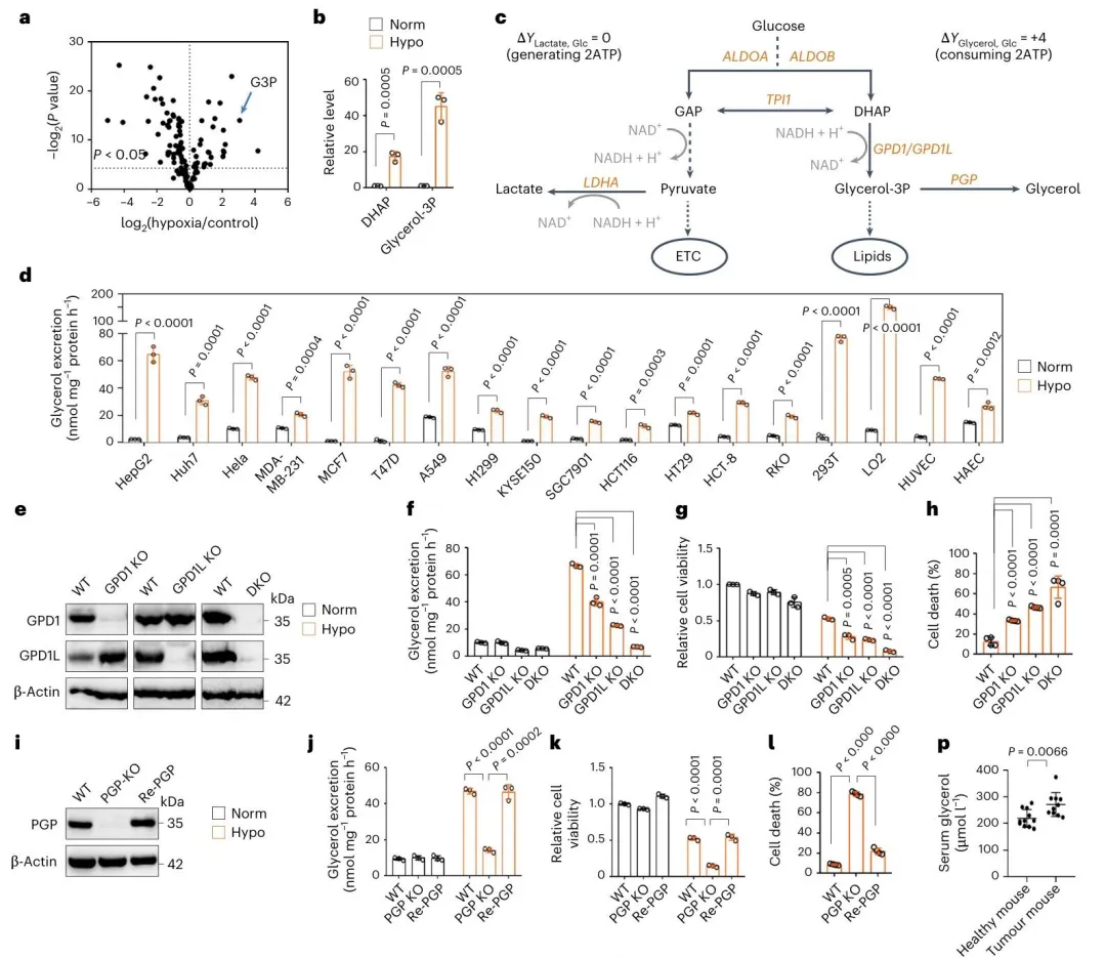
缺氧促进甘油排泄以支持细胞生长
2. HIF1α-葡萄糖摄取轴的上游调控机制
研究通过gain-of-function与loss-of-function实验证实,HIF1α(缺氧诱导因子1α)是甘油代谢通路的上游调控因子:
- HIF1α敲低可抑制GLUT1(葡萄糖转运体)与HK2(己糖激酶)的表达,显著降低葡萄糖摄取及甘油排泄;
- VHL敲除(稳定HIF1α)可增强甘油代谢通路活性,且ETC抑制剂可进一步协同促进该效应。 这一机制揭示了HIF1α通过调控葡萄糖代谢上游环节,为甘油生物合成提供底物供给,建立了"缺氧感知-底物转运-代谢通路激活"的调控链,体现了代谢网络的层级调控逻辑。
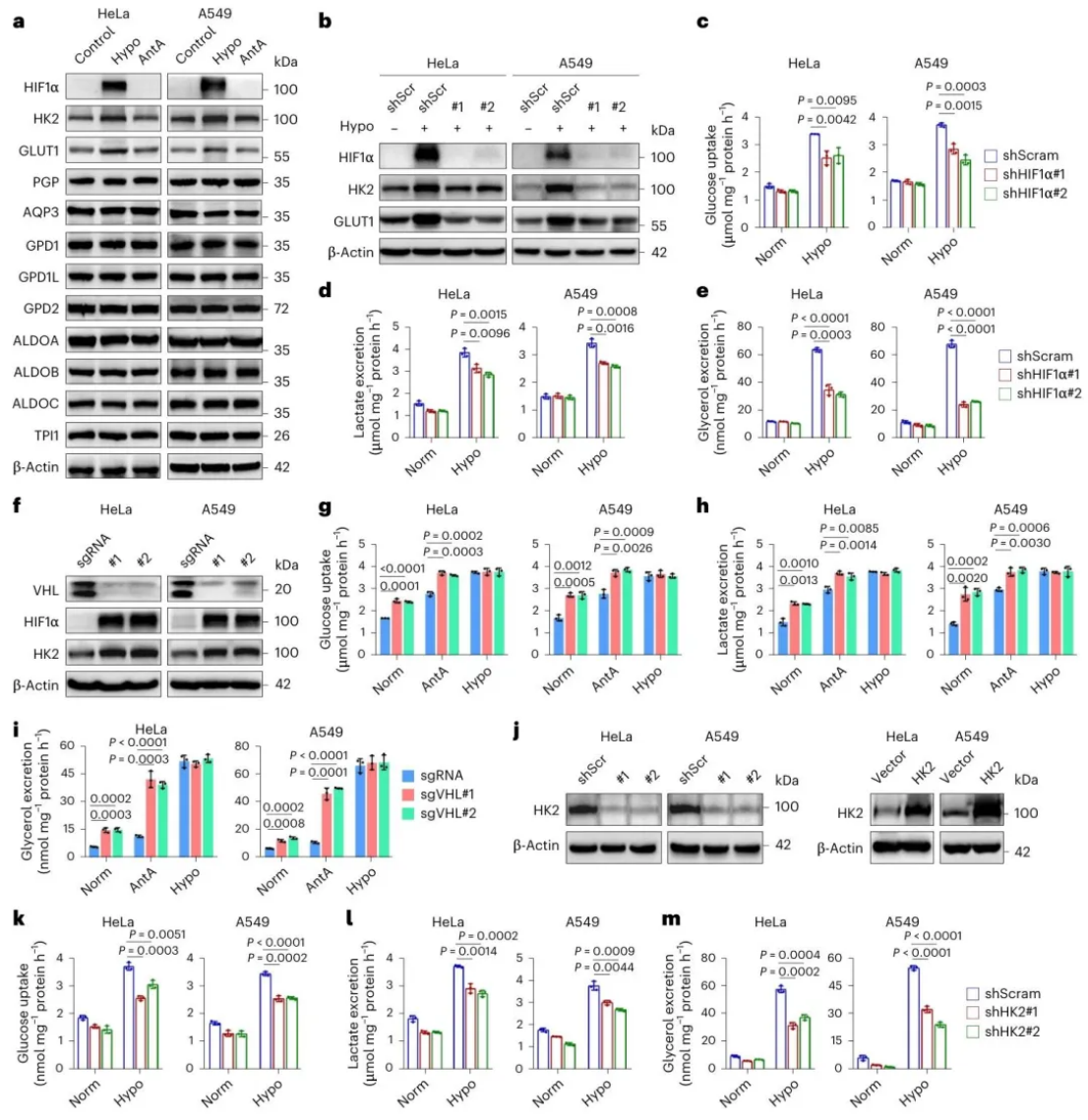
缺氧促进甘油排泄依赖于 HIF1α 诱导
3. AMPK-ALDOB轴的应激平衡调控机制
甘油合成过程需消耗ATP,过量激活会引发能量应激,研究首次发现AMPK通过精准调控ALDOB活性维持能量稳态:
- 能量应激下,AMPK被激活并与ALDOB直接结合,在T245位点进行磷酸化修饰;
- T245磷酸化可显著抑制ALDOB酶活性,减少甘油合成与ATP消耗,避免能量危机;
- 突变体实验证实:T245A(非磷酸化模拟)可增强甘油排泄与能量应激,T245D(磷酸化模拟)则抑制该效应,且不受AMPK调控。
从科研价值来看,该机制首次鉴定了AMPK作为"应激平衡开关"的全新功能,阐明了"代谢通路激活-能量消耗-负反馈调控"的闭环机制,为理解代谢网络的稳态调控提供了典型范例。
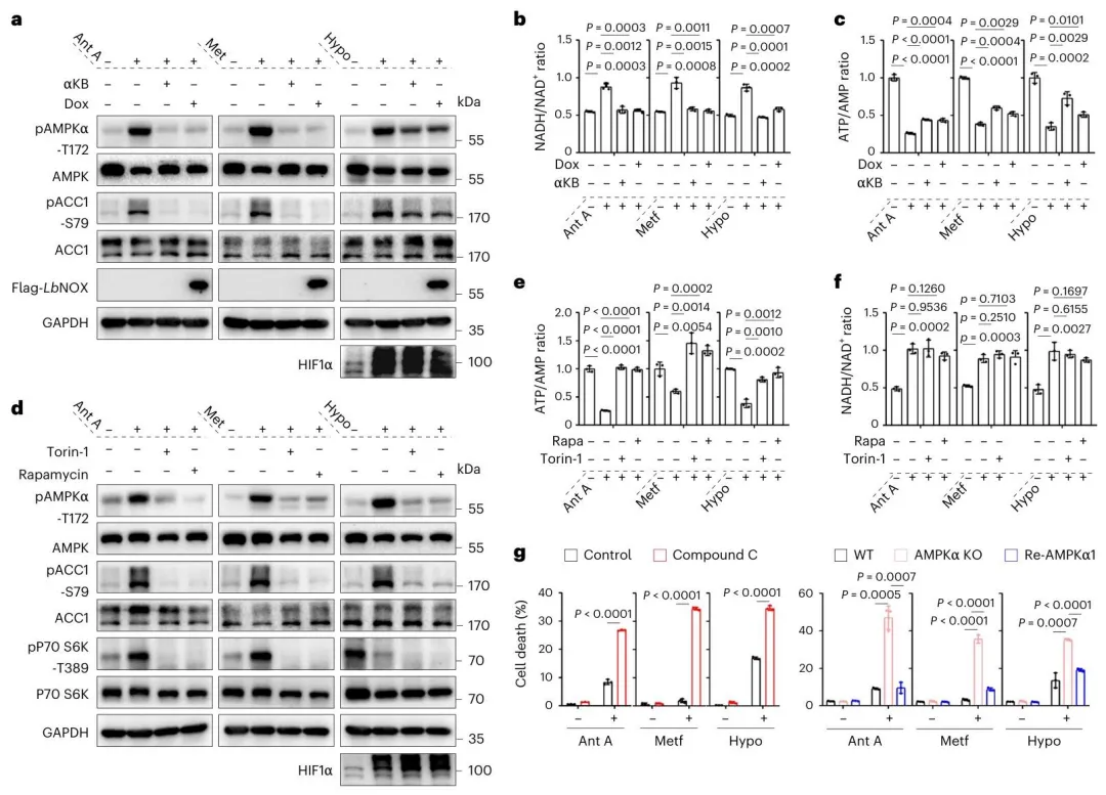
还原应激与能量应激的平衡调控
四、 研究结论的科研突破与学术价值
1. 理论突破
- 提出"甘油排泄-NADH耗散"理论,首次明确甘油代谢在还原应激调控中的核心作用;
- 建立"AMPK-ALDOB-甘油代谢"调控轴,揭示了能量应激与还原应激的协同平衡机制;
- 构建"代谢权衡"模型,解释了肿瘤细胞通过适度甘油代谢促进生长、过量则抑制增殖的双向调控效应。
2. 学术价值
- 拓展了AMPK的调控底物谱,首次证实ALDOB是AMPK的直接磷酸化靶点;
- 明确了ALDOB作为甘油合成关键同工型的特异性功能,纠正了此前"醛缩酶同工型功能冗余"的认知;
- 发现甘油代谢相关基因(ALDOB、GPD1等)可作为癌症预后生物标志物,为临床转化提供理论基础。
五、结语
1. 现有研究的局限性
从科研严谨性出发,本研究仍存在以下待完善之处:
- 机制验证集中于细胞系与裸鼠模型,缺乏临床样本的功能验证(如患者来源肿瘤异种移植模型PDX);
- 未探索甘油代谢在正常组织缺氧适应中的作用,无法明确肿瘤特异性;
- 未解析AMPK-ALDOB通路与脂质合成、糖酵解等其他代谢通路的串扰机制。
2. AMPK 调控研究与 LabEx 科研服务
本研究通过严谨的科研设计与创新的技术方法,系统解析了 AMPK 介导的甘油代谢调控机制,不仅深化了对肿瘤缺氧适应的认知,更为代谢领域的科研探索提供了可借鉴的理论框架与技术范式。
而 LabEx 作为一站式生物标志物发现服务平台,凭借覆盖核酸 - 蛋白多维度的 30 + 检测技术平台、5000 + 检测指标及 100 万 + 样本检测经验,可通过多因子检测、转录组测序、DSP 空间多组学等核心技术,为该机制的进一步验证、临床转化及生物标志物开发提供全方位技术支撑,助力科研成果从基础研究迈向临床应用。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


