一、外泌体的定义、来源与分子组成
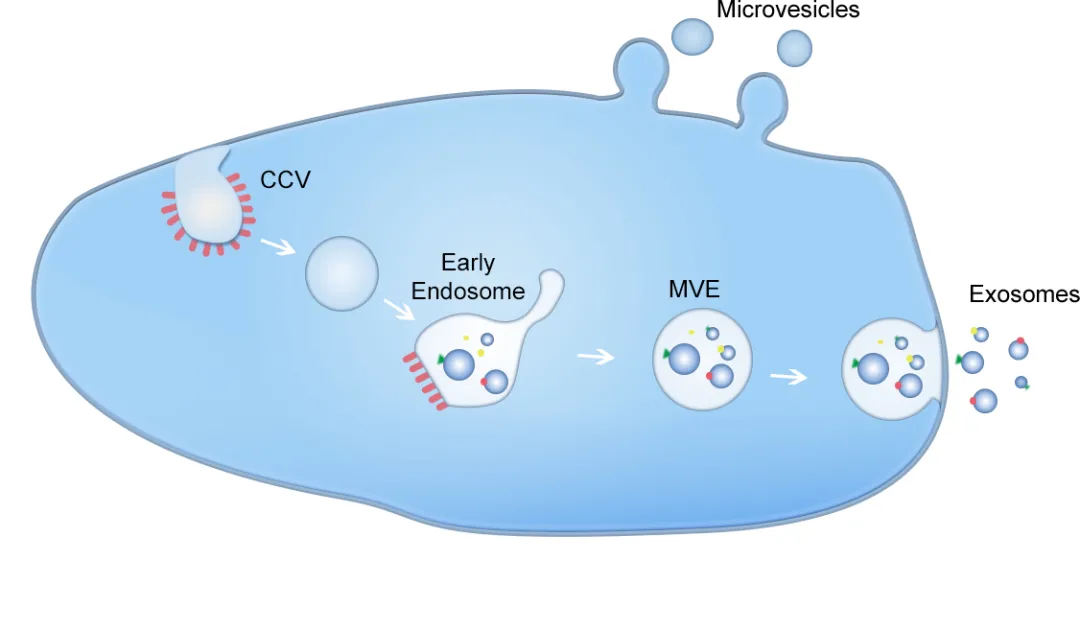
外泌体是一类直径介于30至150纳米的细胞外囊泡,由细胞主动分泌并广泛存在于体液中。其生物发生具有明确的胞内途径:起源于晚期内体,通过内体膜向内出芽形成多囊泡体,随后多囊泡体与细胞质膜融合,将其腔内囊泡释放至细胞外空间,此即外泌体。因此,外泌体并非由质膜直接出芽产生,而是经由严格调控的多囊泡内体途径生成。
在结构上,外泌体具有典型的脂质双分子层膜结构,该结构为其内部活性成分提供了稳定的微环境。其腔内富含一系列复杂的生物大分子,主要包括功能性蛋白质、信使RNA、微RNA等多种非编码RNA,以及DNA片段。这些分子共同构成了外泌体介导细胞间通讯、物质交换与信息传递的分子基础,在生理稳态与病理进程中均发挥着重要作用。
二、外泌体研究历程的重要里程碑
外泌体研究的演进跨越数十年,其认知过程伴随着一系列关键发现。
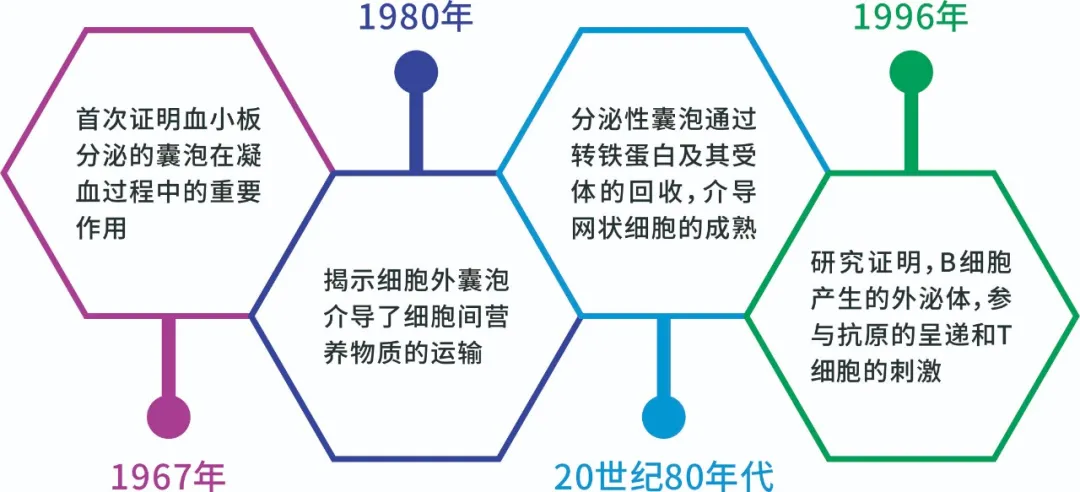
该领域的早期线索可追溯至二十世纪中后期。约1967年,研究人员首次在生物样本中观察到膜性囊泡结构。至1980年,学术界首次通过实验证实,由血小板释放的囊泡在生理性凝血过程中扮演着重要角色,推动了相关研究的发展。
随后的十余年间,细胞外囊泡的功能研究取得了实质性进展。约1996年,研究发现这些囊泡能够介导细胞间的营养物质转运,拓展了对其生理功能的认识。同期,另一重要研究揭示,特定分泌性囊泡通过参与转铁蛋白及其受体的循环机制,对网状红细胞的成熟过程起到了关键的调控作用。更关键的是,同年研究证实,源自B淋巴细胞的外泌体,能够参与抗原呈递过程并激活T淋巴细胞,这首次明确了外泌体在适应性免疫应答中的直接作用。
这些里程碑式的工作逐步揭示了外泌体作为重要的细胞间通讯介质,在维持生理稳态和调控免疫反应等多方面所具有的基础性生物学功能,为后续研究奠定了坚实的理论与实验基础。
三、外泌体研究的核心要素与鉴定体系
外泌体研究主要围绕其组成与功能的完整逻辑链条展开,包含以下几个基本要素:
✔️来源与成分:明确外泌体的供体细胞类型及其所携带的特征性内含物。
✔️靶向与归宿:确定外泌体特异性识别的受体细胞或组织。
✔️功能与机制:阐明外泌体介导的生物学效应及其具体的分子作用途径。
外泌体的鉴定方法与标准
对外泌体的可靠鉴定是相关研究的基础,通常采用多方法联用的策略,主要分为整体鉴定与单颗粒鉴定两个层面。
(一)整体鉴定
此层面侧重于通过群体水平的生物化学分析确认外泌体的身份。
💯特异性蛋白标志物检测:常采用蛋白质印迹法。
阳性标志物:要求至少检测到三个阳性蛋白标志物,其组合应包含至少一种跨膜蛋白(如四跨膜蛋白家族成员CD63、CD9、CD81)或脂质结合蛋白,以及至少一种胞质蛋白(如多囊泡内体形成相关蛋白TSG101或膜联蛋白)。
阴性标志物:必须确认至少一种特定细胞器(如线粒体、高尔基体、内质网)的标记蛋白为阴性,以排除细胞碎片等杂质污染。
(二)单颗粒鉴定
此层面侧重于对单个囊泡的物理特性进行表征。
膜泡结构观察:采用透射电子显微镜或原子力显微镜进行形态学分析,主要观察其是否具备典型的茶托状或球形双层膜结构。
尺寸分布分析:采用纳米颗粒跟踪分析等技术,精确测定囊泡群体的粒径大小及其分布范围,以确认其符合外泌体典型的纳米级尺度。
以上多维度、互补的鉴定标准共同构成了目前学术界广泛认可的、用于确认外泌体身份的核心实验框架。
四、外泌体miR-934在结直肠癌肝转移中的作用机制研究
(一)临床相关性发现
通过生物信息学分析与临床样本验证,研究发现miR-934在结直肠癌肝转移患者组织样本中表达显著上调,且其高表达与疾病进展及患者不良预后密切相关。
(二)外泌体递送功能验证
研究证实miR-934可被有效包裹于结直肠癌细胞来源的外泌体中。通过透射电镜观察囊泡形态、纳米颗粒追踪分析粒径分布及特异性蛋白标志物检测等综合鉴定方法,确认了外泌体的结构完整性,并在其中检测到高水平的miR-934,为后续功能研究提供了物质基础。
(三)表型功能分析
体外及体内实验表明,结直肠癌细胞来源的外泌体可通过递送miR-934,有效诱导巨噬细胞向M2表型极化,进而促进肿瘤细胞的侵袭能力及肝脏转移进程。
(四)分子机制解析
机制研究揭示,外泌体miR-934通过靶向巨噬细胞内的hnRNPA2B1基因,下调PTEN表达,进而激活PI3K/AKT信号通路,是诱导M2极化的核心分子事件。极化后的M2巨噬细胞通过分泌CXCL13,激活肿瘤细胞表面的CXCR5受体及下游NF-κB信号,形成一个由CXCL13/CXCR5/NF-κB/p65/miR-934构成的分子反馈环路。此环路持续强化肿瘤微环境中肿瘤细胞与巨噬细胞间的相互作用,最终驱动结直肠癌肝转移的恶性进展。
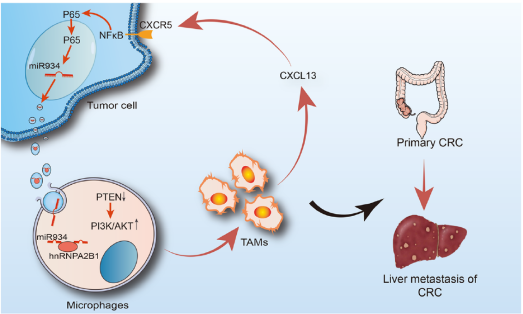
综上,本研究系统阐释了外泌体递送的miR-934通过调控肿瘤相关巨噬细胞极化,进而促进结直肠癌肝转移的完整作用轴与分子反馈机制。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


