一、引言
聚合酶链式反应(PCR)作为分子生物学研究的基础技术,其产物的纯化回收是后续克隆、测序、表达等实验的关键前置步骤。在实际操作过程中,DNA片段的损失难以完全避免,回收率波动直接影响下游实验的可行性与可靠性。如何有效提升PCR产物的纯化回收率,始终是实验技术优化的重要方向。本文从原理层面分析影响回收效率的关键因素,并系统阐述相应的优化策略。
二、PCR产物纯化的基本原理与回收率影响因素
2.1 纯化技术原理概述
目前主流的PCR产物纯化方法主要基于离心柱膜吸附技术或磁珠分离技术。离心柱法利用硅胶膜在高盐低pH条件下特异性结合DNA,经洗涤去除引物二聚体、核苷酸及聚合酶等杂质后,在低盐高pH条件下洗脱回收。磁珠法则通过表面修饰的羧基与DNA在PEG/NaCl体系中发生选择性结合,借助磁分离实现纯化。
2.2 影响回收率的核心参数
影响回收效率的因素可归纳为样本属性与操作条件两大类。样本方面,DNA片段长度、浓度以及PCR体系中的残留成分均对结合效率产生影响。操作方面,结合缓冲液pH值、离子强度、洗脱温度及时间等参数直接决定最终回收产量。
三、样本前处理环节的优化策略
3.1 PCR产物的质量评估
纯化前对PCR产物进行质量评估具有重要意义。电泳检测可明确目标条带亮度、特异性及是否存在非特异性扩增。对于存在明显杂带或引物二聚体的样本,单纯依赖柱纯化难以完全去除干扰物,应考虑切胶回收方案。此外,高浓度样本需注意避免柱过载,低浓度样本则需调整结合体系以提高捕获效率。
3.2 样本稀释与结合缓冲液配比调整
样本中残留的PCR成分可能干扰DNA与硅胶膜的结合。适当稀释样本可降低离子强度波动带来的影响。结合缓冲液与样本的体积比例需严格遵循说明书基础并酌情优化,增加结合缓冲液比例有助于提高短片段DNA的回收效率,但可能降低长片段的洗脱得率,需根据目标片段长度进行平衡。
四、结合与洗涤条件的精细化控制
4.1 结合体系pH与离子强度的调节
硅胶膜对DNA的吸附依赖于高盐条件促进DNA脱水并与硅羟基形成氢键。结合缓冲液的pH通常维持在酸性范围,有利于DNA吸附。实际操作中应确保结合液与样本充分混匀,避免局部pH偏离。对于长片段DNA(>5 kb),可考虑适当降低结合温度或延长结合时间,以减少剪切力造成的损伤。
4.2 洗涤操作的标准化
洗涤步骤旨在去除蛋白质、盐分及有机溶剂残留。洗涤缓冲液中通常含有乙醇,需确保每次洗涤后离心彻底去除残留液体,避免乙醇携带至洗脱步骤影响DNA溶解。重复洗涤一次虽可提高纯度,但可能造成少量DNA损失,需根据样本纯度要求权衡。
五、洗脱环节的关键技术要点
5.1 洗脱体积与孵育时间优化
洗脱体积直接影响最终DNA浓度。减少洗脱体积可提高浓度,但可能降低绝对回收量。常规建议使用30-50 μL洗脱缓冲液,若对浓度要求较高,可分两次洗脱合并或采用预热洗脱液。洗脱液在膜上停留时间延长有利于DNA充分溶解,推荐孵育2-5分钟后再离心收集。
5.2 洗脱温度与pH的作用
预热洗脱缓冲液至55-65℃可显著提高长片段DNA的洗脱效率。洗脱缓冲液通常为Tris-EDTA(TE)或Elution Buffer,pH偏碱性有助于DNA与硅膜解离。洗脱后快速置于冰上可防止降解,尤其对于后续需进行酶连或转化的样本更为重要。
六、针对不同片段长度的回收率提升方案
6.1 短片段DNA(<200 bp)的回收
短片段DNA易与引物二聚体一同流失,提高回收率需采用专门针对小片段的纯化试剂盒或调整结合条件。增加结合缓冲液中乙醇浓度或延长结合时间可增强短片段吸附,但需注意洗涤彻底以去除残留盐分。
6.2 长片段DNA(>5 kb)的回收
长片段DNA对物理剪切力敏感,操作时应避免剧烈涡旋或反复吹吸。可采用宽口吸头转移液体,洗脱时避免过度加热。部分情况下,可选择特异性针对大片段的磁珠法纯化,减少离心过程带来的损伤。
七、质量控制与回收率验证
7.1 回收产物定量方法
纯化后需通过紫外分光光度法或荧光染料法进行精确定量。紫外分光光度法可同时评估纯度(A260/A280比值),荧光染料法对双链DNA特异性强,更适合低浓度样本定量。结合纯化前定量结果计算回收率,可为后续优化提供数据支持。
7.2 琼脂糖凝胶电泳验证
电泳不仅可观察回收条带的完整性,还可评估是否存在降解或非特异性条带。梯度上样有助于半定量判断回收效率,为实验记录保留直观证据。
八、结语
提升PCR产物纯化回收率是一项系统工程,涉及样本前处理、结合条件优化、洗涤标准化及洗脱精细化等多个环节。根据不同片段长度及下游应用需求,灵活调整操作参数,结合严格的质量控制,可显著提高回收效率与产物质量,为后续分子克隆及分析实验奠定坚实基础。持续关注纯化技术的改进与方法学更新,亦是保障实验结果稳定性的重要路径。
九、PCR技术哪里有?
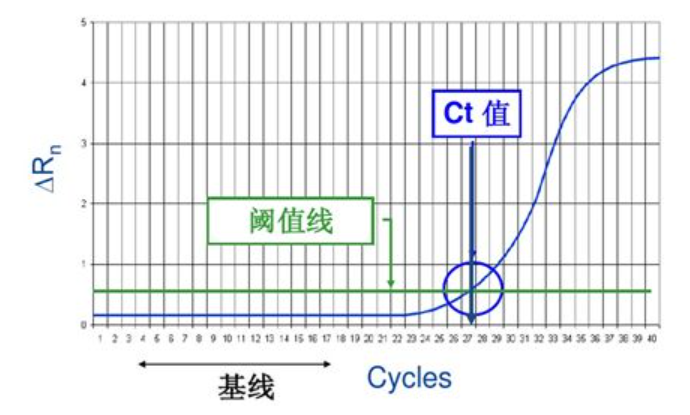
LabEx为您提供专业、全面的PCR技术整体解决方案。基于实时荧光定量PCR(qPCR)、数字PCR(dPCR)及常规PCR平台,我们可对各种生物样本(如组织、细胞、血液、微生物等)中的特定DNA或RNA靶标进行高灵敏度、高特异性的定性与定量分析。我们的服务涵盖从实验设计、核酸提取与质检、引物探针设计优化、PCR扩增、数据分析到结果解读的全流程,并建立严格的质控体系以确保数据的准确性与可重复性。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


