引言
铁死亡作为2012年被正式命名的铁依赖性程序性细胞死亡方式,以铁代谢紊乱、脂质过氧化及抗氧化系统失衡为核心特征,与传统凋亡、坏死等细胞死亡形式存在显著差异。近年来,该领域研究呈指数级增长,其独特的代谢调控网络及与肿瘤、神经退行性疾病、器官损伤等多种疾病的密切关联,使其成为国自然研究的TOP5热点方向。
一、铁死亡的核心定义与生物学特征
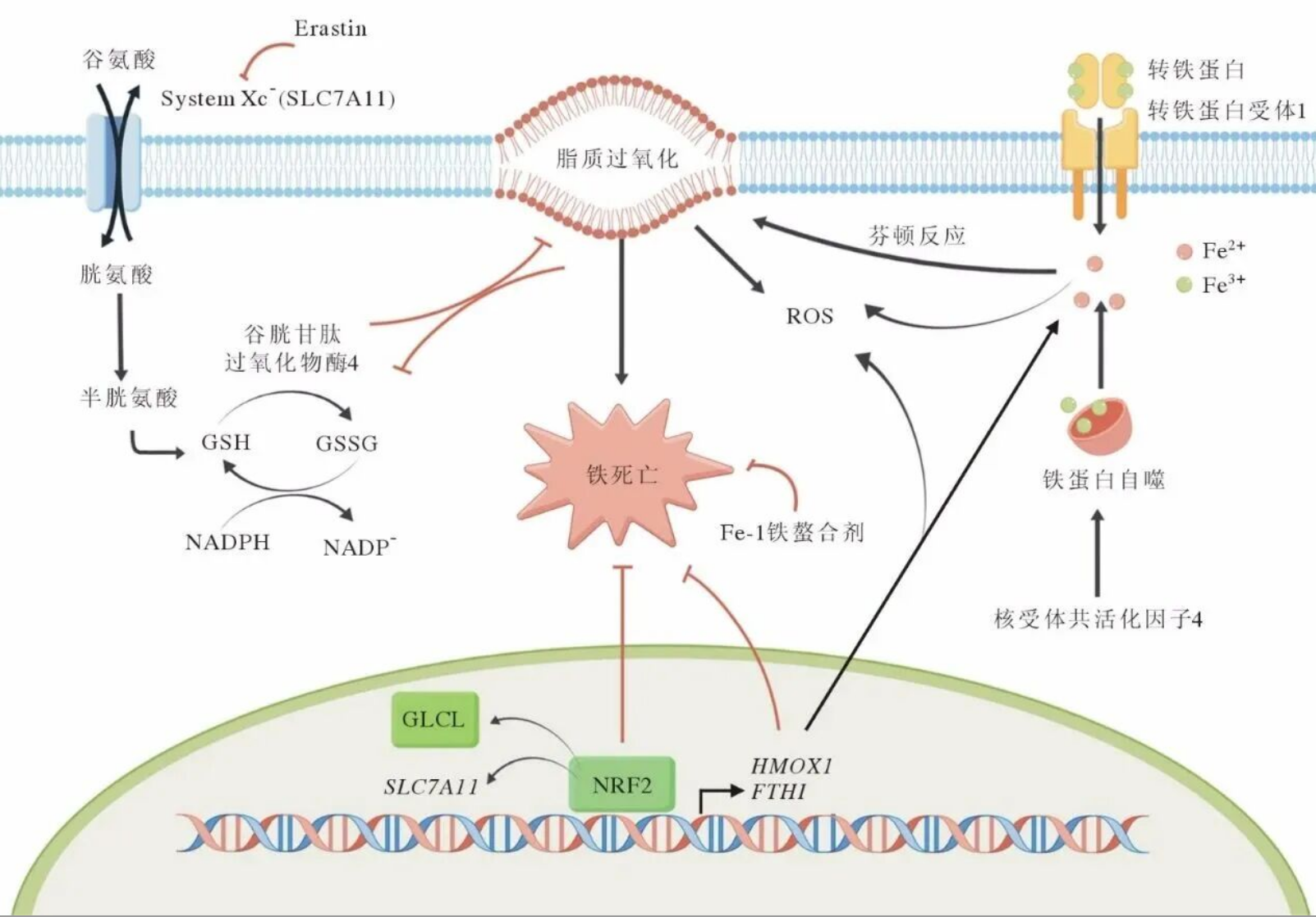
铁死亡(Ferroptosis)是一种由铁依赖性磷脂过氧化作用驱动的新型程序性细胞死亡方式,其发生不依赖传统凋亡或坏死信号通路,也无DNA裂解特征,核心标志为细胞内铁离子异常积累、细胞膜脂质过氧化产物大量堆积及抗氧化系统功能失效,最终导致细胞膜结构破坏、细胞内容物外泄并引发细胞破裂。
铁死亡的发生与细胞内铁代谢、氧化还原稳态及脂质代谢密切相关,其核心生物学过程包含两大关键环节:
一是铁代谢紊乱导致的细胞内游离铁离子积聚,铁离子通过转铁蛋白受体1(TFR1)进入细胞后,铁储存与释放的平衡被打破,游离铁(Fe²⁺)大量增加;
二是铁离子通过芬顿反应催化过氧化氢(H₂O₂)生成羟基自由基(•OH),该自由基与细胞膜上的多不饱和脂肪酸(PUFAs)发生反应,形成4-羟基二烯丙基过氧化物(4-HNE)等脂质过氧化产物,直接破坏细胞膜的完整性。同时,细胞内谷胱甘肽(GSH)耗竭导致抗氧化防御系统失效,无法清除脂质过氧化产物,进一步推动铁死亡的进程。 与凋亡、自噬等细胞死亡方式相比,铁死亡具有显著的代谢依赖性,其发生受铁代谢、氨基酸代谢、脂质代谢及线粒体活性等多种细胞代谢途径调控,这也使其成为连接细胞代谢与疾病发生发展的关键节点。
二、铁死亡的分子调控机制
铁死亡的调控网络复杂且多元,涵盖核心调控因子、关键信号通路及细胞代谢途径的相互作用,目前已明确的调控机制主要包括核心分子调控、信号通路调控及代谢途径调控三个层面,各层面相互交织形成精密的调控网络。
(一)核心调控因子
铁死亡的发生受多个关键分子的直接调控,其中GPX4、System Xc⁻及FSP1为三大核心调控因子,构成铁死亡抑制的核心体系。
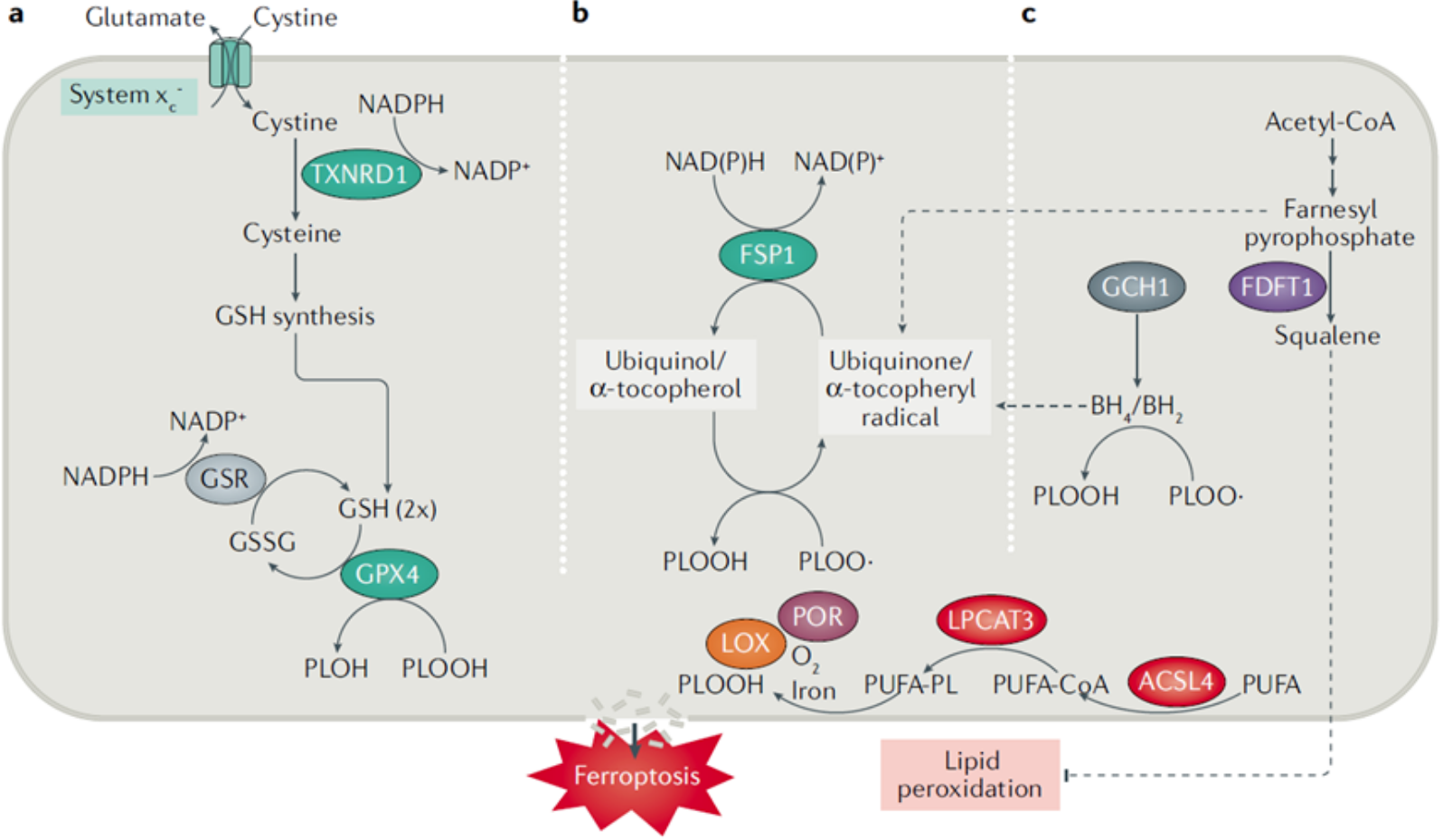
1. GPX4(谷胱甘肽过氧化物酶4)
作为铁死亡最关键的抑制因子,GPX4是一种硒依赖性抗氧化酶,可直接清除细胞膜上的磷脂氢过氧化物(PLOOHs),阻断脂质过氧化的级联反应。GPX4的功能受限或表达下调会直接导致脂质过氧化产物堆积,显著促进铁死亡发生;而铁死亡诱导剂如RSL3可通过共价修饰GPX4活性位点的硒半胱氨酸,使其发生不可逆失活,从而诱导铁死亡。此外,GPX4的表达受硒代谢、转录因子TFAP2c/Sp1及C/EBPα等调控,补硒可通过激活相关转录因子促进GPX4表达,发挥抗铁死亡作用。
2. System Xc⁻(半胱氨酸/谷氨酸交换系统)
作为细胞膜上的重要转运蛋白,System Xc⁻负责介导细胞外胱氨酸与细胞内谷氨酸的交换,而胱氨酸是细胞内GSH合成的关键前体。System Xc⁻功能受损会导致胱氨酸摄入不足,GSH合成受阻,抗氧化能力下降,进而促进脂质过氧化与铁死亡发生,其关键亚基SLC7A11的表达异常是多种疾病中铁死亡调控的重要靶点。
3. FSP1(铁死亡抑制蛋白1)
作为GPX4非依赖的铁死亡抑制因子,FSP1可通过减少氧化应激、维持泛醌的还原状态发挥抗铁死亡作用,其底物为甲羟戊酸途径的代谢产物泛醌。FSP1是转录因子NRF2、PPARα的靶基因,其表达还受长链非编码RNA MEG3和miR-214的表观调控,在肿瘤细胞中铁死亡的调控中发挥重要作用。 此外,ACSL4、TFRC等分子也参与铁死亡的调控,ACSL4可促进PUFAs的活化与磷脂合成,为脂质过氧化提供底物,而TFRC作为铁离子转运受体,其高表达会增加细胞内铁离子摄入,促进铁死亡。
(二)关键信号通路调控
近年来研究发现,多种细胞信号通路可通过调控核心因子的表达或活性,影响细胞对铁死亡的易感性,其中Hippo-YAP、AMPK、缺氧信号通路及NRF2通路为研究最为深入的通路。
1. Hippo-YAP通路:该通路通过E-钙粘蛋白-NF2介导的细胞间接触激活,抑制YAP/TAZ的核易位与转录活性。YAP可直接靶向ACSL4、TFR1等铁死亡调控因子,因此Hippo通路抑制或YAP激活会显著增强细胞铁死亡易感性。由于该通路组分在癌症中常发生突变导致YAP过度激活,诱导铁死亡成为治疗此类癌症的潜在策略。
2. AMPK通路:作为能量感应激酶,AMPK在葡萄糖饥饿时被激活,通过抑制PUFAs的生物合成发挥抗铁死亡作用,其保护机制可有效防止肾缺血-再灌注损伤,成为器官保护的重要靶点。
3. 缺氧信号通路:缺氧并非抑制铁死亡,反而可通过线粒体复合体III产生活性氧(ROS)增加,及缺氧诱导因子HIF2α介导的HILPDA表达上调,促进多不饱和脂质富集,从而增强细胞对铁死亡的敏感性,该机制在透明细胞癌的铁死亡调控中具有重要临床意义。
4. NRF2通路:作为氧化应激反应的核心转录因子,NRF2可通过激活其靶基因(如SLC7A11、GPX4)的表达,增强细胞抗氧化能力,从而减轻铁死亡,是铁死亡调控的重要上游通路。
(三)代谢途径的交叉调控
铁死亡与细胞多种代谢途径密切相关,其中甲羟戊酸途径、铁代谢及脂质代谢的交叉调控是关键。甲羟戊酸途径的代谢产物不仅为FSP1提供底物泛醌,其介导的异戊烯化还可稳定硒代半胱氨酸特异性tRNA,为GPX4等硒酶的合成提供保障,使该途径成为连接GPX4与FSP1两大抑制体系的桥梁。铁代谢与脂质代谢的协同失衡则是铁死亡发生的基础,游离铁的积聚为脂质过氧化提供了催化条件,而PUFAs的大量合成则为脂质过氧化提供了底物,二者共同推动铁死亡的进程。
三、铁死亡与重大疾病的关联机制
铁死亡在多种疾病的发生、发展中发挥关键作用,其调控异常与肿瘤、神经退行性疾病、心血管疾病及肝脏损伤等重大疾病密切相关,且在不同疾病中呈现出“双向调控”的特征,为疾病的治疗提供了全新的靶点与策略。
(一)铁死亡与肿瘤
铁死亡在肿瘤中的作用具有显著的临床意义,肿瘤细胞常通过激活铁死亡抑制途径(如上调SLC7A11、GPX4表达)逃避铁死亡,进而产生化疗与免疫治疗耐药。反之,在肿瘤微环境中调控SLC7A11-GSH-GPX4轴、增强脂质过氧化或靶向Hippo-YAP通路诱导铁死亡,可显著提高肿瘤细胞对化疗、免疫治疗的敏感性。此外,缺氧肿瘤微环境中HIF2α-HILPDA介导的铁死亡增敏机制,为靶向清除缺氧肿瘤细胞提供了新方向,而“抑制mtDNA修复+诱导铁死亡”的联合策略也在肺癌模型中证实具有显著的抑瘤效果且毒性较低。
(二)铁死亡与神经退行性疾病
在阿尔茨海默病、帕金森病等神经退行性疾病中,脑内铁离子异常积聚、氧化应激增强及GPX4表达下调等因素共同推动神经元铁死亡的发生,进一步加剧神经元的损伤与丢失。铁死亡通过破坏神经元细胞膜结构、影响线粒体功能,成为神经退行性疾病病理进程的重要推手,而抑制铁死亡、上调GPX4表达则可发挥神经保护作用,为神经退行性疾病的早期干预提供了新靶点。
(三)铁死亡与心血管及器官损伤
铁死亡在心肌缺血-再灌注损伤、肾缺血-再灌注损伤及肝脏损伤中均发挥重要作用。在缺血-再灌注过程中,细胞内铁代谢紊乱、ROS大量生成及抗氧化系统失效,导致心肌细胞、肾小管上皮细胞等发生铁死亡,加剧器官损伤;而激活AMPK通路、抑制铁死亡则可有效减轻器官缺血-再灌注损伤。此外,肝脏内铁的异常积累是肝损伤、肝硬化的重要诱因,铁死亡介导的肝细胞损伤成为肝脏疾病研究的热点方向。
四、总结与展望
自 2012 年被提出以来,铁死亡研究历经十余年的发展,已成为细胞生物学与疾病机制研究的前沿热点,其独特的铁依赖性脂质过氧化特征、复杂的代谢调控网络及与多种重大疾病的密切关联,使其成为国自然研究的重点方向,仅 2024 年医学科学部就围绕铁死亡立项 439 项国家自然科学基金项目,近十年相关基金资助金额超 34 亿元,发文量从年产数篇增长至近万篇,研究热度持续攀升。
目前,铁死亡的核心调控机制已初步明确,GPX4 依赖与非依赖的抑制体系、多条信号通路的交叉调控及代谢途径的协同作用,共同构成了铁死亡的调控网络;而铁死亡在疾病中的 “双向调控” 特征,为疾病的治疗提供了全新的思路。随着多组学技术、高通量筛选平台、超高分辨率成像技术及 AI 辅助药物设计的发展,铁死亡研究将向机制深化、靶点创新、精准治疗的方向迈进,未来需进一步解析铁死亡与天然免疫、自噬、焦亡等细胞死亡方式的相互作用,挖掘新的调控靶点与信号通路;加强跨学科合作,推动铁死亡诱导剂与抑制剂的临床转化;建立标准化的铁死亡检测方法与临床评估体系,实现铁死亡调控策略在重大疾病中的精准应用。
铁死亡作为连接铁代谢、氧化还原稳态与细胞死亡的关键节点,其研究成果不仅将深化对生命过程的理解,更将为肿瘤、神经退行性疾病、器官损伤等重大疾病带来革命性的诊疗策略,具有重要的基础研究价值与临床应用意义。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


