KRAS基因突变在结直肠癌(CRC)的发生进程中扮演着关键角色,同时也是导致治疗抵抗出现的核心驱动因素。然而,截至目前,其背后潜在的分子机制以及有效的靶向治疗方法,依旧处于探索阶段,成果十分有限。
2026年3月4日,苏州大学医学院基础医学院的吴华教授团队,携手苏州系统医学研究所的李贵登研究员、苏州大学附属第一医院的郭凌川教授,于Nature子刊Nature Metabolism上发表了一篇题为“Extracellular CD44 lactylation impairs CD8+ T cell function in KRAS-mutant colorectal cancer”的研究论文。

该研究成功揭示了KRAS突变型(KRAS/MT)结直肠癌(CRC)免疫逃逸的全新机制:肿瘤微环境中的乳酸,会通过对细胞外CD44进行乳酸化修饰,直接对CD8⁺T细胞的功能造成损害,进而抑制抗肿瘤免疫反应。这一发现还表明,针对TRIP6–ENO2–CD44乳酸化信号轴开展靶向治疗,或许有望成为克服免疫治疗耐药性的一种极具前景的新策略。
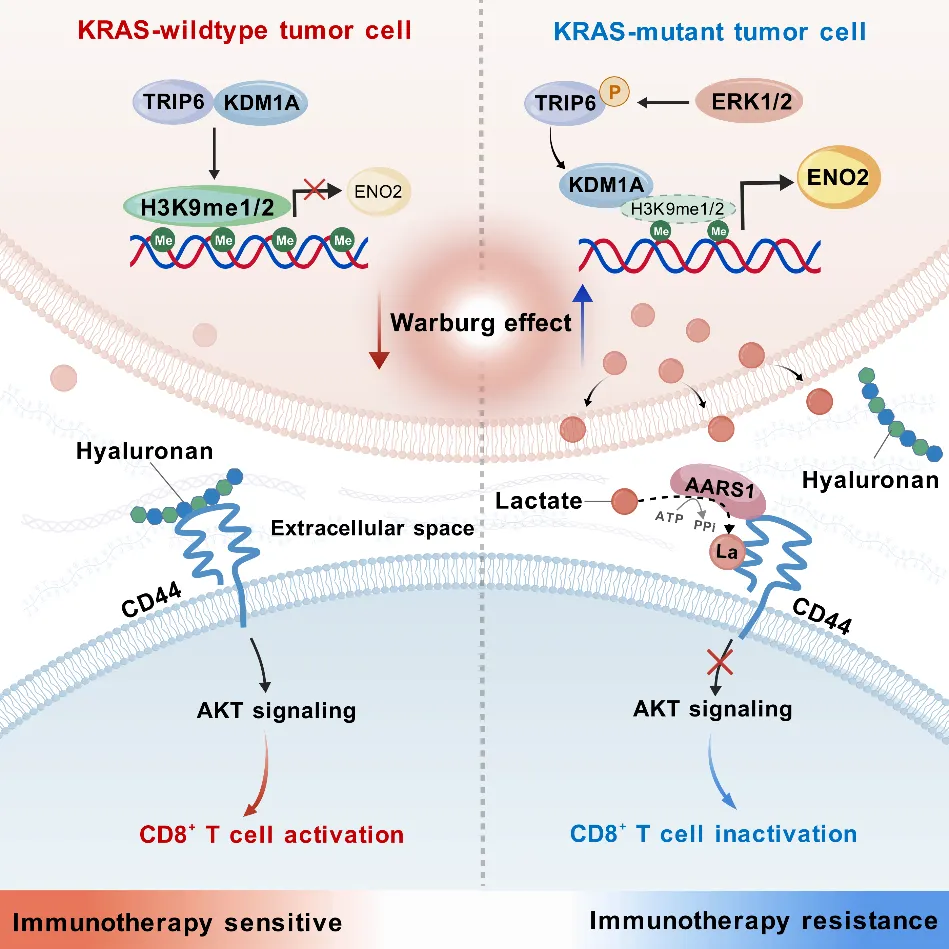
在这项最新研究中,研究团队发现TRIP6的磷酸化修饰是KRAS突变型(KRAS/MT)结直肠癌(CRC)免疫逃逸的关键“开关”。具体而言,在KRAS野生型结直肠癌细胞里,未发生磷酸化的TRIP6会与KDM1A相结合,通过促使H3K9me1/H3K9me2的积累,抑制ENO2酶的表达,从而对糖酵解过程起到限制作用。而在KRAS/MT型结直肠癌细胞中,由ERK1/ERK2介导的TRIP6磷酸化会打破这种相互作用,进而增强由ENO2驱动的糖酵解以及乳酸的生成。随着细胞外乳酸水平的升高,CD8⁺T细胞上的CD44会发生乳酸化修饰(CD44 lactylation),这一过程会损害透明质酸结合能力以及AKT信号转导,最终抑制抗肿瘤免疫反应。
研究团队并未止步于此,他们进一步开发出特异性阻断多肽mPT6。在临床前模型中,mPT6通过阻断TRIP6的磷酸化,成功恢复了T细胞的功能,并且显著提高了PD - 1免疫治疗的效果。
总体而言,这些研究成果不仅揭示了KRAS突变型(KRAS/MT)结直肠癌(CRC)免疫逃逸的新机制,还进一步表明针对TRIP6–ENO2–CD44乳酸化信号轴进行靶向治疗,可能是克服免疫治疗耐药性的一种极具潜力的新策略。
值得一提的是,Nature Metabolism期刊同期刊载了来自上海交通大学医学院童雪梅教授的题为“TRIPping anti - tumour immunity through lactylation”的News & Views文章。文章指出,结直肠癌中的KRAS突变会塑造出免疫抑制性的肿瘤微环境,而吴华等人的这项新研究则揭示了KRAS突变型结直肠癌中,由TRIP6磷酸化诱导的糖酵解通过CD44的细胞外乳酸化这一机制,阻碍了CD8⁺T细胞的功能。













 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


