铁,作为人体发育和新陈代谢不可或缺的微量元素,其重要性不言而喻。然而,铁的“双面性”也不容忽视——它具有氧化还原活性,能催化活性氧生成和脂质过氧化,而这些过程与衰老的关联由来已久。
在灵长类动物衰老的进程中,铁在各组织中的积累情况一直是个谜。铁是否会在各组织中系统性地堆积?若真如此,这种积累是衰老的“幕后推手”,还是衰老带来的“附带结果”?这些问题此前尚未有明确答案。
同时,铁代谢紊乱以及铁死亡与多种年龄相关疾病的关系已被揭示。但铁死亡是一种剧烈且急性的细胞死亡形式,虽能解释特定疾病中的组织损伤,却难以完全阐释衰老这种缓慢、渐进且影响全身所有器官的慢性过程。于是,一个关键问题浮出水面:是否存在一种受调控的、铁依赖的代谢程序,它不像铁死亡那样剧烈,而是以温和、持续的方式,悄然推动细胞衰老和器官功能衰退,进而驱动整个机体走向衰老?
2026年3月11日,中国科学院动物研究所以及中国科学院北京基因组研究所的科研人员,合力在Cell子刊Cell Metabolism上发表了题为“Vitamin C inhibits ACSL4 to alleviate ferro-aging in primates(维生素C抑制ACSL4以缓解灵长类动物的铁衰老)”的研究论文,为上述问题提供了新的解答。
首次提出“铁衰老”概念,开辟衰老研究新领域
该研究首次提出并系统阐述了一种由铁过载触发、ACSL4驱动、脂质过氧化介导的衰老程序化通路,并将其命名为“铁衰老”(ferro-aging)。研究进一步证实,维生素C(VC)可直接抑制ACSL4活性,改善各组织中的铁衰老标志物,对神经、代谢和全身健康状况产生积极影响。这些发现不仅为理解氧化损伤与衰老的关系搭建了更精细的分子框架,也为衰老干预开辟了全新路径。
衰老“生锈”理论:铁积累成衰老元凶
传统观点认为衰老与氧化应激有关,但具体机制一直模糊不清。此次研究首次系统性地揭示了“铁衰老”这一全新的衰老机制。研究团队发现,在人类和猴子的衰老过程中,多种组织会出现铁元素异常积累。这些过量的铁如同催化剂,引发脂质过氧化反应,就像细胞层面发生“生锈”过程。这种慢性、低度的“生锈”与急性的铁死亡不同,它通过促进细胞衰老,导致器官功能逐渐衰退。
ACSL4蛋白:衰老的“关键加速器”
在众多参与铁代谢和脂质过氧化的分子中,研究团队锁定了关键蛋白——ACSL4。它负责将多不饱和脂肪酸转化为更易被氧化的形式,为“生锈”过程按下“加速键”。进一步实验表明,在老年小鼠中,通过CRISPR-Cas9基因编辑特异性敲低肝脏中的Acsl4基因,不仅能改善肝脏及多组织器官的衰老状态,还能显著提升老年小鼠的认知能力和运动协调性。这证明以肝脏为靶器官的ACSL4基因治疗是一种可行的衰老干预策略,且外周器官干预带来系统性获益的现象提示,延缓核心器官衰老可能带来多系统功能改善。
维生素C:ACSL4的天然“克星”
在确定ACSL4为核心靶标后,研究团队进一步筛选可干预铁衰老的小分子药物,发现维生素C是ACSL4的高效抑制剂,能有效抑制其活性。进一步机制研究显示,维生素C可直接结合ACSL4蛋白,占据其催化活性中心附近的关键口袋,从而抑制酶活性。同时,维生素C还能激活细胞的抗氧化防御系统(Nrf2通路),双管齐下对抗铁衰老。这一发现将维生素C这一广谱抗氧化剂重新定义为具有明确分子靶点的酶抑制剂,揭示了其通过直接靶向ACSL4发挥抗衰老作用的新机制。
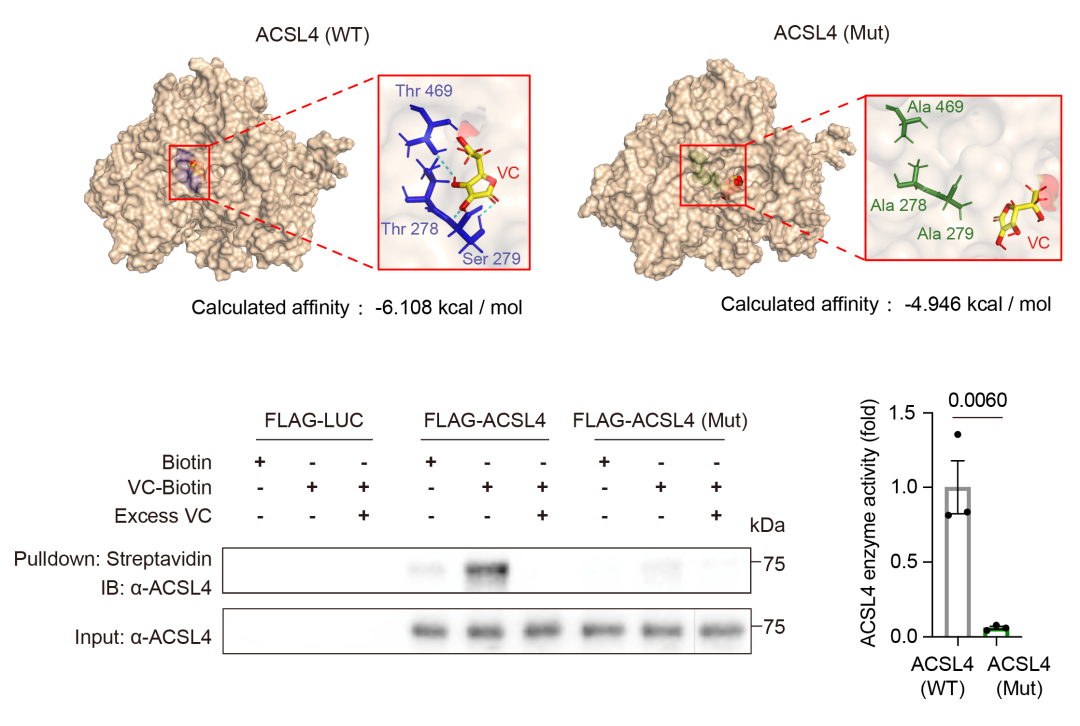
长期补充维生素C:显著减缓衰老进程
为验证维生素C在整体动物水平的效果,研究团队开展了长达40个月的干预实验。老年食蟹猴每天口服维生素C(30毫克/公斤体重),对照组则接受常规饲养。结果显示,长期补充维生素C的食蟹猴全身多个组织的铁衰老特征显著降低,大脑和肌肉中的脂质过氧化物减少,心脏等器官的衰老和炎症标志物下降,认知功能和代谢状态也得到改善。通过多组学衰老时钟分析,研究团队发现,维生素C干预逆转了其表观遗传衰老。
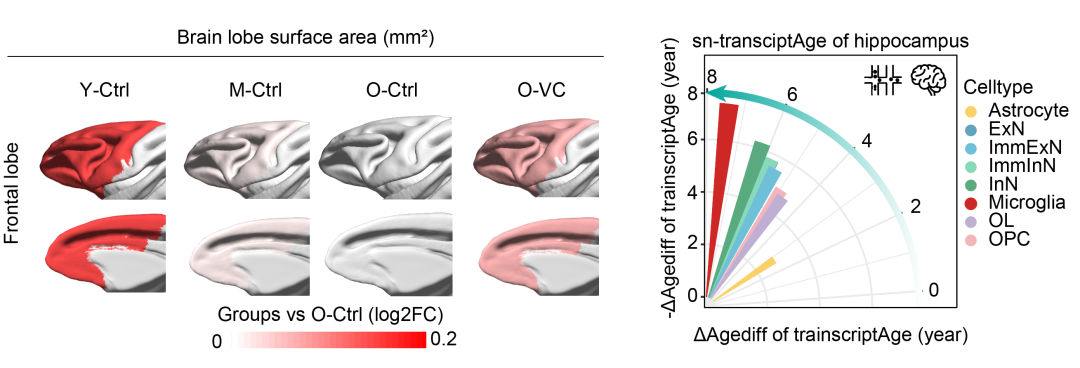
为人类抗衰老带来的启发
这项研究意义重大——它提出了全新的衰老机制,铁衰老这一概念为人们理解衰老过程提供了全新视角;研究还发现了可进行干预的靶点,ACSL4 为抗衰老药物的研发指明了新方向;同时,研究验证了维生素 C 具有抗衰老潜力,为维生素 C 在临床上的应用提供了科学支撑。
总体而言,这项研究不仅揭开了衰老的新机制——铁衰老的神秘面纱,更为我们带来了一种简单、安全且容易获取的潜在抗衰老方法——维生素 C。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


