摘要
获得性耐药是限制结直肠癌(Colorectal Cancer, CRC)靶向与化疗疗效的关键瓶颈。2026年3月7日,中南大学周钰娟、廖前进团队在《Advanced Science》上发表的题为”POU2F1 Promotes Chemoresistance in Colorectal Cancer Cells via Attenuates the MDR2 Degradation Mediated by PPP1R11 Lactylation”的研究,揭示了转录因子POU2F1通过调控一条全新的“乳酸化轴”驱动CRC化疗耐药的核心机制。研究发现,POU2F1在耐药细胞中高表达,其通过转录激活单羧酸转运蛋白4(MCT4),促进胞内乳酸外排,进而导致蛋白磷酸酶1调节亚基11(PPP1R11)的乳酸化水平降低。这一修饰的缺失削弱了PPP1R11的蛋白稳定性及其E3泛素连接酶活性,从而阻断了其对多药耐药蛋白2(MDR2)的泛素化降解。该研究不仅阐明了POU2F1介导耐药的新机制,更首次将乳酸化修饰与ABC转运蛋白的稳定性调控相关联,为逆转CRC耐药提供了全新的理论靶点。

一、核心发现:POU2F1-MCT4-PPP1R11乳酸化轴的鉴定
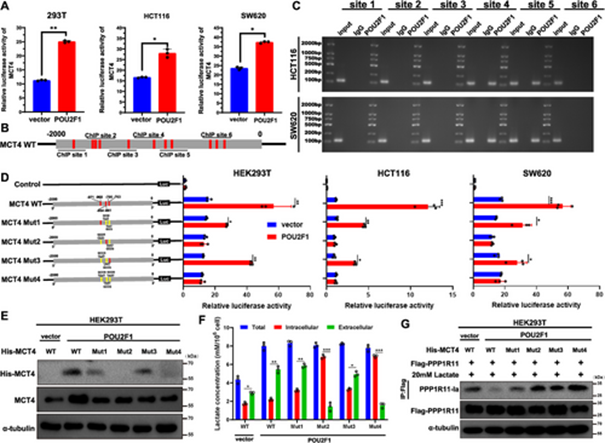
POU2F1通过促进MCT4的转录活性上调其表达
Xia L, Lin J, et al. POU2F1 Promotes Chemoresistance in Colorectal Cancer Cells via Attenuates the MDR2 Degradation Mediated by PPP1R11 Lactylation. Adv Sci (Weinh). 2026 Mar 7:e22316.
(一)POU2F1在耐药细胞中高表达,并调控MDR2蛋白稳定性
研究团队首先发现,在化疗耐药的结直肠癌细胞中,POU2F1的表达水平显著上调。不同于以往认为POU2F1主要转录调控MDR1的观点,本研究发现POU2F1主要通过一种非转录的方式影响MDR2。机制上,POU2F1并不直接调控MDR2的mRNA水平,而是通过抑制MDR2的蛋白降解,使其在细胞内累积,从而增强药物外排能力。
(二)POU2F1通过促进乳酸外排,抑制PPP1R11的乳酸化修饰
进一步的机制挖掘显示,POU2F1直接结合于MCT4的启动子区域,转录激活MCT4的表达。MCT4作为关键的乳酸转运蛋白,其高表达加速了胞质内的乳酸外排至细胞外。这一过程导致胞内乳酸浓度下降,进而降低了PPP1R11蛋白第59位赖氨酸(K59)的乳酸化修饰水平。
(三)PPP1R11乳酸化是其稳定并降解MDR2的前提
研究证实,PPP1R11是MDR2的负调控因子。正常情况下,PPP1R11的K59位乳酸化修饰对其自身蛋白稳定性至关重要。这一修饰使得PPP1R11蛋白结构更稳定,并维持其作为E3泛素连接酶的活性。活化的PPP1R11能够特异性地识别并结合MDR2,促进MDR2在K413和K538位点发生泛素化修饰,最终引导MDR2进入蛋白酶体降解途径,从而维持细胞对化疗药物的敏感性。
(四)“POU2F1-MCT4-PPP1R11乳酸化轴”的完整环路
基于上述发现,研究团队勾勒出一条完整的耐药调控环路:
耐药状态下:POU2F1高表达 → MCT4转录上调 → 胞内乳酸被大量外排 → PPP1R11的K59乳酸化水平降低。
乳酸化缺失的后果:PPP1R11蛋白失去稳定性,E3酶活性丧失 → 无法对MDR2进行泛素化标记 → MDR2蛋白累积 → 化疗药物被大量泵出细胞外 → 获得性耐药形成。
反之,若阻断该环路,例如抑制POU2F1或MCT4的功能,则可恢复胞内乳酸水平,增强PPP1R11乳酸化,促进MDR2降解,从而逆转耐药。
二、研究意义与展望
(一)理论创新
本研究首次将乳酸化修饰与ABC转运蛋白的稳定性调控直接联系起来。过去对乳酸化的研究多集中于组蛋白或转录因子对基因表达的调控,而本研究揭示了乳酸化修饰直接调控一个E3连接酶(PPP1R11)的活性,进而影响耐药蛋白(MDR2)的降解。这极大地拓展了人们对乳酸化修饰生物学功能的认识,也为理解“瓦博格效应”如何塑造耐药表型提供了全新的分子解释。
(二)临床转化潜力
该研究为克服结直肠癌化疗耐药提供了多个潜在的干预靶点:
1. 靶向POU2F1:直接抑制上游转录因子,从源头阻断该通路的激活。
2. 靶向MCT4:通过抑制乳酸外排,人为提高胞内乳酸水平,有望“恢复”PPP1R11的乳酸化,促进MDR2降解。
3. 靶向PPP1R11-MDR2互作:设计小分子干扰两者的结合,或直接靶向MDR2的泛素化位点。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


