食管鳞状细胞癌(ESCC)作为一种极具侵袭性的恶性肿瘤,在采用抗 PD-1 免疫疗法进行治疗时,不同患者间的疗效存在显著差异,而肠道微生物群很可能是影响这一疗效差异的关键因素。
2026 年 3 月,四川大学华西医院在 Cell 子刊《Cell Host & Microbe》上发表了题为《Gut microbiota-derived indole-3-lactic acid suppresses anti-PD-1 efficacy in esophageal squamous cell carcinoma》的研究论文。

此项研究揭示,肠道微生物中的唾液乳酸杆菌(L. salivarius),其代谢产物吲哚 -3- 乳酸(ILA)能够通过 AhR/NF-κB 信号轴对 T 细胞免疫产生抑制作用,进而导致食管鳞状细胞癌(ESCC)出现免疫治疗耐药现象。这一发现为攻克食管鳞状细胞癌免疫治疗耐药难题提供了全新的潜在策略。
在本次研究中,研究团队开展了全面且深入的分析工作。他们收集了 122 份接受新辅助免疫治疗的食管鳞状细胞癌(ESCC)患者的粪便样本,经过详细分析发现,在治疗无应答的患者体内,唾液乳酸杆菌(L. salivarius)存在明显的富集情况。为进一步验证这一发现,研究团队借助人源化微生物组、原位 ESCC 小鼠模型以及单细胞 RNA 测序技术展开研究。结果表明,唾液乳酸杆菌所产生的吲哚 -3- 乳酸(ILA),能够抑制肿瘤浸润的 NKG7⁺ CD8⁺ Tpex 细胞,促使其走向终末耗竭状态,最终削弱了机体的抗肿瘤免疫能力。而当使用 ILA 缺陷的唾液乳酸杆菌菌株时,ILA 的产生被消除,同时免疫治疗抵抗现象也随之消失。体外实验进一步证实,ILA 能够靶向作用于芳香烃受体(AhR),并下调 Tpex 细胞中的核 NF-κB 信号通路。通过药理性激活 NF-κB,可以恢复 Tpex 细胞的功能,逆转免疫治疗耐药性。此外,研究团队还在两个独立的验证队列中,证实了唾液乳酸杆菌 -ILA-NKG7⁺ CD8⁺ Tpex 信号轴是 ESCC 患者产生耐药的一种重要机制。
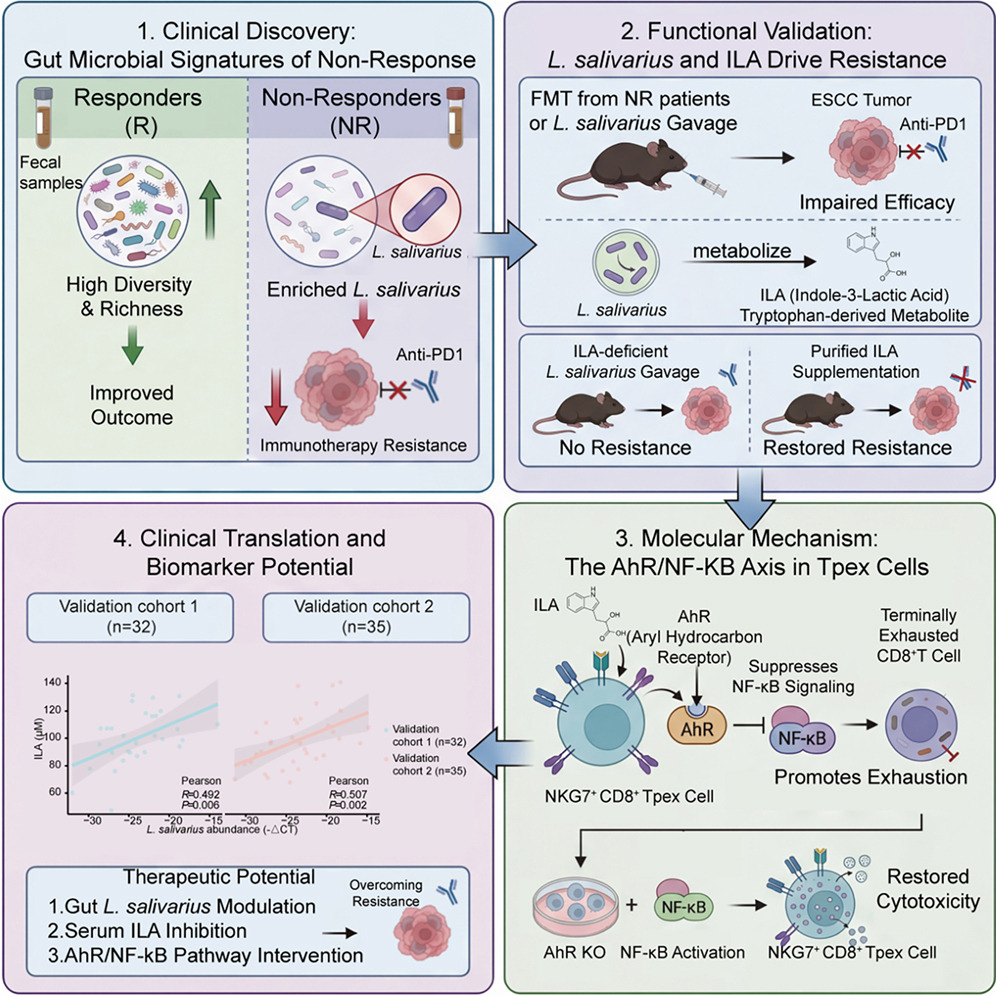
该研究的核心成果可归纳如下:
(1)肠道微生物唾液乳酸杆菌(L. salivarius)能够诱导食管癌对抗 PD-1 治疗产生耐药性。
(2)细菌来源的吲哚 -3- 乳酸(ILA)会促使 NKG7⁺ CD8⁺ Tpex 细胞走向终末耗竭。
(3)ILA 通过 AhR/NF-κB 信号轴对 T 细胞免疫发挥抑制作用。
(4)唾液乳酸杆菌 -ILA 信号轴为增强免疫疗法提供了新的作用靶点。
总体而言,这些研究成果充分表明,唾液乳酸杆菌(L. salivarius)及其代谢产物吲哚 -3- 乳酸(ILA)是肿瘤微环境(TME)的关键调控因子,为克服食管鳞状细胞癌(ESCC)的免疫治疗耐药问题提供了极具潜力的策略。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


