在科研领域,单细胞蛋白组技术凭借其精准解析单个细胞蛋白表达特征的优势,成为探究免疫机制、挖掘疾病生物标志物的核心工具。其中,Abseq单细胞蛋白组技术表现突出,能够实现对单细胞水平蛋白表达的高效、精准检测,为复杂疾病的机制研究提供关键支撑。在Nature的一项重要研究中,科研人员充分发挥Abseq单细胞蛋白组技术的独特优势,结合流式分析技术,取得了突破性发现——成功鉴定出肿瘤特异的Treg细胞,并确定了其生物标志物,这一成果为未来肿瘤靶向治疗带来了新的曙光。
值得一提的是,在这项研究中,Abseq单细胞蛋白组技术与流式分析技术发挥了关键作用,二者配合默契、相得益彰。大量实验结果显示,两种技术相互验证,为研究结果提供了坚实的支撑。其中还在单细胞RNA测序样本处理环节,全部采用流式分选技术进行样本富集,这一操作不仅显著提升了单细胞数据分析的精度,还有效节约了测序成本。而Abseq单细胞蛋白组技术与流式技术强强联合,为单细胞研究打造了一套全方位、多维度的解决方案,诚邀广大科研、临床及工业领域的用户踊跃试用!
接下来,详细介绍这篇发表在Nature期刊上的文章——“Extricating human tumour immune alterations from tissue inflammation”。该研究对头颈部鳞状细胞癌(HNSCC)以及部位匹配的非恶性炎症口腔粘膜(OM)的免疫特征展开了系统性分析。研究过程中,科研人员发现了一群独特的肿瘤特异Treg亚群。这群细胞具有显著的免疫抑制特性,能够对TCR信号做出应答,并且处于活跃增殖状态。更为重要的是,研究团队借助Abseq技术创新性地鉴定出了该亚群的生物标志物,这一发现为肿瘤精准治疗开辟了全新的思路。
研究背景
免疫疗法在癌症治疗领域已取得了令人瞩目的成功,然而,其发展之路并非一帆风顺,仍面临着诸多挑战。其中,一个亟待解决的问题是,免疫疗法所靶向的通路并非肿瘤专属,在其他组织微环境中同样存在。尽管目前已有大量研究聚焦于肿瘤微环境的炎症反应,但我们对肿瘤特异的免疫变化依然知之甚少,这在一定程度上限制了免疫疗法在肿瘤治疗中的精准应用和进一步发展。
研究方法
(1)单细胞蛋白组与RNA测序联合技术
(2)流式分析技术
实验结果
1. OM和HNSCC的免疫表型趋于一致
在肿瘤组织中,功能衰竭的T细胞和Treg细胞往往被视为抗肿瘤免疫反应失效的关键因素,且T细胞的效应功能与抗原呈递细胞(APCs,Antigen Presenting Cells)紧密相关。为深入探究相关免疫机制,作者运用两组包含30个参数的高维流式panel,对OM和HNSCC组织及血液中的免疫细胞图谱进行了深度剖析。
研究结果令人意外,OM和HNSCC组织的免疫表型竟基本相似。在CD45+活细胞中,CD3+ T细胞、CD19+ B细胞以及CD56+ NK细胞的比例,还有CD4/CD8比例都大致相同(Fig 1a)。在APC细胞方面,cDC2s、DC3及CD16+非常规单核细胞的比例在OM和HNSCC组织中也基本一致,不过CD141+ cDC1s在HNSCC肿瘤组织中的比例略低(Fig 1b)。
为了精准鉴定特定免疫亚群之间的差异,作者借助了FAUST这一机器算法。该算法能够以无监督的方式发现并注释统计上相关的细胞表型。结果显示,在T细胞panel中,HNSCC组织中富集了一个CD8+ T细胞亚群和四个CD4+ Treg亚群;在APC细胞panel中,HNSCC组织中富集了CD40及PD-L1共表达的CD14+细胞以及cDC2s、DC3细胞。

2. 分析肿瘤富集的APC与T细胞之间的细胞通讯
为进一步探究上述免疫细胞的一致性与区别,作者采用了单细胞RNA测序技术,不仅发现了与流式结果相一致的免疫表型,还鉴定出了肿瘤特有的转录特征和蛋白表达特征。随后,作者运用NicheNet方法对肿瘤特异性的T细胞和APC细胞通讯展开了研究。
研究发现,HNSCC肿瘤T-APC细胞通讯中富集的配体受体相互作用情况如下:ICOS配体通过ICOS发挥作用,IL-18通过IL18-R1发挥作用,IL1B通过IL-1受体1型及2型发挥作用。
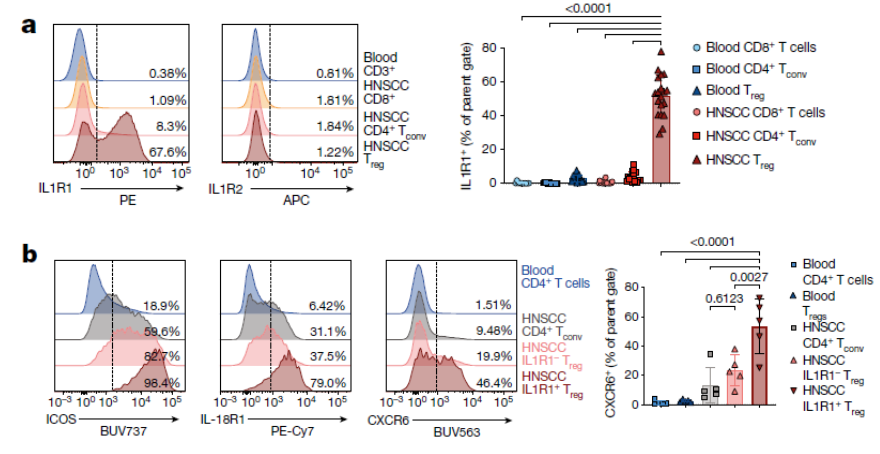
鉴于流式和单细胞RNA测序(scRNA-seq)均显示HNSCC肿瘤Tregs细胞存在差异,作者进一步对Treg-APC的相互作用进行了验证。通过流式分析发现,IL1R1(在T细胞与APC通讯中富集)特异性地表达在肿瘤浸润的Treg细胞上(Figure 2a)。几乎所有的IL1R1+ T细胞都共表达ICOS、IL-18R1以及趋化因子受体CXCR6(Figure 2b)。
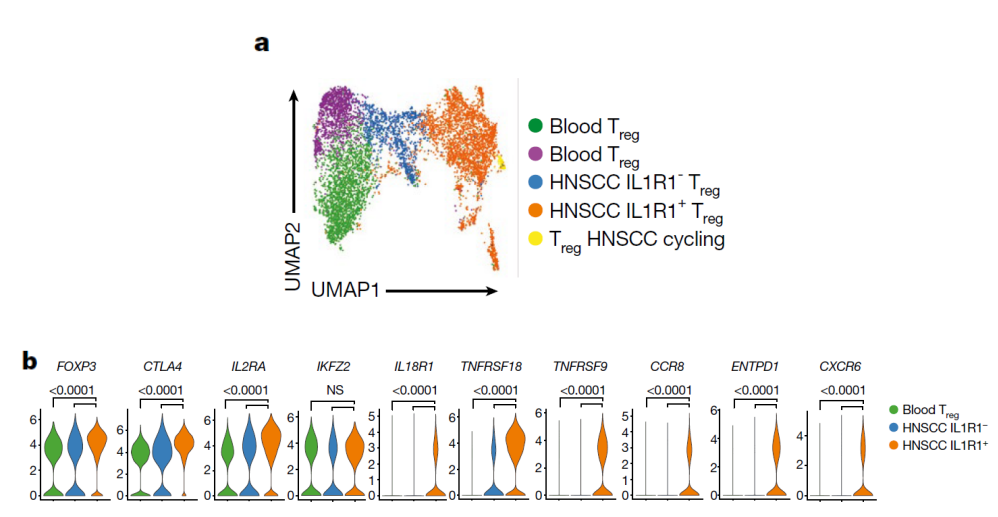
3. IL1R1+ Treg细胞的单细胞转录组与蛋白组特征分析
为了更清晰地区分肿瘤浸润的IL1R1+ Treg细胞和IL1R1- Treg细胞,作者从OM、HNSCC以及外周血中分选了Treg细胞,并结合免疫响应基因panel进行单细胞RNA测序。
结果显示,肿瘤中的IL1R1+ Treg细胞(Figure 3a,橙色亚群)和IL1R1- Treg细胞(Figure 3a,蓝色亚群)各自形成了独立的亚群,与外周血Treg细胞存在明显差异。在IL1R1+ Treg细胞中,选择性富集了超过50个转录本(Figure 3b),其中包括TNFRSF18(编码GITR)和TNFRSF9(编码4-1BB);这类细胞在蛋白水平也呈现出特异性表达特征,表明IL1R1+ Treg细胞代表了肿瘤浸润Treg细胞中一群具有独特转录组特征的免疫亚群。
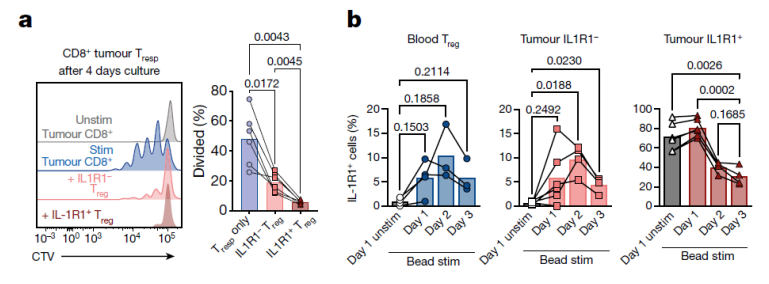
4. IL1R1+ Treg细胞高度抑制性的功能研究
在CD8+ T细胞及CD4+ T细胞的体外增殖抑制实验中,IL1R1+ Treg细胞展现出了比IL1R1- Treg细胞更有效的抑制效果(Figure 4a)。另外,通过anti-CD3、anti-CD28和anti-CD2磁珠刺激,肿瘤浸润IL1R1+ Treg细胞中IL1R1的表达在第1天升高,第2-3天下降(Figure 4b)。这一现象提示,IL1R1+ Treg细胞能够应答TCR信号并调控IL1R1的表达。
为进一步研究肿瘤浸润IL1R1+ Treg细胞应答激活信号的免疫反应,作者利用佛波酯(PMA)及离子霉素进行短时间刺激,然后运用单细胞转录组联合Abseq膜蛋白测序技术,系统分析了这类细胞的转录组和蛋白组变化。对CD4+ T细胞及Treg细胞进行无监督聚类分析后,结果显示存在三个Treg亚群:IL1R1-、IL1R1+及活跃增殖的IL1R1+ Treg细胞。
PMA及离子霉素刺激后,Treg细胞的差异表达蛋白及差异表达基因情况如图Figure 5a-b所示。例如,这类细胞高表达TNFRSF9及CTLA4转录本,并且通过Abseq技术检测证实,其CTLA4蛋白显著高表达。这表明IL1R1+ Treg细胞处于激活状态且具有功能活性,并且存在一个活跃增殖的亚群。

通过Abseq单细胞膜蛋白检测结果,作者成功鉴定出一组生物标记物,能够唯一地识别IL1R1+ Treg细胞。仅使用2个膜表面蛋白,就可以从组织和外周血所有CD45+的免疫细胞中标记出这类细胞。并且通过流式分析验证了标志物的特异性:几乎所有的CD45+IL1R1+ICOS+细胞都是Treg细胞(Figure 6a)。这一发现依托Abseq技术的精准蛋白检测能力,为未来靶向肿瘤特异性Treg细胞的治疗提供了全新的思路和靶点。

最后,作者通过实验验证并结合公开的scRNA-seq数据集(涵盖19种不同的肿瘤类型)分析发现,IL1R1+ Treg细胞并非仅特异性存在于HNSCC肿瘤中,而是以不同比例分布于各种实体肿瘤中。清除肿瘤浸润性Treg细胞被认为是一种极具前景的抗肿瘤治疗方法,而该研究借助Abseq技术鉴定出的肿瘤特异Treg细胞生物标志物,为靶向肿瘤特异Treg细胞、同时不影响其他Treg细胞的免疫调节功能提供了可能,为肿瘤免疫治疗的精准化发展奠定了基础。
单细胞Abseq和流式检测技术哪里有?
乐备实提供单细胞Abseq检测和流式检测服务,且Abseq数据可直接导入FlowJo分析。
免疫研究不用愁,乐备实 Ab-seq 全搞定!多色 Panel 自由组合,一站式解锁免疫全景。













 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


