一、cGAS-STING信号通路在炎症性疾病中的治疗靶点作用
在许多生物体中,外源DNA的检测是免疫应答的关键环节。在哺乳动物细胞中,这一功能主要由cGAS-STING信号通路介导。该通路作为连接DNA识别与诱导先天免疫防御反应的核心机制,发挥着至关重要的作用。
cGAS-STING通路是由环鸟苷酸-腺苷酸合成酶(cGAS)和干扰素基因刺激因子(STING)两种蛋白质构成的分子信号传导途径。cGAS能够识别细胞内的双链DNA。当外源性微生物DNA进入细胞后,cGAS与之结合并被激活,启动其酶活性,生成特定的信号分子。这些信号分子随后激活位于内质网上的STING蛋白,进而触发下游信号级联反应,诱导多种与炎症相关的基因表达,从而启动机体对病毒和细菌感染的防御机制。
cGAS-STING通路的一个显著特征在于,其激活由生命活动的基本分子——DNA所触发,这一特性使其区别于其他多种先天免疫信号机制。
免疫学研究显示,cGAS-STING通路对于理解感染性疾病及自身免疫性疾病的发病机制具有重要价值,并已成为相关疾病治疗的关键干预靶点。
Andrea Ablasser教授发表于Nature Reviews Immunology(IF:100.3)的综述文章The cGAS-STING pathway as a therapeutic target in inflammatory diseases系统总结了cGAS-STING信号通路的主要组成分子,梳理了在不同病理生理条件下该通路活性的诱导机制,并探讨了针对该通路的药理干预策略及其在炎症性与自身炎症性疾病治疗中的潜在应用价值。

二、cGAS-STING信号通路概述
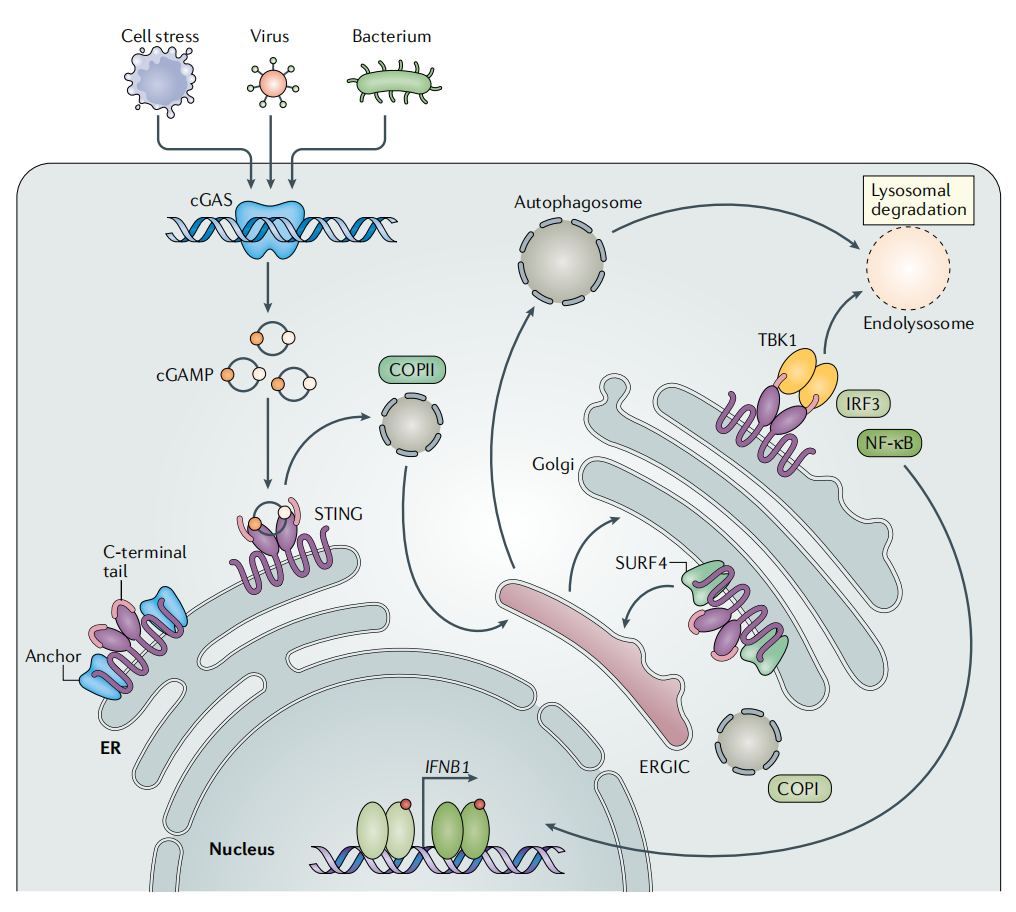
在免疫应答过程中,细菌DNA通常通过吞噬体膜的破裂进入吞噬细胞的胞质溶胶;病毒则通过直接注射自身DNA或逆转录其RNA实现遗传物质的递送。凋亡或坏死的细胞被吞噬细胞摄取后,通常被运输至溶酶体进行降解。当凋亡或坏死细胞数量庞大,其所含DNA总量超过溶酶体中DNA酶的降解能力时,未降解的DNA将渗漏并积聚于胞质溶胶中,从而激活cGAS-STING信号通路。
cGAS是一种天然免疫传感器,能够识别多种来源的胞质双链DNA(dsDNA),包括病毒、细菌、线粒体、微核及逆转录来源的DNA。dsDNA与cGAS结合后,激活cGAS的酶活性,催化ATP与GTP合成第二信使cGAMP。
位于内质网(ER)膜上的同型二聚体蛋白STING可识别并结合cGAMP,结合后STING发生构象改变,进而触发其寡聚化。随后,STING通过内质网-高尔基体中间隔室(ERGIC)转运至高尔基体。到达高尔基体后,STING在两个半胱氨酸残基(Cys88和Cys91)处发生棕榈酰化修饰。其C末端招募TANK结合激酶1(TBK1)并与之相互作用,TBK1随后磷酸化STING蛋白C末端的Ser366残基,并进一步磷酸化干扰素调控因子3(IRF3)。磷酸化的IRF3形成二聚体,发生核移位,诱导靶基因的表达。此外,STING还可激活核因子κB(NF-κB),后者亦能上调I型干扰素(IFN)的表达水平。
cGAS-STING信号通路与自噬过程密切相关。该通路不仅作为一种细胞自主防御机制诱导自噬,其自身活性也受到自噬相关组分的调控。
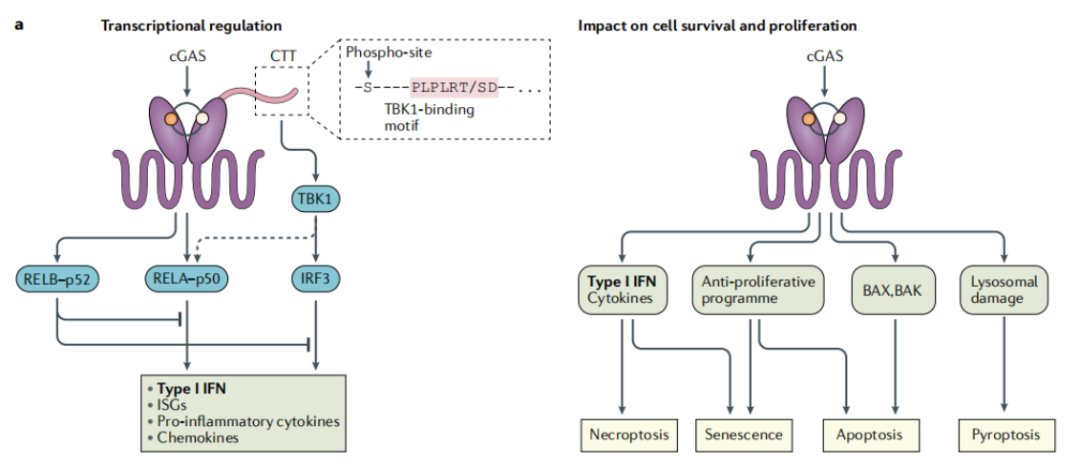
在整个进化历程中,cGAS-STING通路的激活主要发挥抗病毒感染的作用,并与抗病毒细胞程序密切相关。
三、细胞间cGAMP信号传递
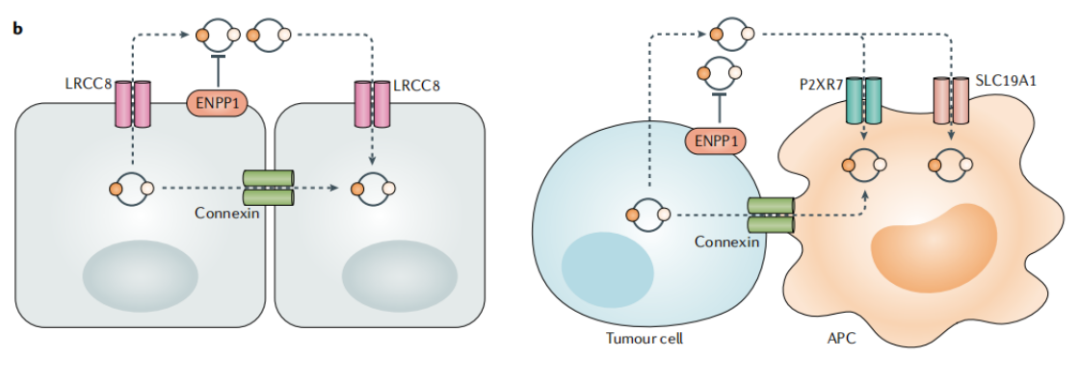
cGAS与STING之间通过一种可传递的第二信使分子——cGAMP相连接。细胞间cGAMP信号传导最初被证实由缝隙连接介导。缝隙连接是由连接蛋白构成的细胞间通道,能够直接连通相邻细胞的胞质。这类连接不仅存在于相同类型的细胞之间,也可见于在生理性免疫反应中相互作用的异质性细胞群体中。
在细胞外空间中,cGAMP可被外核苷酸焦磷酸酶/磷酸二酯酶家族成员1(ENPP1)降解。与此同时,多种细胞类型利用由LRRC8亚基组成的电压依赖性阴离子通道(VDAC)实现cGAMP的导入与导出。研究还表明,肿瘤细胞能够输出cGAMP,而骨髓细胞则通过SLC19A1或P2XR7通道摄取cGAMP。
四、cGAS-STING对细胞扰动的感知
尽管通过DNA配体介导的变构激活机制使cGAS-STING通路能够作为经典的模式识别受体发挥作用,哺乳动物细胞还受益于cGAS对特定生理背景下非自身及自身DNA的识别所激发的危险信号感知。重要的是,这些不同的激活模式并非相互排斥,在某些情况下可能以冗余方式触发cGAS活性,在另一些情况下则可能表现出协同效应。
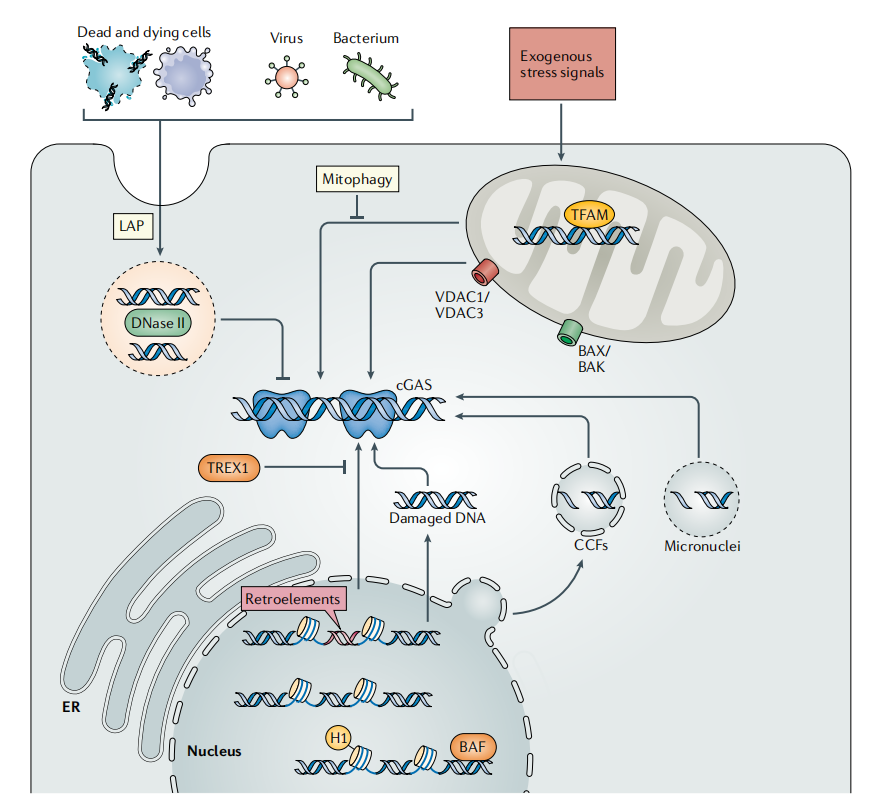
死亡或凋亡细胞的尸体被吞噬细胞摄取后,通过LC3相关吞噬作用(LAP)靶向输送至溶酶体,在此过程中DNase II处于活跃状态。通过这一途径有效处理细胞外DNA,有助于限制cGAS-STING通路的活性。在线粒体中,转录因子A线粒体(TFAM)通过形成类核结构稳定线粒体DNA(mtDNA),这对于抵消mtDNA应激及异常cGAS激活具有重要意义。mtDNA可通过线粒体内膜突出,进而经由BAX/BAK形成的大孔释放,也可通过线粒体外膜中的电压依赖性阴离子通道(VDAC)孔道释放。此外,线粒体通透性转换孔(MPTP)可能是mtDNA穿越线粒体内膜的另一种途径。
五、疾病中cGAS-STING通路的激活
在细胞及生物体层面,对DNA丰度、区室化隔离及清除过程的精细调控本身具有高度复杂性,因此易受多种因素干扰而失衡。尽管不同病理过程的触发因素具有疾病特异性,但已有证据表明,cGAS-STING通路作为驱动因素,在与多种疾病相关的急性和慢性、低级别炎症状态中表现出相当程度的一致性。
六、未来展望
近年来,针对cGAS-STING信号通路的关注与研究兴趣显著增长。该通路已被证实为先天免疫系统中一个核心的危险感知机制。然而,仍需进一步研究以严谨验证从动物模型向人类疾病临床意义的转化,并提供更精确的证据阐明cGAS-STING通路在疾病发病机制中的致病作用。
未来的关键方向之一,是深入理解实现治疗获益所需的最低通路抑制水平。过度抑制该通路可能增加宿主对感染的易感性,从而在人类中引发不良后果。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


