在生物医药领域,细胞表面蛋白是当之无愧的 “明星靶点”—— 超过 60% 的治疗药物都以它为作用对象,在疾病诊断、靶向治疗中发挥着不可替代的作用。而适配体作为能精准识别这些靶点的 “分子探针”,凭借合成简便、稳定性高、可化学修饰等优势,早已成为科研和临床应用的宠儿。
但长期以来,传统适配体筛选方法(如 SELEX)却陷入了 “低效困境”:不仅通量低,单次实验往往只能筛选出 1-2 个适配体,还容易破坏蛋白天然构象,导致筛选结果与生理状态脱节,大量低丰度蛋白靶点更是被直接忽略。
原理
研究团队提出假设:将 CRISPR 介导的基因扰动与单细胞多组学分析相结合,可突破传统适配体筛选的局限。通过在单个细胞中同时分析基因扰动效果、基因表达谱和蛋白结合事件,建立 SPARK-seq 平台,实现天然细胞环境中适配体-靶点相互作用的高通量映射。该整合设计不仅能够识别低丰度靶点的结合物,还能将适配体发现与动力学分析直接关联,同时开发深度学习框架 SPARTA,用于处理高通量数据、预测适配体结合特性并设计优化变体,加速精准分子工具的开发进程。
下面我们来看下具体的SPARK-seq 工作流程设计:
SPARK-seq 的工作流程包含适配体库构建、富集、单细胞测序与数据分析四个核心步骤(图 1)。首先,设计包含 46 个随机核苷酸核心区域、两侧为 PCR 引物结合区和捕获序列的适配体库;通过四轮 Cell-SELEX 技术富集对目标细胞具有特异性结合能力的适配体(图 1A、B)。随后,将富集后的适配体库与经 CRISPR 敲除 13 种表面蛋白的混合细胞群体共孵育,利用 10X Genomics 5' 端测序技术同时捕获 gRNA(基因扰动标记)、mRNA(基因表达谱)和适配体序列(图 1C)。最后,通过计算流程校正细胞条形码,将每个细胞的基因扰动、基因表达与适配体结合谱关联,并利用 SPARTA 算法进行差异分析与适配体-靶点配对(图 1D、E)。实验通过三种 spike-in 序列验证了适配体测序的误差率约为 6%,三次重复实验中前 10,000 个独特序列的重现性达 99%,证实了测序数据的可靠性。
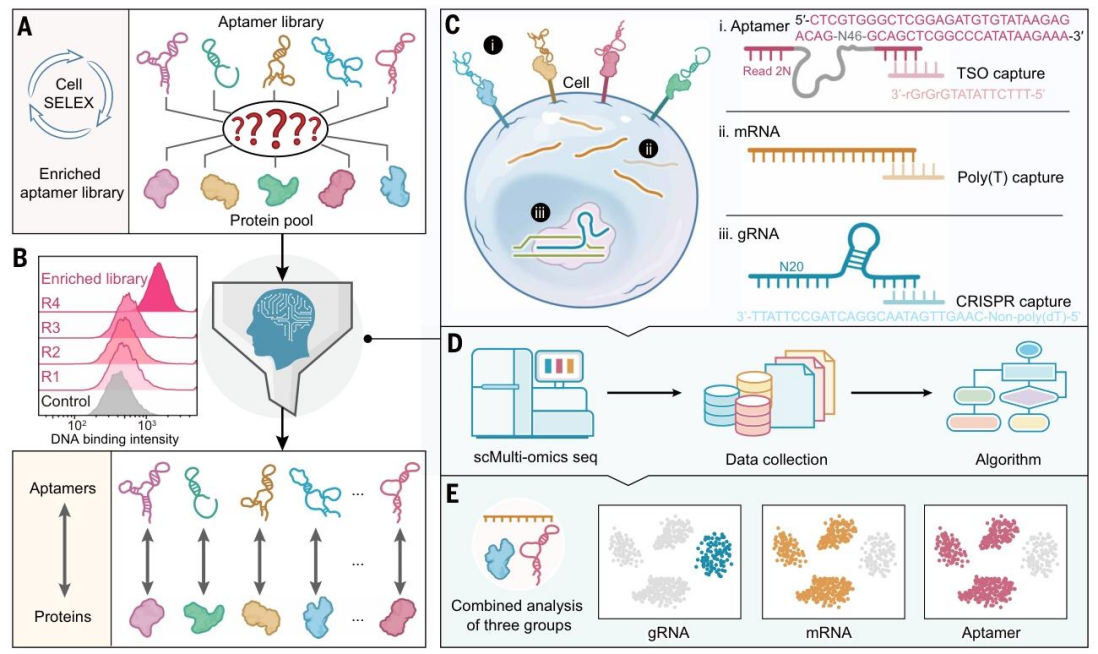
图 1. SPARK-seq 工作流程概述
概念验证实验
为验证 SPARK-seq 能够建立基因敲除、细胞表型与适配体结合之间的直接关联,研究以蛋白酪氨酸激酶7(PTK7)为靶点,在人 SUM159PT 细胞和小鼠 EMT6 细胞中进行 CRISPR 敲除,并使用 PTK7 特异性适配体 sgc8c 进行验证(图 2)。Western blot 结果显示,两种细胞系中 PTK7 的表达水平在敲除后显著降低(图 2A);流式细胞术证实,sgc8c 对 PTK7 敲除细胞的结合能力大幅下降,且能有效区分 PTK7 阳性与阴性细胞群体(图 2B、S2C)。将 sgc8c 修饰为适配体sgc8c-S以适配单细胞测序后,表面等离子体共振(SPR)实验表明其结合亲和力与天然 sgc8c 相当(图 2S、D、E)。混合不同 PTK7 表达水平的人源和鼠源细胞与 sgc8c-S 共孵育后进行 SPARK-seq,UMAP 分析成功区分人源与鼠源细胞(图 2D),且 PTK7 gRNA 阳性细胞的 sgc8c-S 结合水平显著低于对照细胞(图 2E、F、G),证实 SPARK-seq 可在单细胞水平同时检测适配体结合、gRNA 表达和 mRNA 水平,并将适配体与特定敲除细胞群体配对。
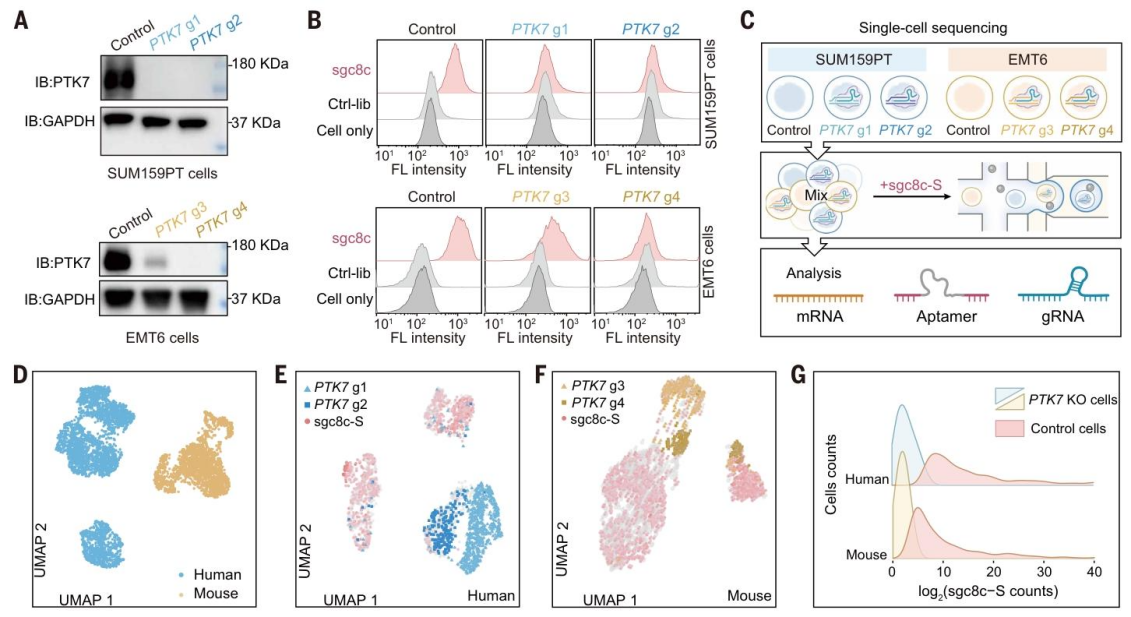
图 2. 基于 sgc8c 适配体的 SPARK-seq 概念验证
高通量适配体-靶点映射
研究通过 SPARK-seq 对富集后的适配体库进行高通量筛选,构建了包含 13 种表面蛋白(9 种高富集膜蛋白 + 4 种不同富集水平蛋白)的 CRISPR 敲除细胞池,经测序后保留 8466 个高质量单细胞和 10,000 个高丰度独特适配体序列(占总读数的 68.84%)(图 3)。利用 BLAST-short-MCL 算法将这些序列聚类为 1906 个适配体家族(图 3A、B),通过 SPARTA 算法整合结合差异计算、质量控制和评分系统,最终识别出 12 个适配体家族与9 种扰动细胞群体的结合差异(图 3C、D、E)。具体映射结果为:家族 5、13、17 结合 CDCP1;家族 3 结合 ITGA3 和 ITGB1;家族 2、6、7 结合 NRP1;家族 11、14 结合 NRP2;家族 1、15 结合 PTK7;家族 4 结合 PTPRD、PTPRF 和 PTPRS(图 3F、G),成功实现了高通量适配体-靶点相互作用映射。
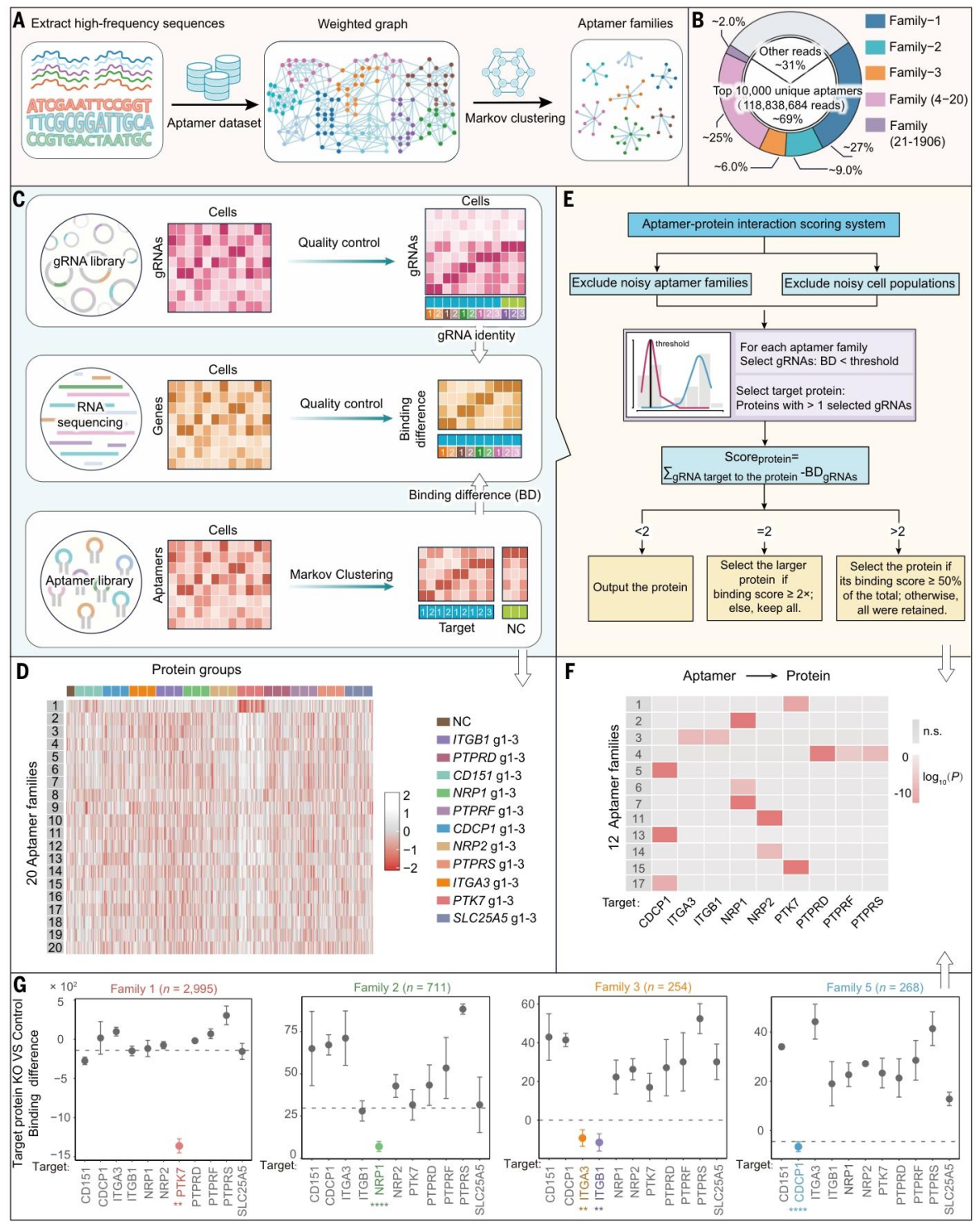
图 3. 高通量适配体 - 靶点映射流程
适配体 - 靶点相互作用验证
为证实映射结果的准确性,研究对每个靶点选择不同结合能力的适配体,通过流式细胞术、SPR 和微量热泳动(MST)进行验证(图 4)。以 PTK7 为例,选择 log₂倍变化(FC)为 2.3060 的 Apt-1-1 和 log₂FC 为 0.1049 的 Apt-15-27,流式细胞术显示两者均特异性结合 PTK7 阳性细胞,不结合敲除细胞(图 4B),SPR 和 MST 证实其对 PTK7 的结合亲和力达纳摩尔级(图 4C)。对于多靶点结合的适配体家族,如家族 3 的 Apt-3-3,流式细胞术显示其无法结合 ITGA3 或 ITGB1 敲除细胞(图 4N),SPR 证实其特异性结合整合素复合物(图 4O);家族 4 的 Apt-4-5 可结合 PTPRD、PTPRF、PTPRS 三种旁系同源蛋白,且 SPR 检测到不同的结合动力学参数(图 4Q、R、T、U、W、X)。此外,在生理温度(37℃)下的流式细胞术和实时相互作用细胞术(RT-IC)验证表明,这些适配体的结合特性与体外实验结果基本一致(图 4Y),最终证实 SPARK-seq 成功映射了 5535 个适配体与 8 种表面蛋白的特异性相互作用(图 4Z)。
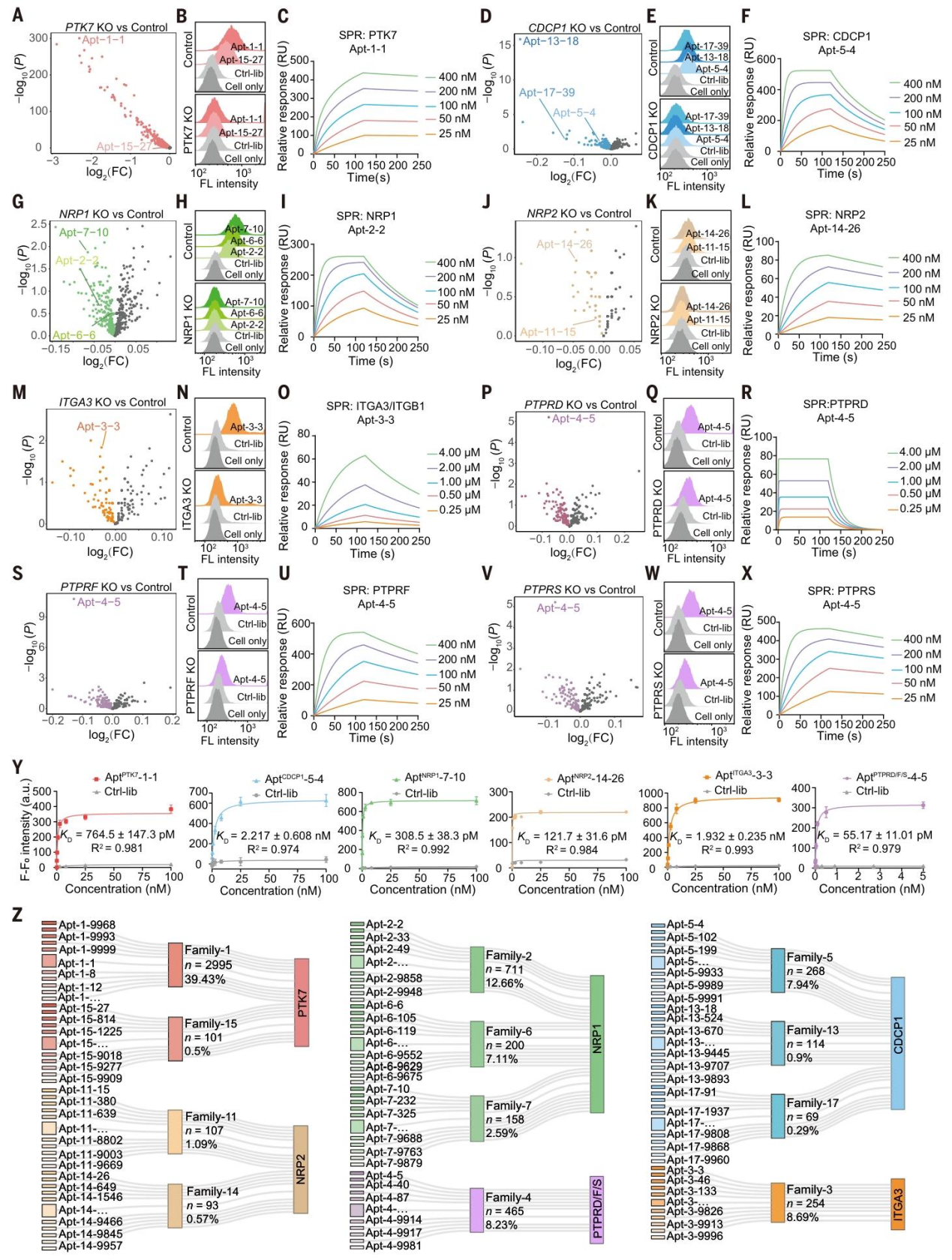
图 4. 适配体 - 靶点相互作用验证
适配体特异性正交验证
研究采用三层验证策略证实 SPARK-seq 筛选适配体的分子特异性(图 5)。流式细胞术竞争实验中,未标记的同源适配体可剂量依赖性降低荧光标记适配体的结合信号,而 10 倍过量的非同源适配体无此效果(图 5A);生物素化适配体下拉实验结合免疫印迹,证实适配体可在天然蛋白质组中选择性识别目标蛋白;SPR 交叉结合实验显示,12 个代表性适配体家族仅与各自的目标蛋白发生高亲和力结合,与非目标蛋白的结合信号与阴性对照相当(图 5B)。针对高度同源的 NRP1 和 NRP2,SPARK-seq 筛选的适配体无交叉反应(图 5D),且 NRP1 适配体可竞争性阻断 VEGF165 结合,NRP2 适配体结合非经典位点(图 5E、F)。定量分析显示,这些适配体对应的目标蛋白在细胞表面的丰度跨度超过两个数量级(图 5G),证实其对不同丰度靶点的识别能力。

图 5. 适配体特异性验证
捕获多样化蛋白靶点
研究分析了 8 个已验证靶点的理化性质,发现其等电点跨度为 4.5-8.5,疏水性与适配体捕获效率无相关性(图 S12A、B),表明 SPARK-seq 的性能不受目标蛋白电荷和疏水性影响。AlphaFold 结构模型显示,这些靶点具有免疫球蛋白折叠、纤连蛋白重复序列等稳定的细胞外结构域,且表面存在带正电的区域,为适配体结合提供了静电互补基础(图 S12C、D、E)。通过质谱和流式细胞术定量证实,目标蛋白的细胞表面丰度从 PTPRD 的 <1000 拷贝 / 细胞到 ITGA3 的> 10⁵拷贝 / 细胞,跨度超过 100 倍(图 5G、图 S12F、G、H),且 SPARK-seq 成功捕获了传统生化技术易遗漏的 CDCP1 等靶点,体现了其在复杂天然环境中识别靶点的优势。
优先富集慢解离速率适配体
研究发现 SPARK-seq 对适配体的富集与解离速率(koff)密切相关,而非平衡亲和力(KD)(图 6)。针对 PTK7 的 3096 个适配体,选择 8 个不同 log₂FC 值的适配体进行分析,流式细胞术证实 - log₂FC 值与荧光强度呈强相关(R²=0.95)(图 6B),SPR 和 RT-IC 实验显示 - log₂FC 值与 koff 显著相关(R² 分别为 0.88 和 0.87),而与 KD 无显著关联(图 6C、D、E、F)。这一相关性在 CDCP1、NRP1、NRP2、PTPRF 等多个靶点中均成立(图 6G-J)。与传统基于丰度筛选的方法相比,SPARK-seq 筛选的高 - log₂FC 值适配体具有显著更慢的解离速率(图 6K-P),部分靶点的解离速率约为传统方法的 1/10。此外,SPARTA 的生成模块可设计功能变体,如 SPARK-Apt-18 展现出最慢的解离速率,为体内成像、靶向药物递送等应用提供了优势。
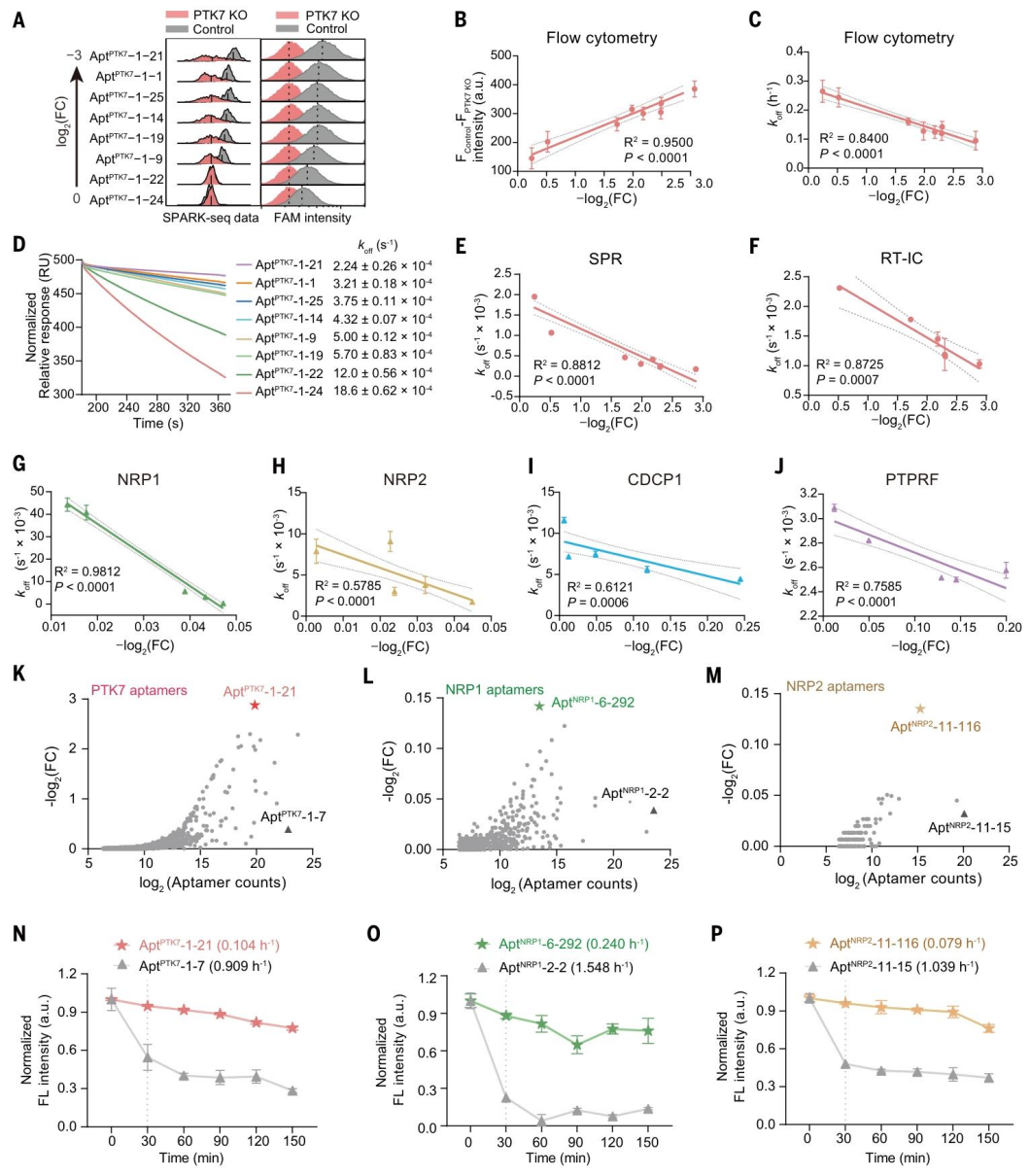
图 6. 具有不同解离动力学特性的适配体鉴定
总结
SPARK-seq 作为《Science》发表的高通量适配体研发平台,核心优势集中于三点:
高通量精准映射:整合 CRISPR 基因扰动、单细胞多组学与 AI 算法,单次实验即可完成 5535 个适配体与 8 种表面蛋白的特异性配对,覆盖超两个数量级蛋白丰度;
优质特性富集:优先筛选慢解离速率适配体(与解离速率相关性 R²=0.8-0.9),结合亲和力达纳摩尔级,且能精准区分同源旁系蛋白,无交叉反应;
智能优化升级:配套 SPARTA 深度学习框架,以 97% 准确率预测适配体结合潜力,还能生成性能更优的功能变体,大幅缩短研发周期。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


