转化生长因子-β(TGF-β)信号通路是真核细胞内高度保守、功能关键的信号传导系统,广泛调控细胞增殖、分化、凋亡、迁移、免疫应答、细胞外基质合成、组织修复等生命过程,与癌症、器官纤维化、自身免疫病等多种疾病的发生发展密切相关。
一、TGF-β信号通路核心组成
TGF-β信号通路由配体、受体、效应分子三部分构成,是信号传递的结构基础。
1. 配体
包括TGF-β1/2/3、激活素(Activins)、抑制素(Inhibins)、骨形态发生蛋白(BMPs)等,通过结合特异性受体启动信号。
2. 受体
为跨膜丝氨酸/苏氨酸激酶受体,分为Ⅱ型受体(TβRII)与型受体(TβRI),配体结合后形成受体复合物并激活下游信号。
3. 效应分子:Smad蛋白家族
Smad是通路核心效应因子,分为三类:
受体调节型Smad(R-Smad):TGF-β通路为Smad2/3;BMP通路为Smad1/5/8,可被受体磷酸化激活。
共同介导型Smad(Co-Smad):主要为Smad4,与激活的R-Smad形成复合物,介导核内信号传递。
抑制型Smad(I-Smad):Smad6/7,负向调控通路,阻断R-Smad活化或促进受体/蛋白降解。
二、TGF-β信号转导机制
TGF-β信号通过经典Smad依赖途径与非经典非Smad依赖途径传递,两条通路协同调控细胞功能。
(一)经典途径:Smad依赖信号转导
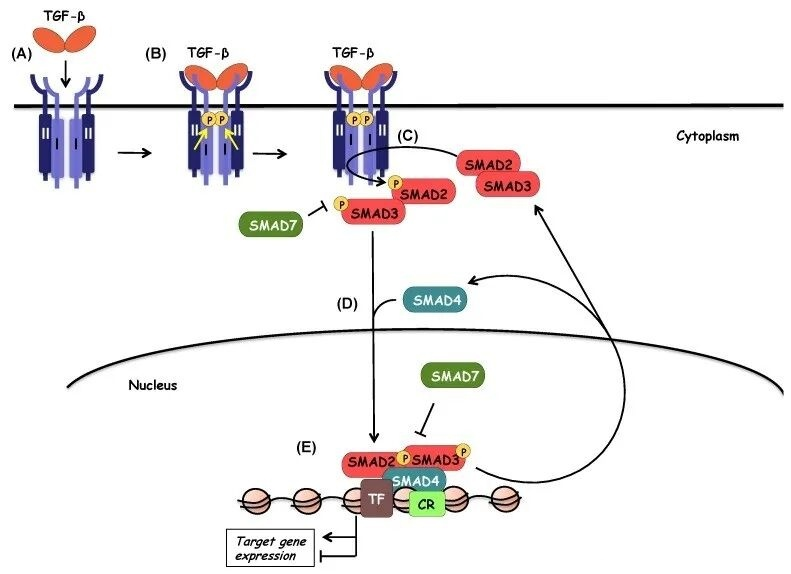
1. 配体结合与受体活化
激活的TGF-β配体结合细胞膜TβRII,招募并磷酸化TβRI,形成异源四聚体受体复合物。
2. Smad磷酸化与复合物形成
活化的TβRI磷酸化Smad2/3,使其构象改变并暴露核定位信号,随后与Smad4结合形成三元活性复合物。
3. 核转位与基因转录调控
Smad复合物进入细胞核,结合靶基因启动子(如CAGA盒),并与转录共激活/抑制因子协同,调控下游基因表达。
4. 负向调控
Smad6/7通过竞争性结合受体、阻断Smad复合物形成、介导泛素化降解等方式,终止信号传导。
(二)非经典途径:非Smad依赖信号转导
TGF-β可独立激活多条下游激酶通路,快速响应胞外信号:
1. MAPK通路:激活ERK、JNK、p38,调控细胞增殖、应激与炎症。
2. PI3K-Akt通路:参与细胞存活、代谢与抗凋亡调控。
3. Rho GTPases通路:RhoA、Rac1、Cdc42调节细胞骨架与迁移。
4.其他通路:NF-κB调控免疫炎症;STAT通路参与免疫细胞信号传递。
三、TGF-β信号通路的生理与病理功能
1. 细胞增殖与分化
生理状态下,TGF-β抑制细胞周期、抑制增殖,并促进干细胞与体细胞定向分化,维持胚胎发育与成体组织稳态。
2. 细胞凋亡与存活
正常组织:上调促凋亡基因(BIM、BIK、DAPK)诱导凋亡。
病理状态:肿瘤微环境中转为促存活信号,支持癌细胞生存。
3. 免疫调节
核心免疫抑制因子:抑制T细胞活化增殖、调控B细胞分化与抗体产生、调节巨噬细胞吞噬与抗原呈递,维持免疫耐受。
4. 细胞迁移与侵袭
诱导上皮-间充质转化(EMT),使细胞获得迁移侵袭能力,参与伤口愈合,也促进肿瘤转移。
5. 组织修复与纤维化
损伤后促进成纤维细胞合成胶原等细胞外基质,加速修复;过度激活则导致肝、肺、肾等器官纤维化。
6. 肿瘤双向调控作用
早期抑癌:诱导细胞周期阻滞、凋亡,抑制肿瘤发生。
晚期促癌:抑制免疫监视、诱导EMT、促进血管生成,驱动肿瘤侵袭转移。
7. 炎症反应调控
兼具抗炎与促炎双重作用,依细胞微环境不同,参与急慢性炎症进程。
四、总结
TGF-β信号通路以Smad依赖为核心、非Smad通路为补充,精准调控细胞命运与组织稳态。其异常激活或抑制,是纤维化、癌症、自身免疫病的重要分子机制,也是疾病靶向治疗的关键靶点。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


