免疫检查点抑制剂的临床治疗效能,部分源于肿瘤抗原特异性T细胞的功能性参与。目前,学界研究多聚焦于CD8⁺T细胞的抗原特异性及转录调控状态,然而,肿瘤微环境(TME)中CD4⁺T细胞的表型特征、异质性分布及功能机制,仍有待进一步阐明。本研究针对黑色素瘤浸润的肿瘤抗原特异性CD4⁺T细胞亚群开展系统性解析,发现其具有CXCL13高表达的核心特征,且证实该细胞亚群与患者生存预后、肿瘤微环境中CD8⁺T细胞、巨噬细胞及B细胞的功能活性均呈显著正相关。
一、亮点聚焦
亮点1:高分辨率单细胞多组学整合:依托BD Rhapsody单细胞分析平台,整合单细胞靶向转录组测序与AbSeq单细胞膜表面蛋白组测序技术,成功解析黑色素瘤浸润CD4⁺T细胞的异质性特征。多组学联合数据可清晰区分CXCL13⁺亚群的功能分化状态,包括滤泡辅助T细胞(TFH)样亚群、细胞毒性亚群及增殖亚群等,为后续功能机制解析提供了坚实的分子基础与数据支撑。
亮点2:TCR克隆型-表型精准映射:通过单细胞TCR测序技术,精准鉴定出66个肿瘤新抗原特异性TCR克隆型,且揭示97%的肿瘤特异性CD4⁺T细胞富集于CXCL13⁺PD-1亚群。该关联性的发现,明确确立了CXCL13作为肿瘤反应性T细胞的核心标志物地位,为肿瘤特异性T细胞的精准识别提供了关键靶点。

英文标题:Neoantigen-specific CD4⁺ T cells in human melanoma have diverse differentiation states and correlate with CD8⁺ T cell, macrophage, and B cell function
中文标题:人类黑色素瘤中的新抗原特异性CD4⁺T细胞具有不同的分化状态,并与CD8⁺T细胞、巨噬细胞和B细胞功能相关
期刊:Cancer Cell
二、技术路线
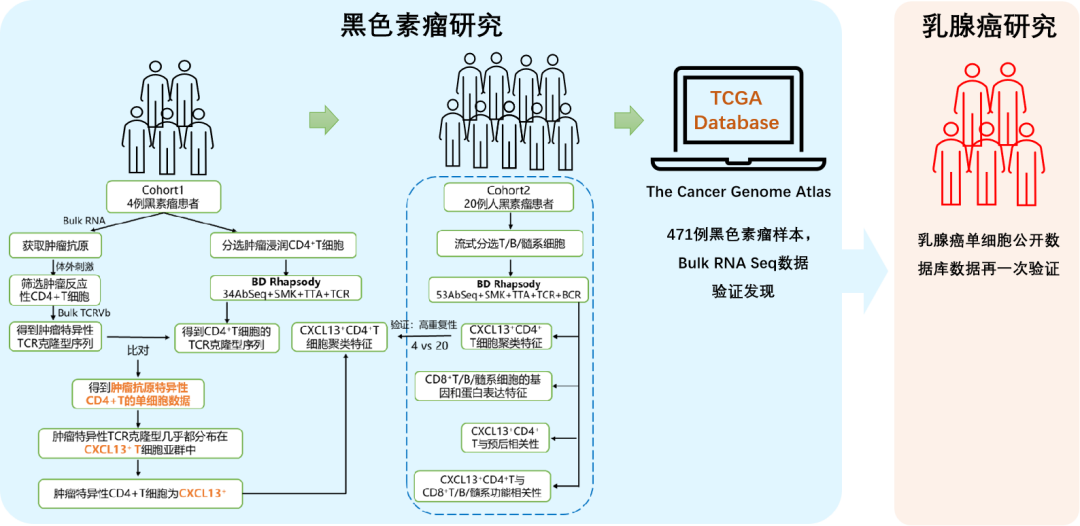
三、研究结果
01 TCRVβ测序鉴定黑色素瘤组织中肿瘤特异性CD4⁺T细胞的TCR克隆型
从4例患者样本中分离获得肿瘤抗原特异性CD4⁺T细胞,具体样本来源包括2例黑色素瘤患者(X205、X422)的肿瘤组织,以及2例接受过细胞治疗患者(X197、X198)的外周血样本。采用TCRVβ测序技术检测上述细胞的TCR克隆型(免疫特征标识),并将该核心数据与后续单细胞实验结果进行匹配验证,确保研究结果的准确性与可靠性。
02 BD单细胞多组学技术揭示黑色素瘤抗原特异性CD4⁺T细胞转录组特征
对4例黑色素瘤患者的CD4⁺T细胞进行单细胞多组学检测分析,共获得10184个细胞,聚类分析显示其可分为3个功能亚群,分别为FoxP3⁺调节性T细胞(Treg,Cluster 0)、CXCL13⁺PD-1⁺常规T细胞(Tconv,Cluster 2/3/5)及CXCL13⁻IL7R⁺常规T细胞(Tconv,Cluster 1/4)。通过匹配已知抗原特异性的40个TCR克隆型(对应259个细胞),发现97%的肿瘤特异性CD4⁺T细胞富集于CXCL13⁺PD-1⁺Tconv亚群,且该亚群呈现明显的克隆扩增特征,由此证实CXCL13⁺为黑色素瘤抗原特异性CD4⁺T细胞的核心表型。
03 BD单细胞多组学测序发现黑色素瘤抗原特异性CD4⁺T细胞存在3种不同的转录状态
对4例黑色素瘤样本的单细胞多组学数据进一步分析显示,抗原特异性CD4⁺T细胞可分为3个CXCL13⁺亚群,分别为TCF7⁺CXCR5⁺亚群(Cluster 2)、TCF7⁻Tim3⁺亚群(Cluster 3)及TCF⁻TYMS⁺亚群(Cluster 5)。为验证该结果的可靠性,将样本量扩展至20例,筛选获得26773个CD4⁺T细胞进行聚类分析,结果成功复现了上述3个具有相同特征的CXCL13⁺亚群(TCF7⁺/TCF7⁻Tim3⁺/TCF⁻TYMS⁺),进一步确认了前期研究结论的稳定性。
04 CXCL13⁺CD4⁺T细胞在肿瘤浸润CD4⁺T细胞中的占比可预测黑色素瘤患者的生存预后
将20例黑色素瘤患者样本依据CXCL13⁺CD4⁺T细胞/CD4⁺T细胞比值是否高于中位数,分为中位数以上组(above median)和中位数以下组(below median)。生存分析显示,中位数以上组患者的生存率显著高于中位数以下组(图3E)。此外,利用TCGA数据库中471例黑色素瘤的批量RNA测序(Bulk RNA-Seq)数据对上述发现进行验证,进一步证实了该结论的可靠性与普适性。
05 BD单细胞多组学鉴定肿瘤微环境CD8⁺T细胞的表型特征
以AbSeq技术检测到的CD8⁺蛋白表达为筛选标准,从肿瘤微环境中筛选获得15332个肿瘤浸润CD8⁺T细胞,聚类分析将其分为4个功能亚群。该类亚群的表型特征与CD4⁺T细胞存在一定相似性,主要高表达PD-1、CD103、CD39等分子,部分细胞可表达CXCL13⁺(分为TYMS⁺和TCF⁺两种亚型)。基因表达谱分析结果显示,CD8⁺与CD4⁺T细胞在CXCL13相关亚群间存在显著的表达相似性,提示两者可能存在协同调控机制。
06 肿瘤微环境中CXCL13⁺CD4⁺T细胞与CD8⁺T细胞的活化呈正相关
研究证实,在黑色素瘤微环境中,CXCL13⁺CD4⁺T细胞与CD8⁺T细胞活化亚群(如PD-1⁺、CD103⁺等表型细胞)呈显著正相关;同时,其特征标记基因(CXCL13、BTLA、IL21)与CD8A在471例患者的RNA测序数据中呈现显著正相关。此外,该细胞亚群还与巨噬细胞及B细胞的活化状态密切相关。上述关联性在乳腺癌免疫治疗队列中得到成功复现,提示CXCL13⁺CD4⁺T细胞与CD8⁺T细胞、髓系细胞的功能协同作用具有跨癌种特征。
四、研究总结
本研究整合流式细胞术与BD Rhapsody单细胞多组学技术,对CXCL13⁺肿瘤抗原特异性CD4⁺T细胞的生物学特性进行了系统性解析。研究结果表明,该细胞亚群不仅与黑色素瘤患者的生存预后呈显著正相关,还与肿瘤微环境中CD8⁺T细胞、巨噬细胞及B细胞的协同抗肿瘤功能密切相关。该多组学联合分析策略为肿瘤抗原特异性T细胞的研究提供了全新的方法论框架,对优化免疫治疗疗效评估体系、挖掘潜在治疗靶点具有重要的临床参考价值与学术意义。
五、免疫研究相关单细胞Abseq检测哪里有?
乐备实提供小鼠免疫研究单细胞Abseq检测服务,且Abseq数据可直接导入FlowJo分析。













 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


