一.样本&试剂寄送要求

二.贴壁细胞制备Protocol
1、在超净台内,使用75%乙醇擦拭外包装铝箔袋
2、拆开铝箔袋,取出内置器皿后,用尖镊将内置爬片取出放入所用培养板或培养皿内,
3、用胰酶消化好细胞,充分吹打,使之成单细胞悬液(注意:这一点很重要,关系到将来爬出来片子的质量)
4、种植细胞时,根据玻片的大小,先在每个孔里准备放爬片的位置滴少量培养基,目的是使玻片与培养皿靠培养基的张力粘合到一起,然后放玻片,防止加细胞悬液时玻片漂起,造成双层细胞贴片。整个过程注意无菌操作。
5、根据自己的需要选择合适的细胞密度种入培养板内即可。
6、使用细胞爬片时,(比如在6孔板钟放入爬片,6孔板的孔底面积往往比爬片面积多出一部分,加细胞悬液时,常常就是细胞铺满整个孔底,有时,细胞生长边集现象,就是靠近壁边缘细胞密度要高一些,这样处于中央细胞爬片上的细胞数量相对较少),比较好的做法是,将爬片放入孔内后,加细胞悬液时,只滴到爬片上,一直滴到液体布满整个爬片,但又不易溢出爬片边缘,放到培养箱里,等细胞贴壁后,取出,再滴加培养基布满整个孔底,继续培养,这样爬片上的细胞生长的密度就会很集中。
7、细胞放到爬片上,之后加任何试剂,都应沿培养板板壁少量一点点倒入液体,直到细胞被液体淹没,尽量不要把细胞冲到细胞爬片以外!
8、作用一定时间后取玻片。取玻片时由于玻片与培养皿底结合较紧,张力较大,一般将注射器针头针尖向背面弄个小钩,这样将爬片轻轻勾起,用小镊子取出就可以了。如果要做诸如24h,48h,72h等这样时间点的实验的话,将所需数量的爬片取出时应用酒精灯火焰烧一下针头和镊子。末取出的可接着继续培养。
9、细胞爬片,有多层包装,在超净台无菌状态下打开包装,未用完的爬片按照原先包装方式再包装起来即可。
10、爬片表面带有正电荷,请勿用手触摸,以免效果不佳!
三.悬浮细胞制备Protocol
取悬浮细胞液,1500-3000rpm离心5min,离心管底部能看到白色细胞团,弃上清;PBS清洗两遍,离心收集清洗好的细胞,弃上清;加入固定液,重悬,室温固定15-20min。
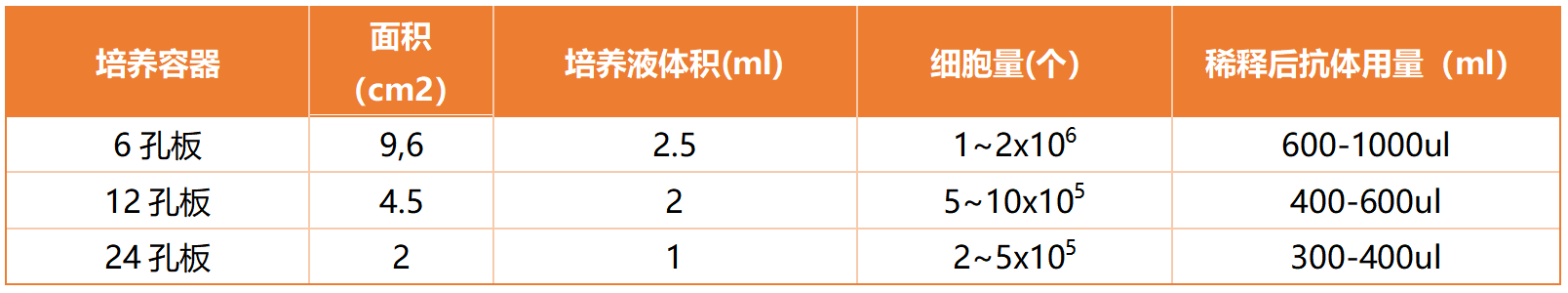
四.常见细胞容器对应细胞培养量及抗体体积
五.细胞样本关键注意事项
1、爬片消毒:必须彻底,75% 酒精消毒后需用 PBS 充分洗涤,避免酒精残留导致细胞死亡
2、固定:避免使用甲醇 - 丙酮混合液固定,适合膜蛋白但易使细胞皱缩,但会破坏脂质和膜结构。固定剂首选4%多聚甲醛,适合膜蛋白和大部分胞内蛋白,但可能掩盖磷酸化表位,固定后务必PBS洗3次(每次5分钟),彻底去除残留固定剂。
3、细胞吸附:多聚赖氨酸包被不充分或细胞静置时间不足会导致细胞脱落,若细胞吸附效果差,可延长静置时间至 45min,或提高细胞浓度。
4、细胞密度控制:不同细胞系的生长速度和贴壁能力差异较大,建议细胞在爬片上生长至 50%~70%汇合度,密度过高会导致细胞重叠,不便于清晰观察单个细胞的形态和结构影响后续染色观察;密度过低则细胞数量不足,实验结果不稳定。
5、对照设置:设置阴性对照,排除非特异性染色干扰。
6、制备细胞样本的时候建议一个组别多送几个样本,实验前都会观察选取细胞状态好的使用。
六.孔板耗材推荐(优选本公司产品,其他耗材实验端不指定品牌)
1.多聚-D-赖氨酸包被细胞培养板(细胞贴壁速度更快,贴壁更牢)

2.共聚焦爬片(防止运输过程中爬片移动)

3.腔室载玻片













 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


