一、NF-κB信号通路在疾病机制与靶向治疗中的研究进展
一项关于NF-κB信号通路的研究《 NF-κBin biology and targeted therapy: new insights and translational implications》发表于Signal Transduction and Targeted Therapy期刊。该研究系统梳理了NF-κB信号通路的组成、激活机制及调控网络,并分析了其与其他关键信号通路之间的交互作用。研究进一步阐明,NF-κB信号通路在炎症反应、免疫调节及肿瘤微环境形成中发挥重要作用,并广泛参与多种人类疾病的病理过程,包括但不限于癌症、炎症与自身免疫性疾病、心血管疾病、代谢性疾病、神经系统疾病以及新型冠状病毒感染(COVID-19)。此外,研究还讨论了靶向NF-κB信号通路的治疗策略,并对该领域的未来研究方向提出了展望,为理解NF-κB信号传导的生物学功能及其临床转化提供了重要参考。

二、典型与非典型NF-κB信号转导概述
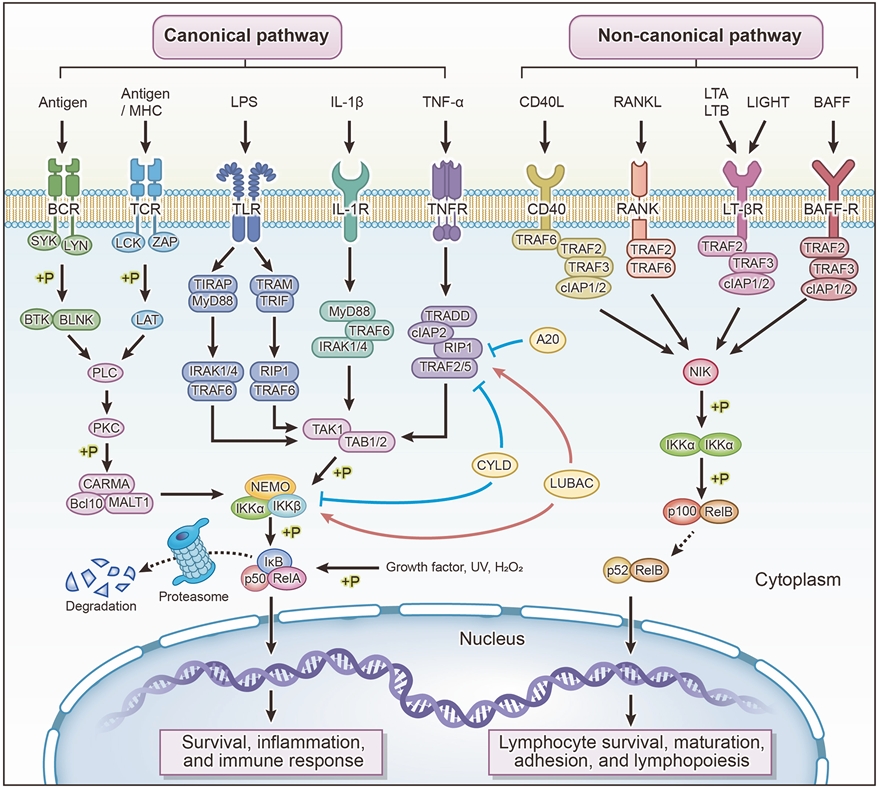
典型的NF-κB信号转导主要由BCR、TCR、TLR、IL-1R及TNFR等受体激活。其中,BCR与TCR可启动多阶段酶促反应,进而激活CARMA1/BCL-10/MALT1复合物;而TLR、IL-1R及TNFR主要促进TAK1/TAB复合物的活化。上述两种活化的复合物均可磷酸化IKKα/IKKβ/NEMO(IKKγ)复合物。随后,IKKα与IKKβ对IκBα进行磷酸化修饰,促使其发生泛素化并最终被蛋白酶体降解。这一过程导致p50/RelA转录因子的释放,后者进入细胞核并激活靶基因的转录。典型的NF-κB信号通路主要发挥促进细胞存活、介导炎症及免疫应答的生物学功能。
在非典型NF-κB信号转导中,CD40、RANK、LT-βR及BAFF-R等受体可激活NIK,进而磷酸化IKKα并促进p100向p52的降解转化。随后,p52亚基与RelB结合形成复合物,并发生核易位,从而参与调控淋巴细胞的生成、存活、成熟及粘附过程。
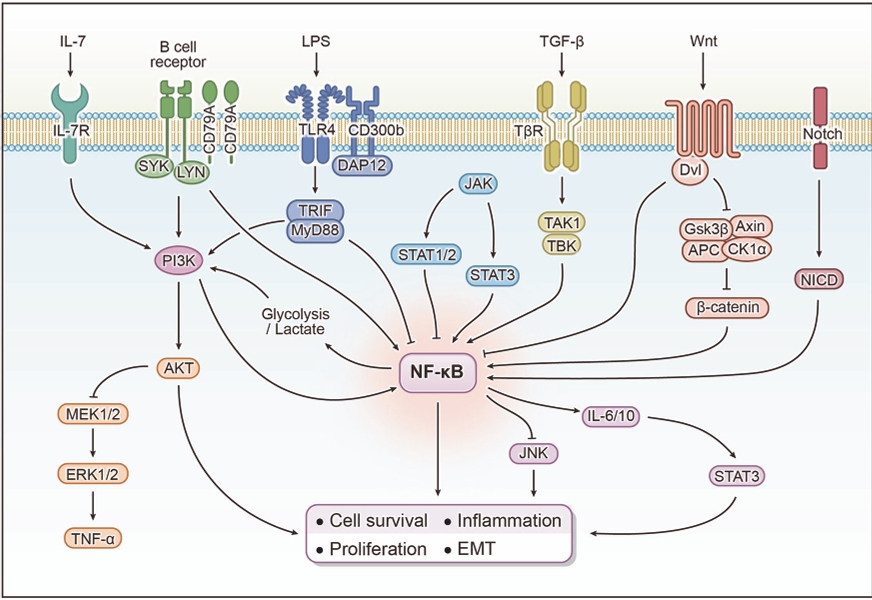
三、NF-κB信号通路与其他信号通路之间的串扰
(1)BCR与IL-7R可通过cIAP-IKK通路激活PI3K,进而刺激NF-κB信号。乙型肝炎病毒X蛋白可诱导有氧糖酵解,并通过NF-κB/己糖激酶2通路生成乳酸,进而激活PI3K/AKT信号。
(2)NF-κB能够抑制由TNF-α介导的JNK信号转导过程。
(3)NF-κB信号通路的产物IL-6可激活STAT3。其中,JAK-STAT3作为NF-κB的上游调节因子,能够促进NF-κB信号转导;而STAT1则对NF-κB介导的肿瘤细胞存活发挥抑制作用。
(4)TAK1可促进NF-κB的转录活性。
(5)Wnt/β-catenin信号通路能够激活细胞质中的NF-κB;而Dvl则在细胞核中抑制NF-κB信号传导。
(6)Notch1可与NF-κB结合,从而增强NF-κB的转录活性。
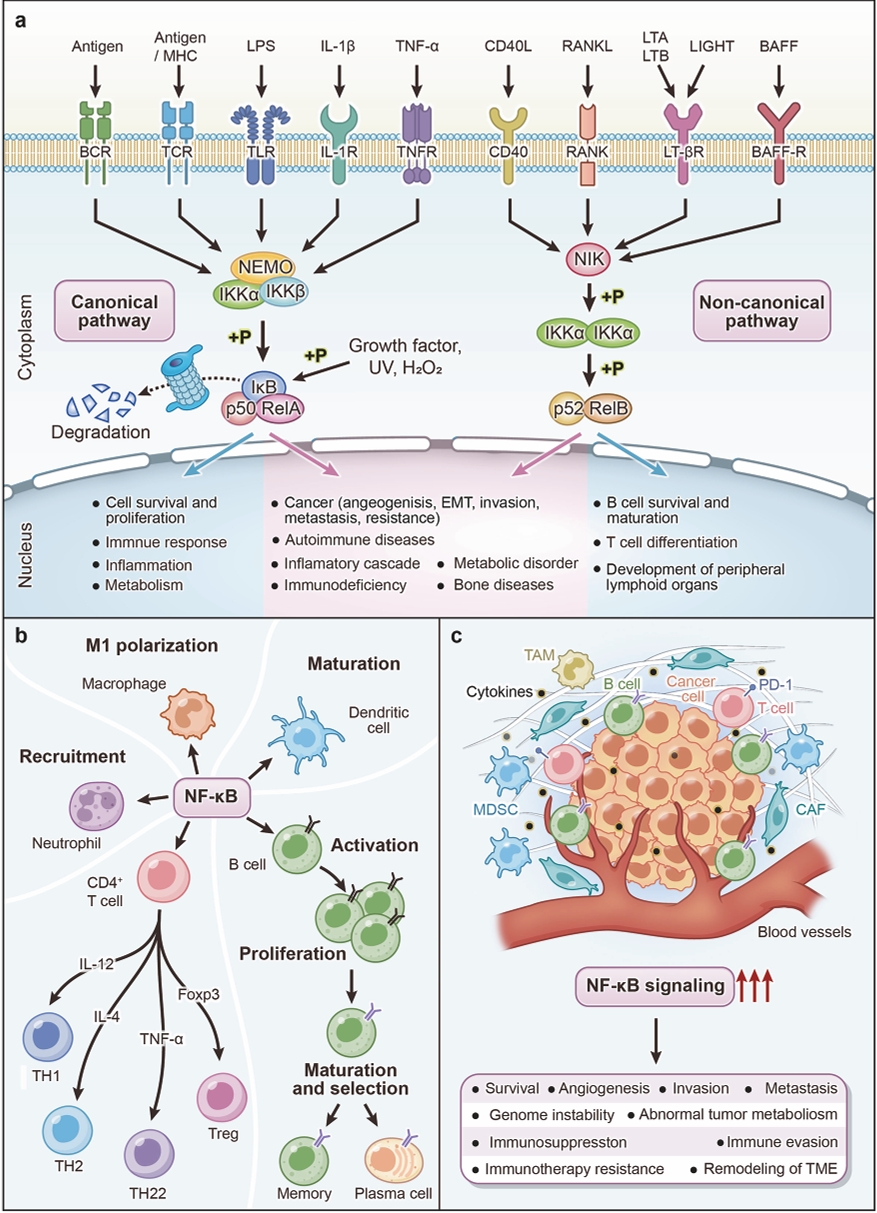
四、NF-κB信号转导的生物学功能
a 在生理环境中,NF-κB信号转导支持细胞存活,调控炎症反应及对外界刺激的免疫应答,同时参与代谢与稳态的调节。当NF-κB信号过度激活时,可在病理条件下增强肿瘤的恶性特征,包括促进血管生成、上皮-间充质转化(EMT)、侵袭、转移及治疗耐药性。此外,NF-κB信号失调还可能诱发炎症风暴及代谢紊乱。
b NF-κB在先天免疫与适应性免疫中均发挥关键作用。在先天免疫方面,NF-κB促进巨噬细胞向M1表型分化,并参与树突状细胞的成熟及中性粒细胞的募集。在适应性免疫方面,NF-κB增强B细胞的活化、增殖、成熟及选择过程。同时,在不同细胞因子的刺激下,NF-κB可驱动CD4+ T细胞向多种亚型分化。
c 肿瘤的发生与进展与肿瘤微环境(TME)密切相关。NF-κB信号的过度激活不仅促进肿瘤细胞的存活、侵袭、转移、基因组不稳定及代谢异常,还可重塑免疫抑制性微环境,从而推动免疫逃逸及对免疫治疗耐药性的产生。
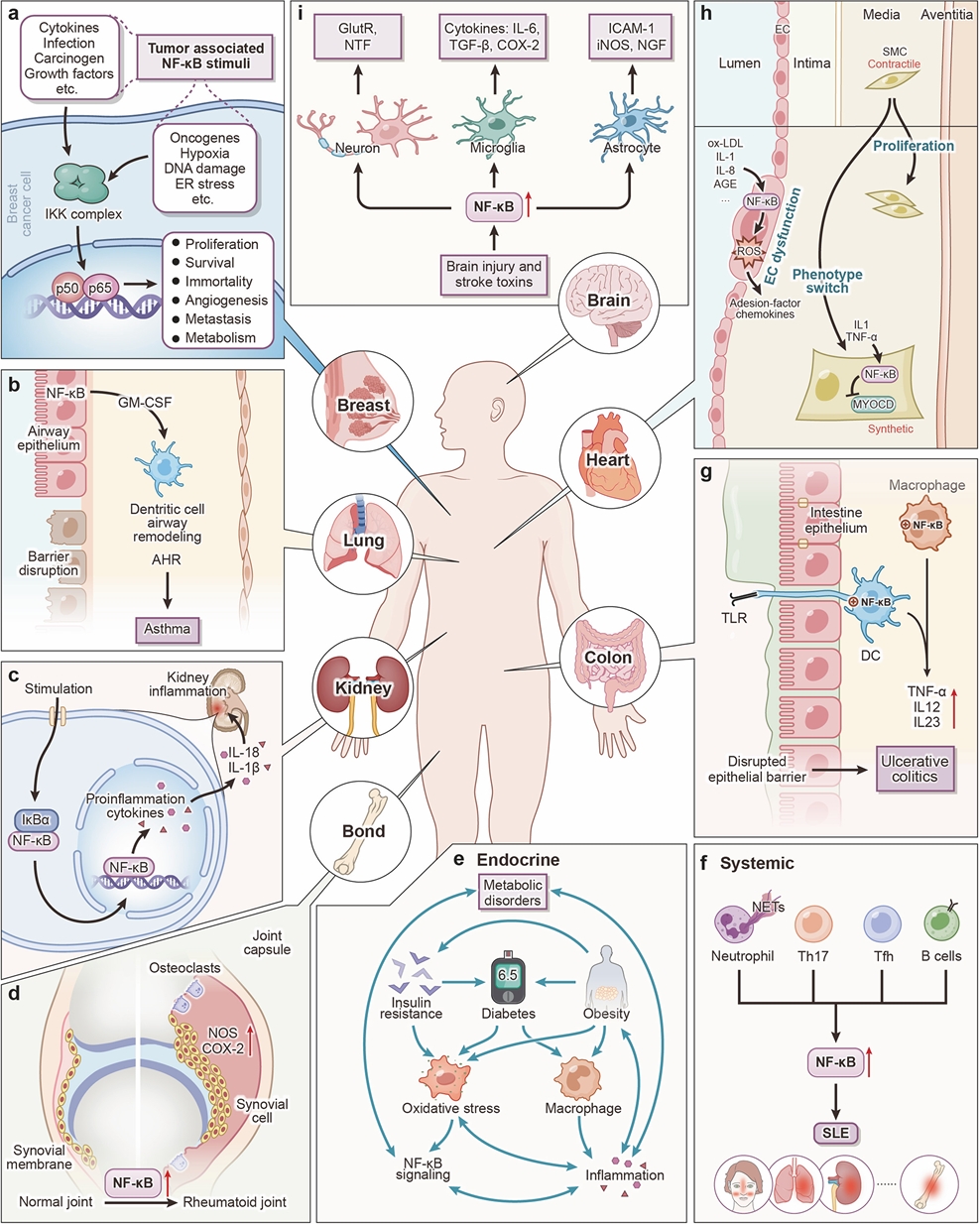
五、NF-κB在多种器官系统相关疾病中的关键作用
a 在乳腺癌细胞中,NF-κB表达上调,可促进下游基因的表达,进而推动肿瘤生长、转移及血管生成。
b 在呼吸系统中,呼吸道上皮细胞内NF-κB表达升高可加剧TH2细胞相关的炎症反应及气道高反应性,从而参与哮喘的发生发展。
c 在肾脏中,活化的NF-κB促进炎症因子IL-1β与IL-18的高表达,诱发肾脏炎症反应。
d 在关节组织中,活化的NF-κB可促进慢性炎症及成纤维样滑膜细胞的增殖,进而推动滑膜组织中类风湿关节炎(RA)的进展。
e NF-κB信号、代谢性疾病与炎症之间存在双向调控关系。胰岛素抵抗、糖尿病及肥胖等代谢疾病可通过调节氧化应激水平及巨噬细胞功能,导致NF-κB信号过度激活及炎症反应增强。
f 在系统性红斑狼疮(SLE)中,NF-κB可促进多克隆B细胞的活化及自身抗体的产生。
g 在巨噬细胞中,NF-κB激活可诱导促炎性细胞因子(如TNF-α、IL-12及IL-23)的分泌,这些因子直接或间接参与溃疡性结肠炎(UC)中常见的黏膜组织损伤。
h NF-κB通过调控一系列炎症介质的表达,参与调节动脉粥样硬化过程中不同细胞的命运。
i 在脑损伤发生后,神经元、星形胶质细胞及小胶质细胞中的NF-κB表达上调,导致IL-6及诱导型一氧化氮合酶(iNOS)等炎症因子的分泌增加,从而诱发局部脑组织炎症。TBK1作为保护性因子,可通过抑制NF-κB信号传导发挥神经保护作用。
六、靶向NF-κB信号通路的人类疾病治疗策略
针对NF-κB信号通路的抑制剂已在多种临床场景中得到应用,用于治疗肿瘤、糖尿病及其他疾病。这些药物通过不同机制实现对NF-κB通路的抑制。
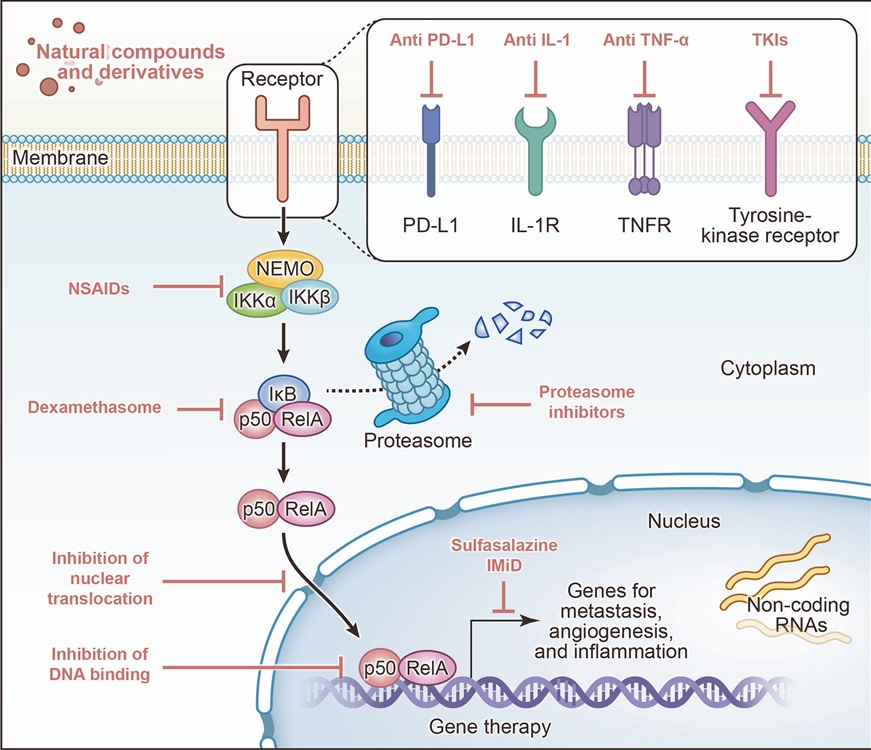
非甾体抗炎药可选择性地抑制IκB,从而阻断NF-κB的活化。地塞米松通过直接与RelA亚基结合,抑制其功能活性。免疫调节剂(IMiD),如沙利度胺,可抑制NF-κB下游的转录功能以发挥疗效。
单克隆抗体类药物,包括抗PD-L1、抗IL-1及抗TNF-α抗体,通过阻断配体与相应受体的结合,抑制其生物学效应。
蛋白酶体抑制剂(如硼替佐米、卡非佐米、伊沙佐米及乳胞素)通过阻止蛋白质降解过程发挥作用,最终诱导细胞凋亡与死亡。他克莫司可抑制钙调磷酸酶的蛋白磷酸酶活性,阻止NFAT核易位,进而抑制T细胞活化。IκBα超抑制蛋白可阻止NF-κB向细胞核的易位。
酪氨酸激酶抑制剂通过抑制酪氨酸激酶的细胞内磷酸化,从而阻断肿瘤细胞的生长。
天然化合物及其衍生物,如白藜芦醇、槲皮素及异硫氰酸酯等,通过多种机制抑制NF-κB,发挥抗肿瘤作用。
此外,靶向非编码RNA的策略也在开发中,例如抗微小RNA(抗miR)寡核苷酸,可用于抑制促进NF-κB信号通路的miRNA。基于NF-κB激活的基因表达疗法,则是一种利用癌细胞中NF-κB过度激活特征的新型癌症基因治疗策略。
七、总结与展望
本综述再次强调,NF-κB信号通路在炎症与免疫反应中发挥重要作用,尤其处于免疫治疗作为肿瘤及其他疾病治疗“变革”背景下的关键地位。事实上,NF-κB信号通路在多种被认为难以克服的疾病中已展现出初步应用潜力,其影响范围超出了本文所讨论的内容。
以艾滋病为例,CD4+ T细胞中存在的长期潜伏状态对其根治构成了重大挑战。已有研究发现,AZD5582可通过激活小鼠及猕猴模型中的非典型NF-κB信号通路,有效促进人类免疫缺陷病毒(HIV)及猴免疫缺陷病毒(SIV)的表达。这一发现为联合应用AZD5582与HIV清除药物以实现艾滋病根除提供了理论基础。
如本文所述,靶向NF-κB信号通路的治疗策略因其广泛参与多种生物学过程,将不可避免地带来副作用。因此,实现精确的药物设计、合成及递送系统势在必行,而纳米材料的应用将是推动这一进程的关键环节。
未来的研究应致力于提升靶向NF-κB信号通路治疗的有效性,同时减轻潜在不良反应,从而在免疫治疗领域取得重要突破。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


