一、引言
适应性免疫应答是机体在抗原刺激下,由T、B淋巴细胞介导的特异性、可记忆性防御反应,其中T淋巴细胞介导的细胞免疫应答主要负责清除胞内寄生菌、病毒感染细胞及恶变细胞,在宿主防御与免疫监视中占据不可替代地位。胸腺发育成熟的初始T细胞经淋巴循环定居外周免疫器官,通过T细胞受体(TCR)精准识别抗原提呈细胞(APC)表面的抗原肽 - MHC分子复合物(pMHC),在双信号与细胞因子网络调控下活化、增殖并分化为效应T细胞与记忆T细胞,完成抗原清除并维持免疫平衡。本文基于经典免疫学理论与分子机制,系统梳理T细胞介导适应性免疫应答的完整过程与调控规律,阐明其生物学意义与临床转化价值。
二、T细胞对抗原的特异性识别
(一)抗原识别的核心特征:MHC限制性
初始T细胞的TCR与APC提呈的pMHC特异性结合启动免疫应答,此过程严格遵循MHC限制性——TCR在识别抗原肽的同时,必须识别同个体APC表面的自身MHC分子,确保T细胞仅对自体细胞提呈的抗原产生应答,避免自身免疫损伤。
(二)抗原提呈途径与靶细胞特异性
- 外源性抗原(细菌、胞外蛋白等):经MHC Ⅱ类分子途径提呈,主要激活CD4⁺辅助性T细胞(Th)。
- 内源性抗原(病毒蛋白、肿瘤抗原等):经MHC Ⅰ类分子途径提呈,主要激活CD8⁺细胞毒性T细胞(CTL)。
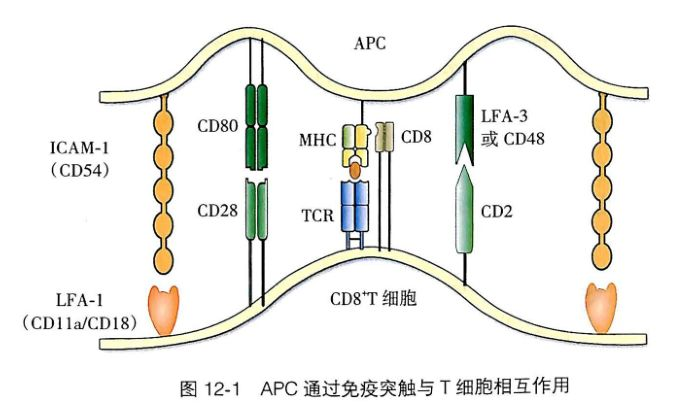
(三)APC与T细胞的相互作用及免疫突触形成
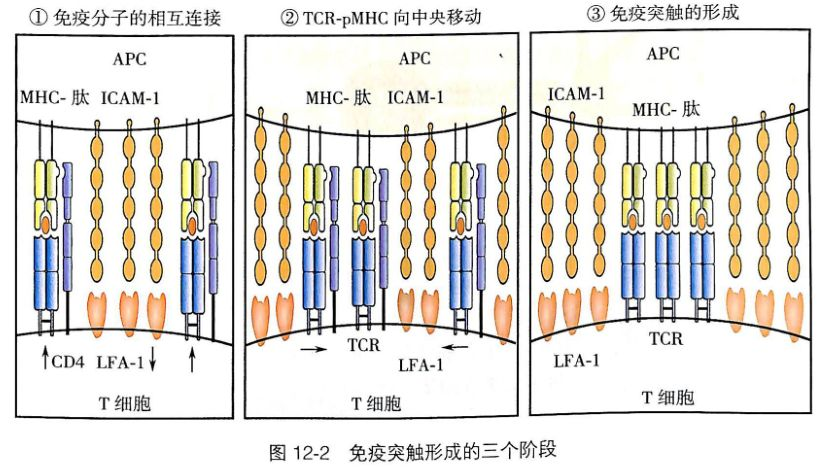
T细胞与APC先通过黏附分子发生非特异性可逆结合;若TCR特异性识别pMHC,则在细胞接触面形成免疫突触。该结构稳定细胞结合、启动跨膜信号转导,介导共刺激分子配对作用,为T细胞完全活化提供必需的第二信号,是免疫应答启动的结构基础。
图片来源 医学免疫学第六版
图片来源 医学免疫学第六版
三、 T细胞的活化、增殖与分化
(一)T细胞活化的双信号模型
1. 第一信号(抗原特异性信号)
TCR结合pMHC,经CD3及CD4/CD8共受体传导信号,激活胞质蛋白酪氨酸激酶,使CD3胞内区ITAM基序磷酸化,启动级联反应,激活NFAT、NF - κB等转录因子,驱动T细胞初步活化与IL - 2等基因转录。
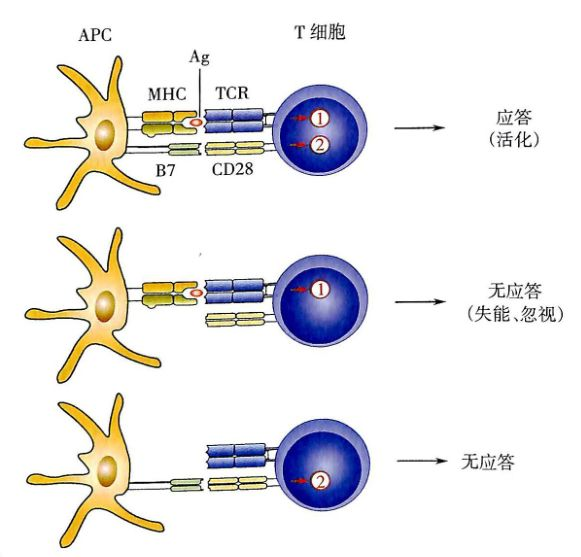
2. 第二信号(共刺激信号)
由APC与T细胞表面多对共刺激分子(如CD28/B7)相互作用提供,缺失第二信号将导致T细胞无能(anergy),是防止自身免疫的重要质控机制。
图片来源 医学免疫学第六版
(二)信号转导与关键细胞因子
TCR活化信号主要经PLC - γ途径与Ras - MAPK途径向下游传递,最终激活IL - 2基因表达。IL - 2作为T细胞自分泌生长因子,是驱动克隆增殖的核心细胞因子。
(三)CD4⁺与CD8⁺T细胞的分化
1. CD4⁺Th细胞
初始Th0细胞在局部细胞因子微环境调控下定向分化:
- Th1:介导巨噬细胞活化与迟发型超敏反应,增强细胞免疫;
- Th2:辅助B细胞产生抗体,介导体液免疫与过敏反应;
- Th17:参与固有免疫与炎症应答,与感染及自身免疫病相关;
- Tfh:定位于淋巴滤泡,调控B细胞增殖、类别转换与亲和力成熟。
2. CD8⁺CTL细胞
- Th依赖途径:靶细胞低表达共刺激分子,需APC与Th细胞提供信号及细胞因子,辅助CTL前体活化增殖;
- Th非依赖途径:高表达共刺激分子的树突状细胞(DC)可直接激活CD8⁺T细胞,诱导自身分泌IL - 2并分化为功能性CTL。
四、效应T细胞的功能与免疫应答转归
(一)辅助性T细胞的效应功能
- Th1:募集活化单核/巨噬细胞,诱导以单个核细胞浸润为主的迟发型炎症;
- Th2:辅助体液免疫,参与Ⅰ型超敏反应;
- Th17:诱导上皮与间质细胞分泌炎性因子,参与黏膜防御与炎症损伤;
- Tfh:通过IL - 21调控生发中心反应,促进高亲和力抗体产生。
(二)CTL的特异性杀伤机制
CTL高效、特异性杀伤靶细胞而不损伤正常组织,主要通过两条途径:
1. 穿孔素 - 颗粒酶途径:穿孔素在靶细胞膜形成孔道,颗粒酶进入胞内启动凋亡;
2. 死亡受体途径:CTL表面FasL与靶细胞Fas结合,激活胱天蛋白酶级联反应诱导凋亡。
(三)免疫应答的终止与记忆T细胞形成
抗原清除后,活化T细胞通过活化诱导的细胞死亡(AICD)凋亡清除,表达Fas/FasL介导自身凋亡,恢复免疫稳态。少量抗原特异性T细胞分化为记忆T细胞,介导快速、强效的再次应答,其中CD8⁺记忆T细胞的维持依赖MHC Ⅰ类分子与IL - 15、IFN - α等细胞因子,不依赖持续抗原刺激。
五、总结
T细胞介导的适应性免疫应答以特异性识别、双信号调控、克隆扩增、效应分化、免疫记忆为核心特征,构成机体抵御胞内病原体与肿瘤的关键防线。MHC限制性与免疫突触保证识别精准性,双信号模型防止异常活化,效应亚群分工实现抗感染、抗炎与免疫调节协同作用,记忆T细胞则提供持久保护。该网络失衡与感染迁延、肿瘤逃逸、自身免疫病密切相关。深入解析T细胞应答的分子机制,可为疫苗研发、CAR - T细胞治疗、免疫检查点抑制剂及自身免疫病干预提供关键靶点与策略。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


