Prostate cancer cell-derived exosomal IL-8 fosters immune evasion by disturbing glucolipid metabolism of CD8+ T cell
CD8(+) T cell, CP: Cancer, CP: Immunology, PPARα, exosome, glucolipid metabolism, interleukin-8, prostate cancer, CD8(+) T细胞, 癌症, 免疫学, PPARα, 外泌体, 糖脂代谢, 白介素-8, 前列腺癌 LabEX支持文献- Cell Reports
- 生物学1区
- 2023
- 6.9
- 42(11):113424
- Human
- Luminex
- 生殖系统
- 外泌体
- 生殖系统
- 前列腺癌
- GM-CSF,IFN gamma,IL-1 beta,IL-2,IL-4,IL-5,IL-6,IL-8,IL-12p70,IL-13,IL-18,TNF alpha,IL-9,IL-10,IL-17A (CTLA-8),IL-21,IL-22,IL-23,IL-27,IFN alpha,IL-1 alpha,IL-1RA,IL-7,IL-15,IL-31,TNF beta,Eotaxin (CCL11),GRO alpha (CXCL1),IP-10 (CXCL10),MCP-1 (CCL2),MIP-1 alpha (CCL3),MIP-1 beta (CCL4),RANTES (CCL5),SDF-1 alpha,BDNF,EGF,FGF-2,HGF,NGF beta,PDGF-BB,PlGF-1,SCF,VEGF-A,VEGF-D
- 10.1016/j.celrep.2023.113424.
相关货号
Abstract
CD8+T细胞的耗竭是免疫治疗中的一大障碍;然而,相关机制在很大程度上仍属未知。在此研究中,我们发现前列腺癌细胞源性的外泌体能够通过转运白介素-8(IL-8)来抑制 CD8+T细胞的功能。与免疫细胞中检测到的低IL-8水平相比,前列腺癌细胞分泌了大量的IL-8,且进一步富集于外泌体中。前列腺癌细胞源性的外泌体进入 CD8+T细胞后,通过加剧细胞饥饿状态而耗竭了这些细胞。从机制上讲,外泌体中的IL-8会过度激活受体细胞中的 PPARa,从而通过下调 GLUT1和HK2 降低葡萄糖利用率,同时通过上调 CPT1A 和 ACOX1 促进脂肪酸代谢。PPARa 进一步激活解偶联蛋白1(UCP1),从而促进脂肪酸的代谢以产生热量而非合成 ATP。因此,抑制 PPAR和 UCP1 可通过抵消外泌体 IL-8的作用来恢复CD8+T细胞的增殖。本研究揭示出,肿瘤外泌体激活IL-8-PPARa-UCP1轴通过干扰能量代谢过程,对肿瘤浸润的 CD8+T细胞造成损害。
关键词:CD8+T细胞;CP:癌症;CP:免疫学;PPARa;外泌体;糖脂代谢;白细胞介素-8;前列腺癌。
LabEx提供的Luminex检测服务
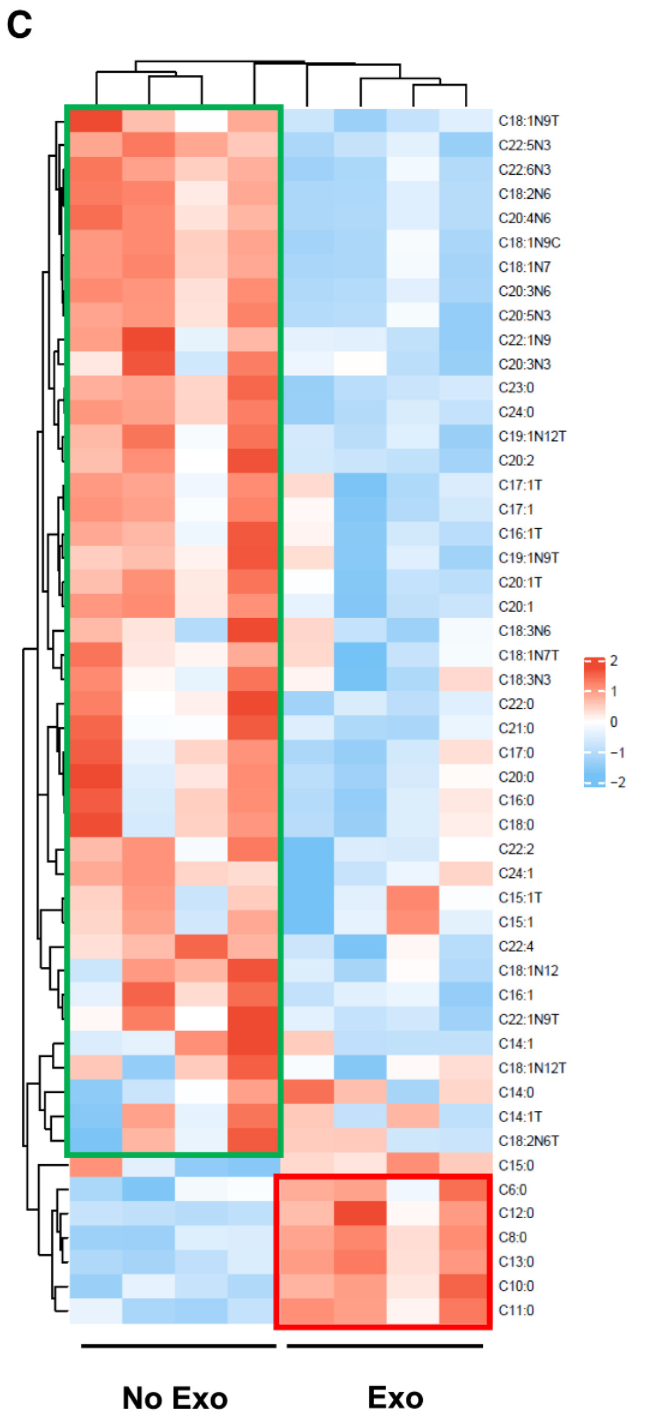
研究者使用人类细胞因子抗体阵列分析了肿瘤外泌体和CD8+ T细胞外泌体中的细胞因子谱。结果表明,炎症相关的细胞因子在肿瘤外泌体中富集,而免疫相关的细胞因子在CD8+ T细胞的外泌体中增加。值得注意的是,癌细胞分泌了大量的肿瘤细胞因子并在外泌体中积累,包括IL-1β、IL-6、IL-8和IL-10。相比之下,这些细胞因子的水平在CD8+ T细胞的外泌体中较低。
分组:有无肿瘤外泌体。
重要发现
在本研究中,研究者发现前列腺癌(PCa)细胞来源的外泌体通过运输白介素-8(IL-8)来阻碍CD8+ T细胞的功能。与免疫细胞中检测到的低IL-8水平相比,PCa细胞分泌大量IL-8,并进一步在外泌体中积累。将PCa细胞来源的外泌体传递给CD8+ T细胞后,通过增强饥饿状态使这些细胞耗竭。机制上,外泌体中的IL-8在受体细胞中过度激活PPARα,从而通过下调GLUT1和HK2来减少葡萄糖利用,但通过上调CPT1A和ACOX1来增加脂肪酸代谢。PPARα进一步激活解偶联蛋白1(UCP1),导致脂肪酸代谢用于产热而非ATP合成。结果,抑制PPARα和UCP1通过抵消外泌体IL-8的作用来恢复CD8+ T细胞的增殖。研究者揭示了肿瘤外泌体激活的IL-8-PPARα-UCP1轴通过干扰能量代谢来损害肿瘤浸润的CD8+ T细胞。
LabEx Luminex平台助力CD8+ T细胞的耗竭相关研究
本周为大家带来的文献为发表Cell Rep. (IF: 7.5)的” Prostate cancer cell-derived exosomal IL-8 fosters immune evasion by disturbing glucolipid metabolism of CD8+ T cell”。本文使用了LabEx提供的Luminex检测服务。
由于传统的放疗和化疗往往难以治疗恶性肿瘤,激发患者免疫系统对抗癌症的免疫治疗极大地改善了癌症治疗。然而,免疫抑制是宿主免疫监视中的一个主要问题,特别是肿瘤微环境(TME)主要通过耗竭免疫系统来维持免疫治疗抵抗力。作为免疫的主要力量,CD8+ T细胞对于维持抗肿瘤效能至关重要。然而,肿瘤浸润的CD8+ T细胞具有较低的杀伤功能。除了免疫检查点介导的免疫受损,越来越多的证据表明,代谢紊乱是TME中CD8+ T细胞功能障碍的一个关键因素。
CD8+ T细胞的耗竭是免疫治疗中的一个主要障碍,然而其相关机制尚不完全清楚。
LabEx提供的Luminex检测服务
研究者使用人类细胞因子抗体阵列分析了肿瘤外泌体和CD8+ T细胞外泌体中的细胞因子谱。结果表明,炎症相关的细胞因子在肿瘤外泌体中富集,而免疫相关的细胞因子在CD8+ T细胞的外泌体中增加。值得注意的是,癌细胞分泌了大量的肿瘤细胞因子并在外泌体中积累,包括IL-1β、IL-6、IL-8和IL-10。相比之下,这些细胞因子的水平在CD8+ T细胞的外泌体中较低。

重要发现
在本研究中,研究者发现前列腺癌(PCa)细胞来源的外泌体通过运输白介素-8(IL-8)来阻碍CD8+ T细胞的功能。与免疫细胞中检测到的低IL-8水平相比,PCa细胞分泌大量IL-8,并进一步在外泌体中积累。将PCa细胞来源的外泌体传递给CD8+ T细胞后,通过增强饥饿状态使这些细胞耗竭。机制上,外泌体中的IL-8在受体细胞中过度激活PPARα,从而通过下调GLUT1和HK2来减少葡萄糖利用,但通过上调CPT1A和ACOX1来增加脂肪酸代谢。PPARα进一步激活解偶联蛋白1(UCP1),导致脂肪酸代谢用于产热而非ATP合成。结果,抑制PPARα和UCP1通过抵消外泌体IL-8的作用来恢复CD8+ T细胞的增殖。研究者揭示了肿瘤外泌体激活的IL-8-PPARα-UCP1轴通过干扰能量代谢来损害肿瘤浸润的CD8+ T细胞。
本网站销售的所有产品及服务均不得用于人类或动物之临床诊断或治疗,仅可用于工业或者科研等非医疗目的。











 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


