RNA 干扰(RNA Interference, RNAi)作为真核生物中高度保守的基因表达调控机制,通过双链 RNA 分子特异性介导目标基因的转录后沉默,成为生命科学领域研究基因功能的核心工具。这一机制不仅是生物体抵御病毒入侵和维持基因组稳定的天然防御系统,更为人工调控基因表达提供了精准高效的技术路径。本文从分子层面系统剖析 RNA 干扰介导基因沉默的完整机制,包括核心作用阶段、关键分子参与及调控特征,阐释这一生物学过程的精密调控网络。
一、RNA 干扰基因沉默的核心阶段
RNA 干扰介导的基因沉默是多步骤协同的分子过程,从双链 RNA 识别到目标 mRNA 功能抑制,可划分为三个紧密衔接的核心阶段。
(一)启动阶段:dsRNA 的加工与 siRNA 生成
基因沉默启动始于双链 RNA(dsRNA)的识别与加工。外源性 dsRNA(如病毒基因组 RNA)或内源性 dsRNA(如重复序列转录产物)产生时,III 型核糖核酸酶 Dicer 特异性识别长链 dsRNA。Dicer 通过 N 端 RNA 解旋酶结构域结合并解开部分双链,C 端两个 RNase III 结构域形成二聚体,将 dsRNA 切割为 21-23 核苷酸的小干扰 RNA(siRNA),这一过程正是Dicer 酶介导 dsRNA 加工生成 siRNA 机制的核心环节。siRNA 每条链 3' 端带 2 个突出核苷酸,5' 端有磷酸基团,这一特征性结构是后续复合体组装的关键信号。Dicer 倾向于在 dsRNA 热力学不稳定区域及富含尿嘧啶序列处切割,确保生成的 siRNA 具有高效靶向沉默能力。
(二)效应阶段:RISC 复合体的组装与活化
siRNA 生成后进入 RNA 诱导沉默复合体(RISC)的组装与活化阶段,这是特异性基因沉默的核心步骤。siRNA 与 Argonaute(Ago)蛋白家族成员(哺乳动物中主要是 Ago2)结合,同时招募 Dicer 和 TRBP 等辅助蛋白形成前 RISC 复合体。复合体内部 siRNA 双链构象变化,5' 端热力学稳定性低的向导链被保留,过客链通过 Ago2 内切酶活性降解,最终形成成熟 RISC 复合体(siRISC)。Ago2 通过 PAZ 结构域结合 siRNA 3' 突出端,MID 结构域结合 5' 端磷酸基团,确保向导链正确定位与稳定结合,为靶向识别 mRNA 奠定基础。
(三)执行阶段:mRNA 的靶向识别与功能抑制
成熟 siRISC 复合体通过向导链序列互补配对,特异性识别细胞质中目标 mRNA。向导链与 mRNA 的互补配对具有高度特异性,尤其是 5' 端第 2-8 位的 “种子区域”,单个核苷酸错配即可显著降低沉默效果。序列完全互补时,Ago2 的 PIWI 结构域发挥核酸内切酶活性,在 mRNA 互补区域中间位置切割磷酸二酯键,导致 mRNA 断裂。断裂后的 mRNA 被 XRN1 等 5'→3' 核酸外切酶降解,丧失翻译能力。互补序列存在差异时,复合体通过抑制核糖体结合或加速 mRNA 脱腺苷酸化实现翻译抑制,两种机制共同确保基因表达高效沉默。
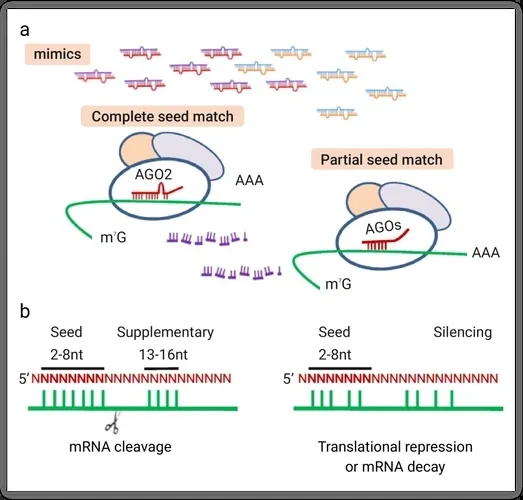
二、关键分子在沉默机制中的作用
RNA 干扰基因沉默机制的高效运行依赖多种关键分子的协同作用,它们通过精确的结构域识别和功能配合构建严密调控网络。
(一)Dicer 酶的核心功能
Dicer 作为 RNA 干扰起始分子,在 dsRNA 加工中不可替代。其结构包含多个功能域:DEXD/H 解旋酶结构域解开 dsRNA 双链;PAZ 结构域识别末端结构确保底物特异性;两个 RNase III 结构域形成催化中心切割 dsRNA 骨架;C 端 dsRNA 结合结构域增强底物亲和力。Dicer 的表达水平和活性受严格调控,在不同细胞类型和发育阶段存在差异,直接影响 RNA 干扰效率,这与细胞抗病毒状态和基因表达模式密切相关。
(二)Argonaute 蛋白的多重作用
Argonaute 蛋白家族是 RISC 复合体核心组分,Ago2 在哺乳动物 RNA 干扰中起关键作用。Ago2 的 PAZ 结构域识别 siRNA 3' 端突出结构;MID 结构域结合 5' 端磷酸基团确保向导链定位;PIWI 结构域赋予核酸内切酶活性,负责切割目标 mRNA 和去除过客链。RISC 复合体活化过程中,Ago2 通过构象变化实现向导链选择与过客链降解,这对沉默特异性至关重要。此外,Ago2 与多种辅助蛋白相互作用,参与 siRISC 复合体核质运输和 mRNA 降解后复合体回收利用。
(三)siRNA 的结构特征与功能
siRNA 结构特征直接决定沉默效率和特异性。理想 siRNA 为 21-23 核苷酸双链 RNA,3' 端突出核苷酸被 Ago2 的 PAZ 结构域识别,5' 端磷酸基团增强与 MID 结构域结合稳定性。序列组成上,GC 含量需控制在 30%-50%,避免连续相同核苷酸和内部二级结构,确保与目标 mRNA 有效配对。向导链选择由双链两端热力学稳定性决定,5' 端稳定性低的链更易成为向导链,确保 RISC 复合体正确活化。
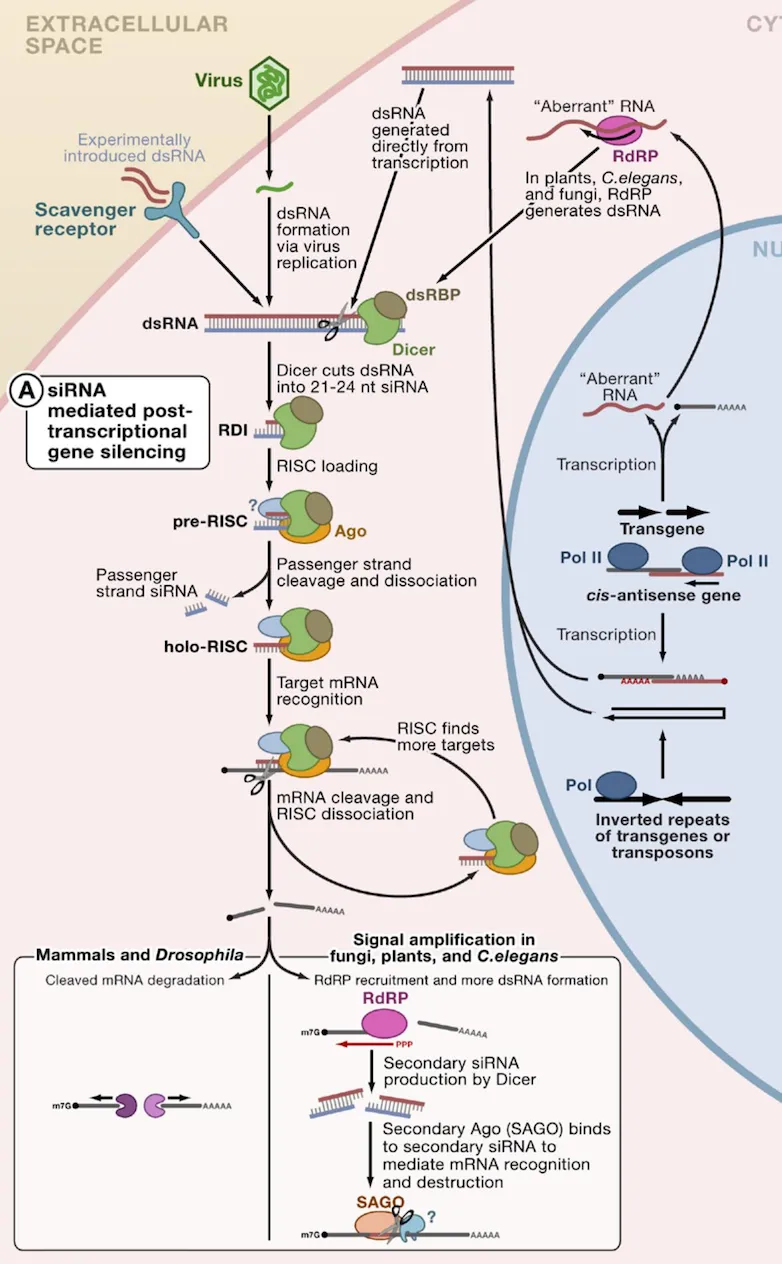
三、RNA 干扰基因沉默的调控特征
RNA 干扰介导的基因沉默机制具有高度调控特征,确保基因表达抑制的特异性、高效性和可控性。
(一)序列特异性调控
序列特异性由 siRNA 向导链与目标 mRNA 互补配对严格控制,依赖两个层面:一是种子区域(2-8 位核苷酸)与 mRNA 的精确互补,决定初始识别效率,RNAi 基因沉默中 siRNA 种子区域(2-8 位核苷酸)序列特异性调控是实现精准靶向的核心分子基础;二是其余区域互补程度影响沉默效率和持续时间。种子区域单个核苷酸错配可使沉默效率降低 50% 以上,多个错配可能完全丧失靶向能力。这种高度特异性使 RNA 干扰能区分同源性 95% 的不同基因,为精准沉默提供分子基础。
(二)效率调控机制
RNA 干扰具有高效放大效应,少量 dsRNA 即可引发大量 mRNA 降解。高效性源于:一是 siRNA 可反复使用,一个 RISC 复合体介导多个 mRNA 切割;二是植物和线虫中,siRNA 通过 RNA 依赖的 RNA 聚合酶(RdRP)扩增,形成沉默信号级联放大。此外,TRBP、PACT 等辅助蛋白与 Dicer 和 Ago2 相互作用,增强 RISC 复合体组装效率和活性,确保低浓度 dsRNA 下也能有效抑制基因表达。
(三)时空特异性调控
时空特异性调控确保基因表达抑制在正确时间和细胞类型中发生。自然状态下,内源性 RNA 干扰的时空特异性通过 Dicer 和 Ago 蛋白组织特异性表达及 dsRNA 产生时空调控实现。人工应用中,可通过诱导型表达系统控制沉默时空,如用组织特异性启动子驱动 siRNA 表达,或通过小分子诱导剂调控 dsRNA 生成,这使研究人员能精确研究基因在特定发育阶段或生理过程中的功能。
四、RNA 干扰基因沉默的生物学意义
RNA 干扰介导的基因沉默机制是高效的基因表达调控方式,在生物体生理活动中具有重要意义,是维持基因组稳定和适应环境变化的关键机制。抗病毒防御中,病毒入侵时其基因组 RNA 或复制中间体形成的 dsRNA 被 Dicer 切割为 siRNA,通过 RNA 干扰降解病毒 mRNA,抑制病毒复制,这在植物、昆虫和低等脊椎动物中是天然免疫的重要组成部分。基因组稳定性维持方面,RNA 干扰沉默转座子和重复序列表达,防止其插入基因组导致突变,RNA 干扰缺陷细胞系中转座子活性显著升高,基因组不稳定性增加。
发育调控中,RNA 干扰(尤其是 miRNA 介导的沉默)通过时空特异性沉默目标基因,参与细胞分化、器官形成等过程。特定 miRNA 表达变化可调控干细胞分化方向,机制异常可能导致发育畸形。此外,RNA 干扰参与应激反应调控,细胞面临环境压力时,通过改变内源性 siRNA 产生模式,沉默非必需基因,优先保障生存必需基因表达,帮助细胞适应环境变化。
RNA 干扰机制的发现揭示了基因表达调控新方式,为生命科学研究提供革命性工具。通过人工设计 siRNA 精准沉默目标基因,已成为解析基因功能、研究疾病机制的核心手段,也为开发基因治疗策略提供重要理论基础,推动基础研究向临床应用转化。
乐备实是国内专注于提供高质量蛋白检测以及组学分析服务的实验服务专家,自2018年成立以来,乐备实不断寻求突破,公司的服务技术平台已扩展到单细胞测序、空间多组学、流式检测、超敏电化学发光、Luminex多因子检测、抗体芯片、PCR Array、ELISA、Elispot、多色免疫组化等30多个,建立起了一套涵盖基因、蛋白、细胞以及组织水平实验的完整检测体系。
我们可提供从样本运输、储存管理、样本制备、样本检测到检测数据分析的全流程服务。凭借严格的实验室管理流程、标准化实验室操作、原始数据储存体系以及实验项目管理系统,已经为超过3000家客户单位提供服务,年检测样本超过100万,受到了广大客户的信任与支持。











 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


