摘要
胞外囊泡(Extracellular Vesicles, EVs)是由细胞主动释放的具有膜结构的异质性囊泡群体,直径范围涵盖 30-40nm 至 8-9μm,广泛存在于各类体液中。胞外囊泡分离纯化方法指通过超速离心、尺寸排阻等技术从样本中提取高纯度囊泡。其中,直径小于 200nm 的小型胞外囊泡(small Extracellular Vesicles, sEVs)因在细胞间通讯中扮演关键角色,成为癌症研究领域的热点。本文系统阐述癌症及肿瘤微环境(Tumor Microenvironment, TME)来源 sEVs 的生物学特征、其在肿瘤进展中的调控机制,以及在癌症诊断生物标志物和治疗策略开发中的应用前景,为癌症精准诊疗研究提供参考。
一、癌症对 sEVs 形成及内容物的调控机制
肿瘤细胞的恶性转化会显著重塑 sEVs 的生物合成途径及 cargo 分选过程。研究表明,多种致癌基因的异常激活是驱动这一变化的核心机制。例如,结肠癌和胶质母细胞瘤中突变型 KRAS 与 EGFR 变体 III 的过表达,可通过调控胞内信号通路,改变 sEVs 中蛋白质组和核酸的整体组成。国家癌症研究所(NCI-60)的 60 种癌症细胞系蛋白质组学分析显示,尽管不同癌症类型的 sEVs 共有的蛋白仅占少数,但每种癌症来源的 sEVs 均携带独特的蛋白质谱,这为通过 sEVs 追溯肿瘤起源组织提供了理论依据。
在核酸层面,癌细胞分泌的 sEVs 常富集特定 microRNAs(miRNAs),这些 miRNAs 可通过调节原发灶微环境或远端转移前龛的细胞功能,促进肿瘤侵袭转移及耐药性形成。其分子机制已得到部分阐明:p53 突变体可通过增强 Rab 偶联蛋白(RCP)依赖的整合素循环,调控蛋白质进入 sEVs 的分选过程,并改变受体基质细胞的表型;而致癌 KRAS 介导的 MEK-ERK 信号通路激活,则会抑制 AGO2 依赖的 miRNAs 向 sEVs 中的装载。深入解析致癌信号对 sEVs 生物学特性的调控,有望发现肿瘤特异性的治疗靶点及通路。
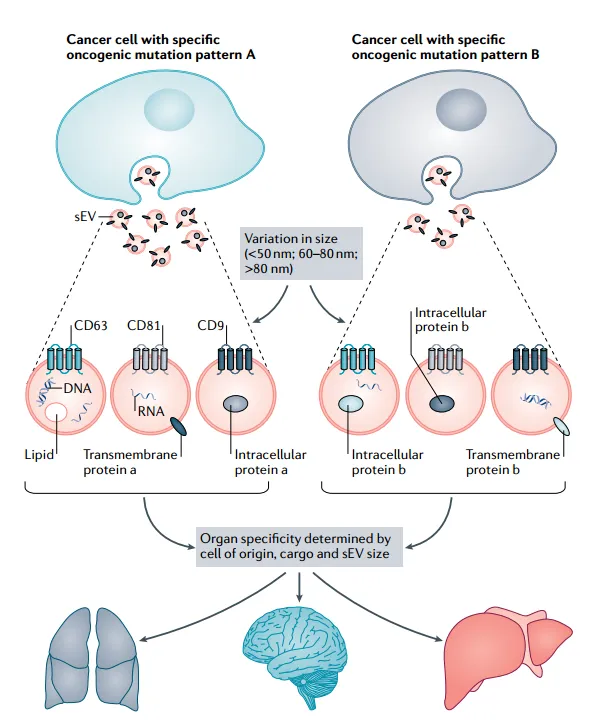
二、sEVs 作为癌症生物标志物的研究现状
sEVs 携带的肿瘤特异性分子为癌症早期诊断、预后评估及疗效监测提供了新型生物标志物来源,其优势在于可从血液、尿液、黏液等体液中无创获取,便于动态监测。
(一)蛋白质类生物标志物
致癌信号驱动的特异性蛋白在 sEVs 表面或腔内的富集,是临床检测的重要靶点。例如,黑色素瘤患者循环 sEVs 中高表达酪氨酸酶相关蛋白 2(TYRP2)、晚期抗原 4(VLA4)、热休克蛋白 70(HSP70)及 MET 癌蛋白,其中 TYRP2 高表达的 sEVs 可促进骨髓祖细胞向转移前微环境迁移,与肿瘤远处转移密切相关。然而,单一蛋白标志物难以满足临床对检测特异性和灵敏度的需求,这主要源于肿瘤的高度异质性,因此多蛋白联合检测成为提升诊断效能的重要方向。
(二)核酸类生物标志物
sEVs 内封装的 RNA 和 DNA 同样具有重要诊断价值。逆转录 - 定量 PCR 技术检测尿液 sEVs 中特定 mRNA 的表达水平,可有效识别高级别前列腺癌;乳腺癌患者血浆 sEVs 中 miR-21 和 miR-1246 的富集程度,可用于疾病诊断及治疗响应监测;多发性骨髓瘤患者 sEVs 的 miRNA 谱则能对肿瘤进展阶段及患者总体生存期进行分层。此外,sEVs 中的双链 DNA(dsDNA)可反映细胞来源的致癌突变谱,为明确肿瘤驱动突变提供关键信息,进一步拓展了其在精准诊断中的应用场景。
三、sEVs 在癌症治疗中的应用潜力
基于 sEVs 在肿瘤进展中的双重作用,其在癌症治疗领域的应用主要围绕 “抑制促瘤功能” 和 “利用载体特性” 两大方向展开。
(一)清除循环肿瘤来源 sEVs
鉴于肿瘤来源 sEVs 对转移的促进作用,清除循环中的此类 sEVs 成为潜在治疗策略。研究显示,功能化介孔二氧化硅纳米颗粒可特异性结合非小细胞肺癌(NSCLC)来源的 sEVs,显著降低荷瘤小鼠循环中肿瘤 sEVs 水平,进而抑制体内转移灶形成。这一方法为阻断肿瘤细胞间通讯、抑制转移提供了新思路。胞外囊泡液体活检标志物,作为疾病诊断的新型无创生物标志物来源。
(二)sEVs 作为免疫治疗调节剂
肿瘤来源 sEVs 因携带新抗原、肿瘤相关抗原及 MHC I 类分子,可通过激活抗肿瘤免疫反应发挥治疗作用。例如,从黑色素瘤患者腹水中分离的 sEVs 表达黑素瘤抗原 MART1,能将抗原递送至自体树突状细胞(DCs),进而交叉激活细胞毒 T 细胞,实现抗原特异性免疫应答的扩增。此外,免疫细胞来源的 sEVs 同样展现出免疫调节潜力:成熟 DCs 来源的 sEVs 诱导抗原特异性 T 细胞激活的效率是未成熟 DCs 的 100 倍;M1 型巨噬细胞来源的 sEVs 可通过促进促炎细胞因子分泌抑制黑色素瘤生长;NK 细胞来源的 sEVs 则能直接诱导肿瘤细胞凋亡。

(三)工程化 sEVs 的靶向治疗应用
通过技术手段对 sEVs 进行工程化改造,可提升其靶向性和治疗效能。电穿孔是目前最常用的 cargo 装载方法,可将细胞毒性药物、小干扰 RNA(siRNA)等载入 sEVs。例如,间充质基质细胞来源的 sEVs 经电穿孔加载 KrasG12D 短发夹 RNA 后,可有效降低胰腺癌细胞中突变 Kras 的表达,抑制原位肿瘤生长。为实现靶向递送,研究者通过将靶向载体(如抗 HER2 亲和体、sigma 受体配体)与 sEVs 表面蛋白融合,或利用光遗传学工具调控 sEVs 的生物分布,显著提升了其在肿瘤部位的富集效率,为精准治疗奠定基础。

四、总结与展望
sEVs 作为细胞间通讯的关键媒介,在癌症的发生发展中发挥着多重调控作用。其携带的特异性分子为癌症无创诊断提供了新型生物标志物,而其天然的生物相容性和靶向递送能力则使其成为理想的治疗载体。未来,随着合成生物学技术的发展及对 sEVs 分选机制的深入理解,有望实现 sEVs 的精准工程化改造,推动其在癌症诊断与治疗领域的临床转化,为癌症患者带来新的治疗机遇。
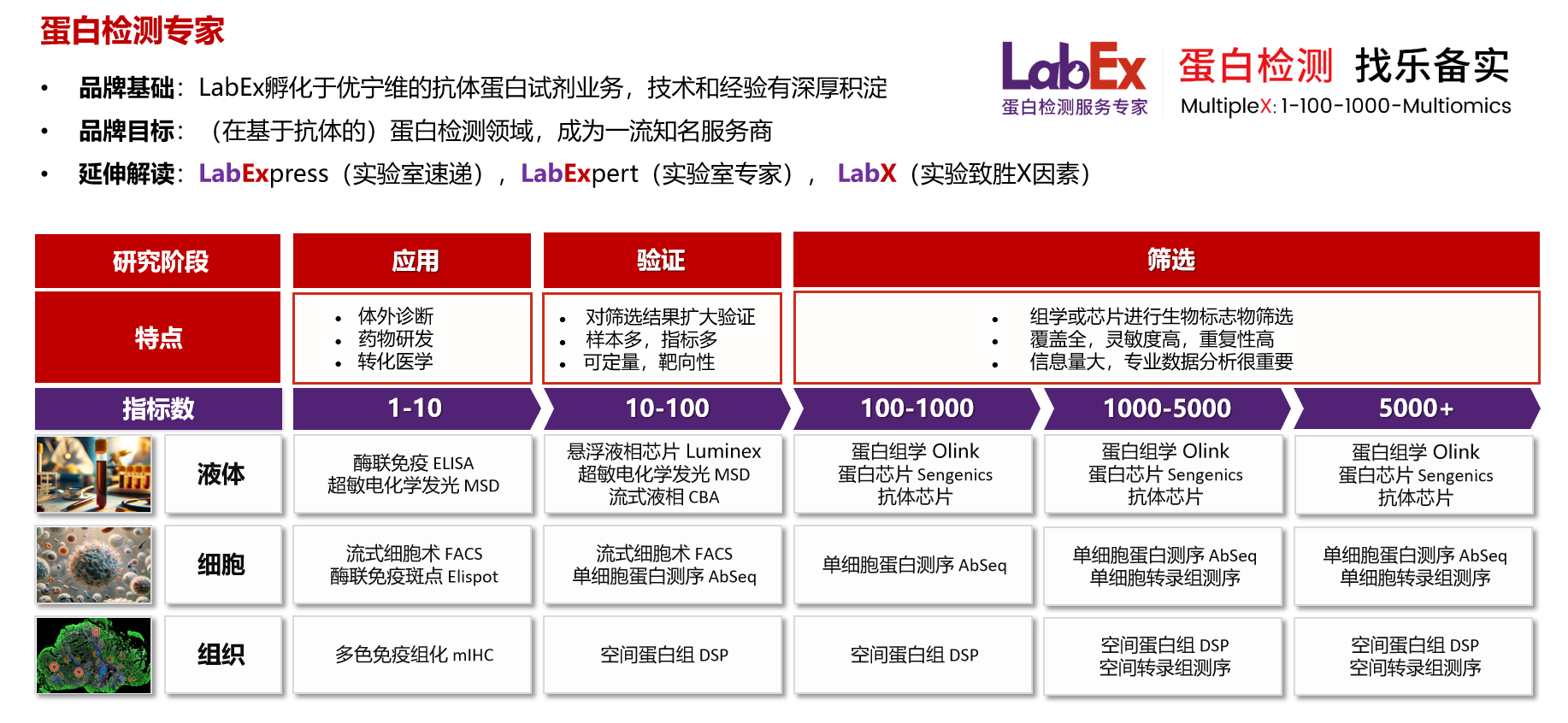
乐备实是国内专注于提供高质量蛋白检测以及组学分析服务的实验服务专家,自2018年成立以来,乐备实不断寻求突破,公司的服务技术平台已扩展到单细胞测序、空间多组学、流式检测、超敏电化学发光、Luminex多因子检测、抗体芯片、PCR Array、ELISA、Elispot、多色免疫组化等30多个,建立起了一套涵盖基因、蛋白、细胞以及组织水平实验的完整检测体系。
我们可提供从样本运输、储存管理、样本制备、样本检测到检测数据分析的全流程服务。凭借严格的实验室管理流程、标准化实验室操作、原始数据储存体系以及实验项目管理系统,已经为超过3000家客户单位提供服务,年检测样本超过100万,受到了广大客户的信任与支持。











 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


