摘要
Hedgehog(Hh)信号通路是进化保守的细胞通讯通路,在胚胎发育、器官形成及成年机体稳态维持中起核心作用,其通过调控细胞增殖、迁移与凋亡相关靶基因表达参与生理过程。RHedgehog 通路 - 一条调控细胞增殖与分化的关键信号转导途径。当 Hh 通路因基因突变、配体异常分泌或微环境紊乱发生组成性激活时,可驱动多种恶性肿瘤发生发展,约 1/3 人类癌症与之相关。非编码 RNA(ncRNA)作为 Hh 通路重要调控因子,通过编码蛋白、吸附 microRNA(miRNA)或结合蛋白质等方式调控通路活性,为癌症诊疗提供新靶点。本文阐述 Hh 通路核心分子组成、传导机制、癌症中异常激活类型,总结 ncRNA 调控机制及临床应用潜力,为癌症精准诊疗提供参考。
一、Hedgehog 信号通路的生物学基础
(一)通路核心组成成分
Hh通路信号转导主要由Hh配体、十二跨膜受体Patched(Ptch)、G蛋白偶联受体Smoothened(Smo)、胶质瘤相关转录因子(Gli)和相关靶基因组成。脊椎动物中有 3 种 Hh 配体:Sonic Hedgehog(Shh)主要分布于神经系统、皮肤和消化道,Indian Hedgehog(Ihh)多见于骨骼和软骨,Desert Hedgehog(Dhh)存在于性腺,三者均能与受体 Patched(Ptch)结合。受体与信号转导蛋白包括 Ptch(Ptch1 和 Ptch2,Ptch1 在间充质细胞中起主导作用)、Smoothened(Smo,G 蛋白偶联受体,为通路 “开关”)及 Gli 转录因子(Gli1、Gli2、Gli3,分激活子与阻遏物)。下游靶基因涵盖负反馈调节基因(如 Hhip)、增殖调控基因(如 Mycn)、细胞周期调控基因(如 CCND1)、凋亡抑制基因(如 Bcl2)、EMT 相关基因(如 Snail)及血管生成基因(如 VEGFA)。

(二)Hh 信号通路的传导机制
Hh 通路信号传递依赖初级纤毛,分无配体抑制和有配体激活两种状态。无配体时,Ptch 定位于初级纤毛,抑制 Smo 膜定位与活性,蛋白激酶复合物磷酸化 Gli2、Gli3,使其裂解为阻遏物(Gli2-R、Gli3-R),进入细胞核抑制靶基因表达。有配体时,Hh 配体与 Ptch 结合,Ptch 内吞降解,Smo 构象激活并迁移至初级纤毛顶端,与 Sufu 蛋白作用释放全长 Gli 蛋白(Gli-A),Gli-A 进入细胞核激活靶基因表达,同时 Hhip 表达形成负反馈调节。
二、Hedgehog 通路在癌症中的异常激活类型
(一)1 型:配体非依赖性致癌激活
由 Hh 通路核心组分基因突变导致,无需配体即可持续激活。如 Smo 激活突变(在基底细胞癌、髓母细胞瘤中常见)使其摆脱 Ptch 抑制;Ptch 失活突变(散发性基底细胞癌中突变频率高)丧失对 Smo 抑制;Sufu 失活突变(髓母细胞瘤、卵巢癌中存在)导致 Gli-A 持续入核激活靶基因。
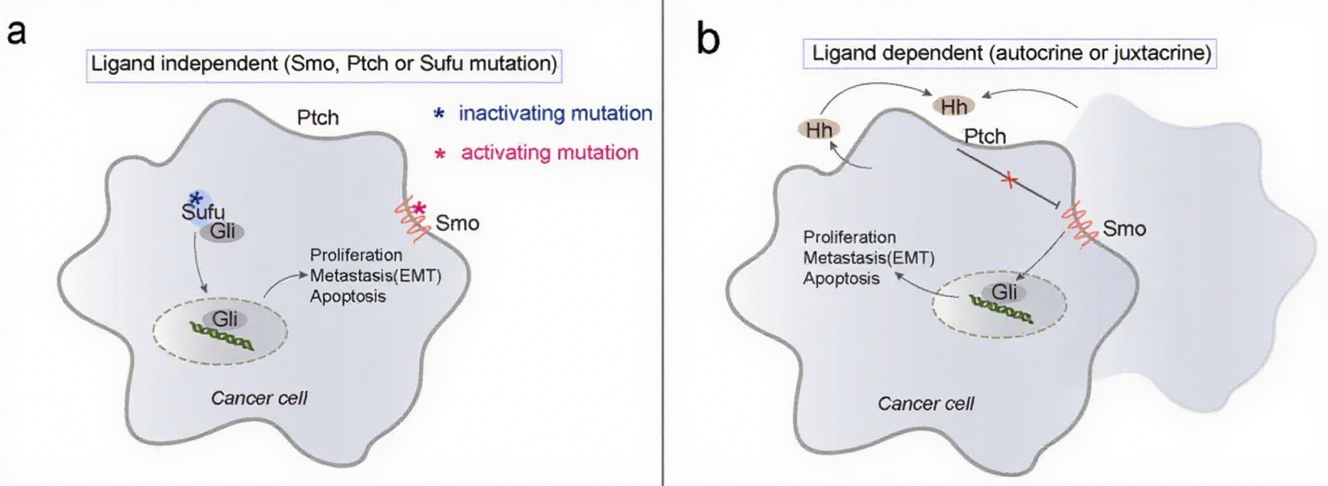
(二)2 型:配体依赖性自分泌激活
依赖肿瘤细胞自身分泌 Hh 配体,通过自分泌循环激活通路。如胃癌中肿瘤细胞高表达 Shh、Ihh,激活通路后上调 CCND1、Bcl2 促进增殖并抑制凋亡;胰腺癌中导管癌细胞分泌 Shh 激活自身通路,诱导 EMT 增强迁移能力。Hh 配体自分泌激活是消化道肿瘤发生的必需条件。
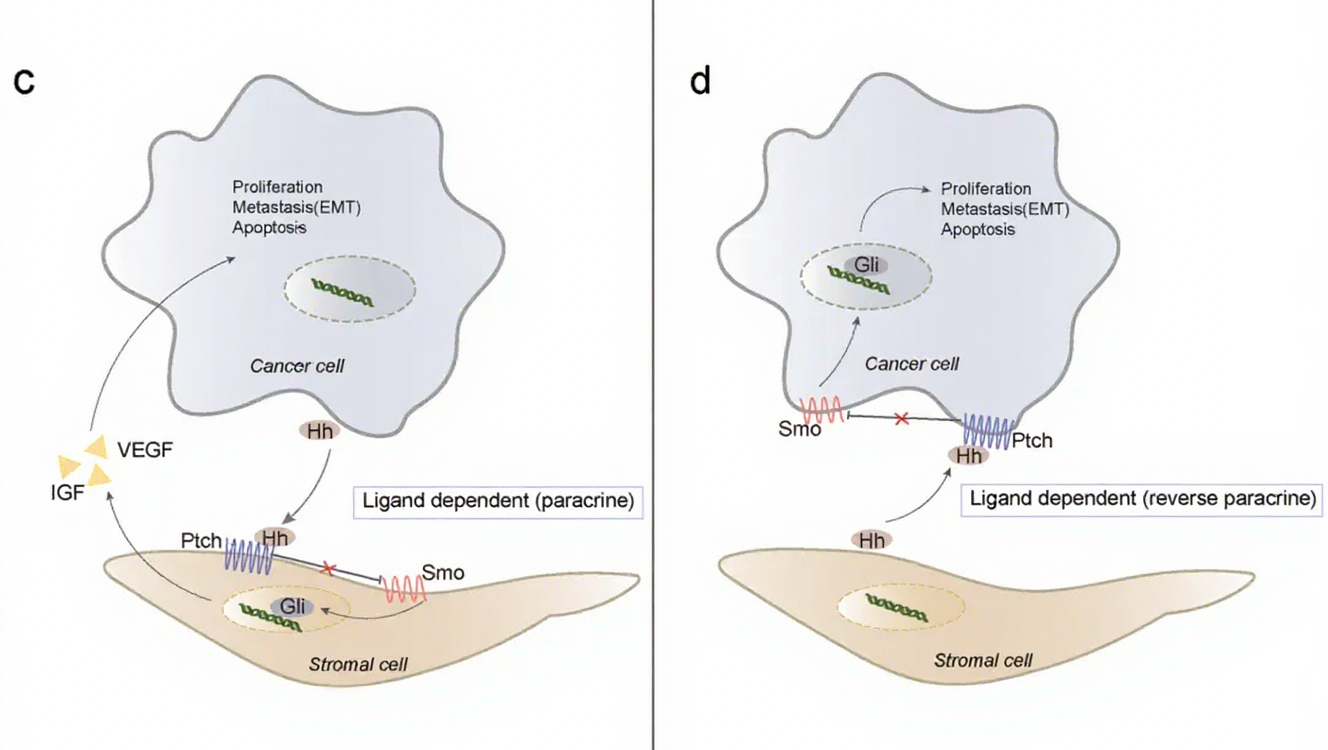
(三)3 型:配体依赖性旁分泌 / 反向旁分泌激活
依赖肿瘤细胞与肿瘤微环境(TME)基质细胞相互作用。旁分泌激活中,肿瘤细胞分泌 Hh 配体激活基质细胞通路,基质细胞分泌 VEGF、IGF-1 等反馈促进肿瘤生长;反向旁分泌激活中,基质细胞分泌 Hh 配体作用于肿瘤细胞,如 B 细胞淋巴瘤、多发性骨髓瘤中,骨髓基质细胞分泌配体维持肿瘤细胞存活增殖。
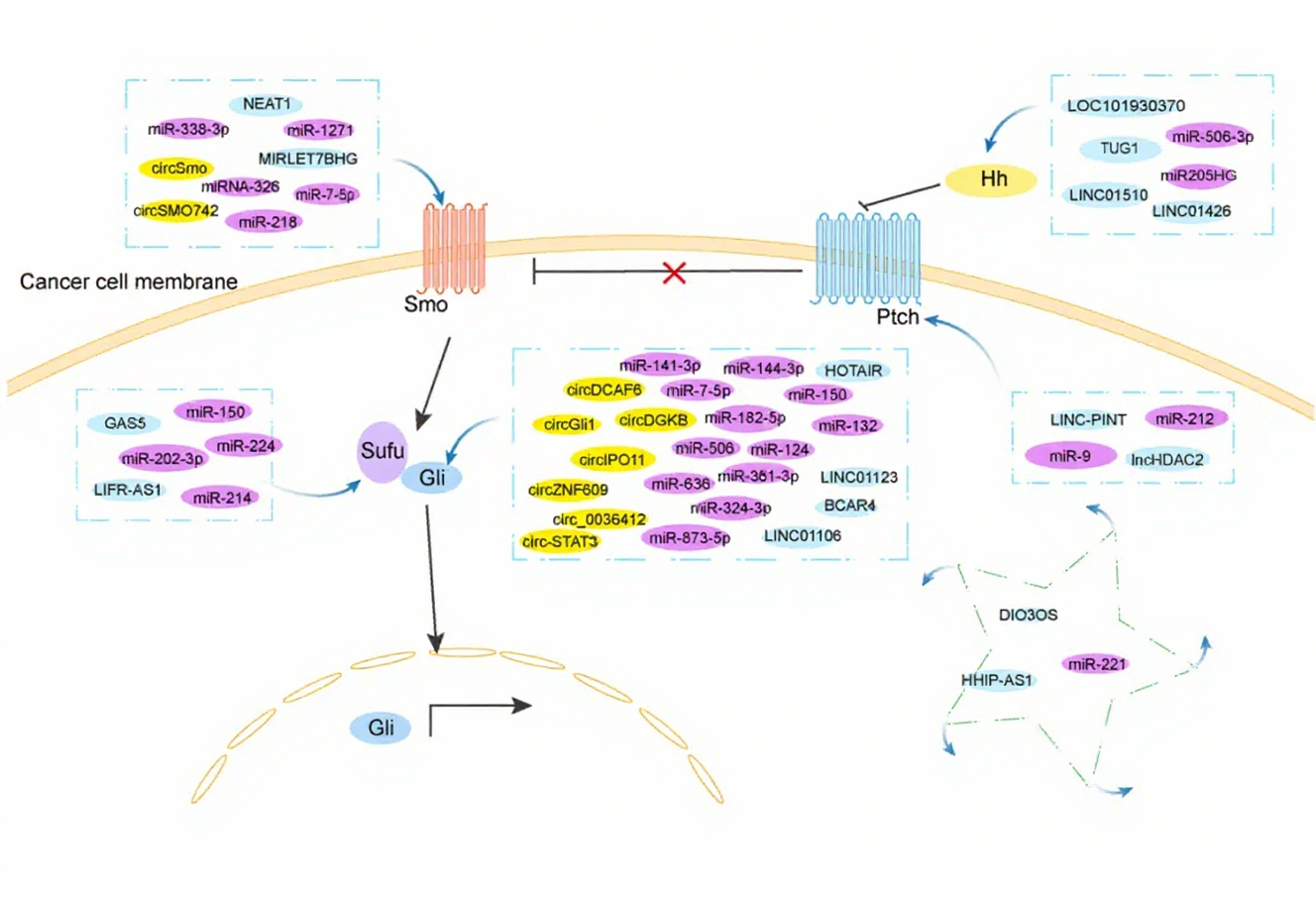
三、非编码 RNA 对 Hedgehog 通路的调控机制
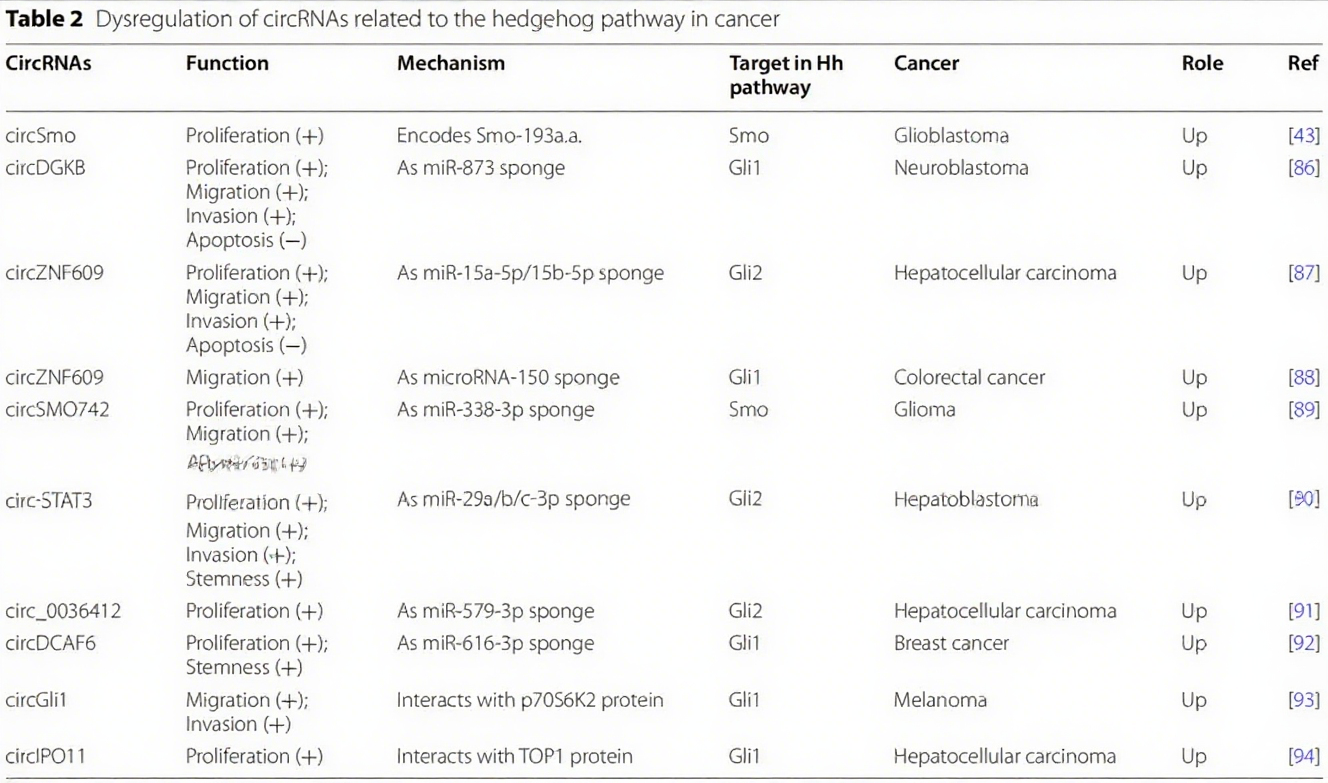
(一)CircRNA 的调控作用
CircRNA 稳定性高、组织特异性强,可编码功能蛋白或吸附 miRNA / 蛋白质调控 Hh 通路。如 circSmo 编码 Smo-193a.a. 蛋白,结合 Smo 增强其胆固醇修饰与激活,上调 Gli1、CCND1 等表达,促进胶质母细胞瘤进展;circCCDC66 在肝癌中吸附 miR-1322,上调 Gli1 表达激活通路。
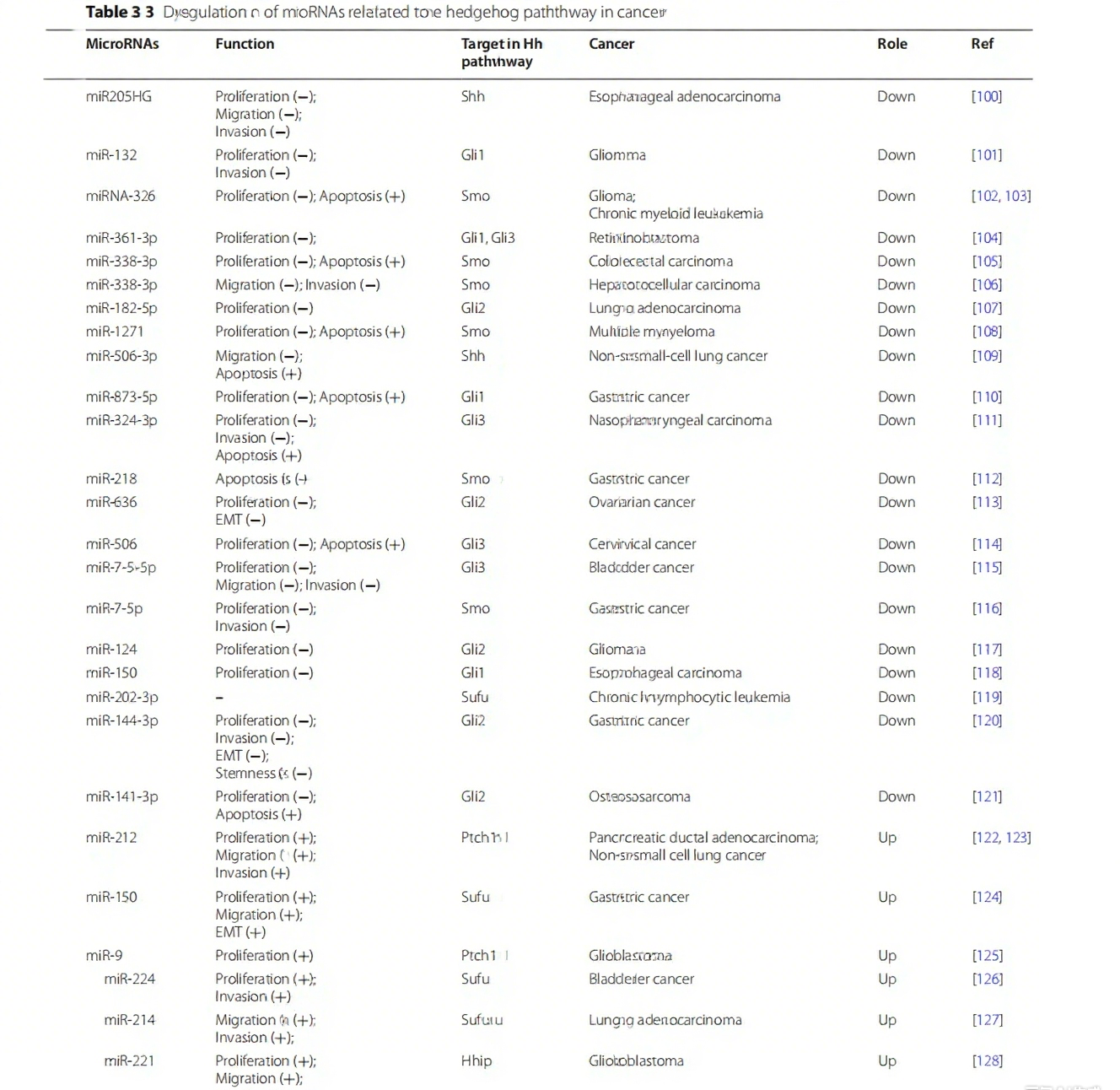
(二)miRNA 的调控作用
miRNA 通过靶向 Hh 通路组分 mRNA 抑制翻译或促进降解调控通路。如 miR-326 在肺癌中靶向 Smo 抑制通路;miR-148a 在胃癌中靶向 Gli1 抑制其表达;miR-124 在胶质母细胞瘤中靶向 CCND1 抑制细胞周期进展。
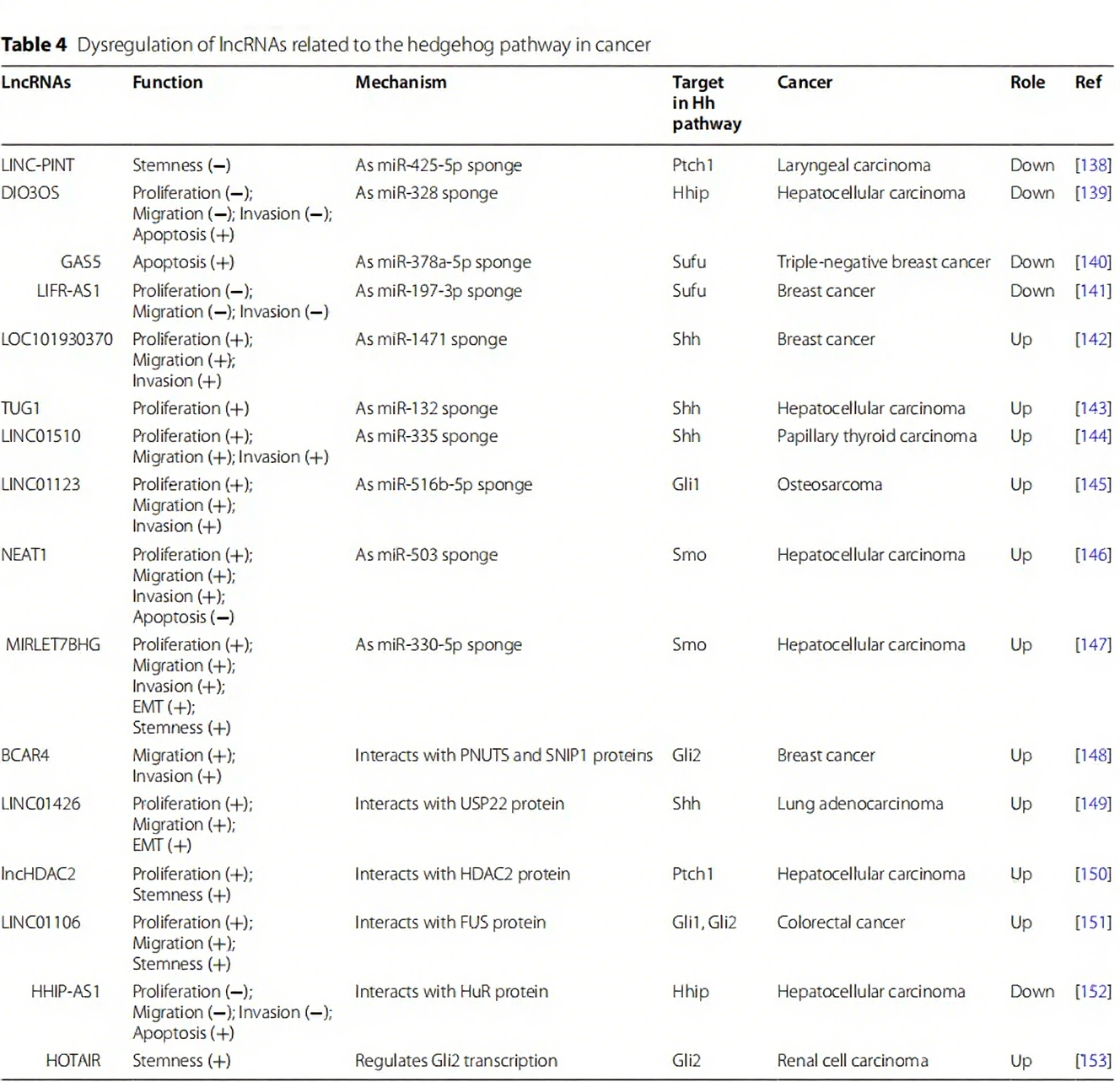
(三)LncRNA 的调控作用
LncRNA 通过吸附 miRNA 或结合蛋白质调控 Hh 通路。如 LINC-PINT 在喉癌中吸附 miR-425-5p,上调 Ptch1 抑制通路;LncRNA BCAR4 在乳腺癌中结合 PNUTS、SNIP1 激活 Gli2 表达;LINC01426 在肺腺癌中募集 USP22 稳定 Shh 蛋白增强通路活性。
四、Hedgehog 通路相关的临床应用潜力
(一)生物标志物开发
Hh 通路相关分子可作为癌症诊断与预后标志物。如胶质母细胞瘤患者血清中 circSmo 高表达与不良预后相关;视网膜母细胞瘤中血清 miR-361-3p 下调可用于诊断;基底细胞癌中 Smo 蛋白高表达可判断肿瘤恶性程度。
(二)治疗策略探索
针对 Hh 通路的治疗策略包括通路抑制剂与 ncRNA 靶向递送系统。Smo 抑制剂维莫德吉已用于晚期基底细胞癌治疗,Gli 抑制剂 GANT61 处于临床前研究阶段。ncRNA 靶向递送系统中,PBAE 纳米颗粒负载 siRNA 靶向 circRNA ciRS-7 可控制肾细胞癌进展,工程化外泌体负载 miR-21 抑制剂与 5 - 氟尿嘧啶可逆转结直肠癌耐药。
五、总结与展望
Hh 通路异常激活是癌症重要驱动因素,ncRNA 对其调控为癌症机制研究提供新视角,相关生物标志物与治疗策略展现临床潜力。RHedgehog 通路功能 - 主导胚胎发育、干细胞维持及组织修复但目前存在抑制剂耐药、ncRNA 递送系统靶向性与安全性待优化、通路交叉调控机制未明等挑战。未来需深入解析调控网络,开发多靶点联合治疗策略,推动精准诊疗技术临床转化。
乐备实是国内专注于提供高质量蛋白检测以及组学分析服务的实验服务专家,自2018年成立以来,乐备实不断寻求突破,公司的服务技术平台已扩展到单细胞测序、空间多组学、流式检测、超敏电化学发光、Luminex多因子检测、抗体芯片、PCR Array、ELISA、Elispot、多色免疫组化等30多个,建立起了一套涵盖基因、蛋白、细胞以及组织水平实验的完整检测体系。
我们可提供从样本运输、储存管理、样本制备、样本检测到检测数据分析的全流程服务。凭借严格的实验室管理流程、标准化实验室操作、原始数据储存体系以及实验项目管理系统,已经为超过3000家客户单位提供服务,年检测样本超过100万,受到了广大客户的信任与支持。











 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


