Treg 细胞:免疫系统的 “平衡守护者”,而非 “攻击者”
 一、Treg 细胞的主要分类
一、Treg 细胞的主要分类根据分化起源与诱导场景,Treg 细胞可分为三大核心类型,各类型的来源与功能定位存在明确差异:
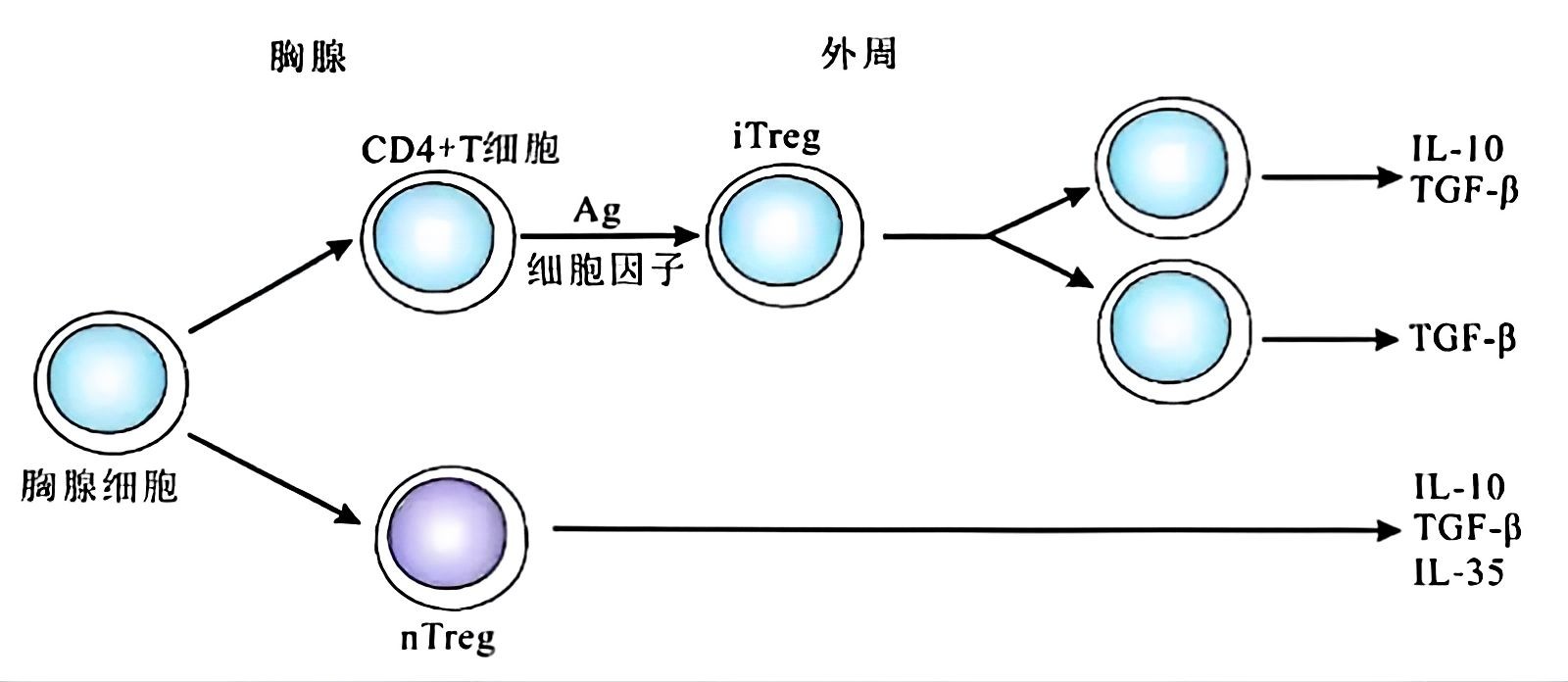
1. 胸腺来源 Treg(tTreg,又称自然 Treg/nTreg)
源于胸腺内的 CD4+T 细胞前体,经 TCR 与自身抗原高亲和力结合、并在胸腺微环境信号诱导下分化成熟,核心表型为CD4⁺CD25⁺Foxp3⁺ 。其主要功能是维持机体系统性免疫耐受,通过抑制自身反应性 T 细胞活化,预防免疫系统 “误伤” 正常组织。
2. 外周诱导 Treg(pTreg)
由外周循环中的初始 CD4+T 细胞,在特定微环境(如肠道黏膜、肿瘤微环境、感染灶)中,经抗原刺激及局部细胞因子(如 TGF-β、IL-10)诱导分化而来。该亚型具有强适应性,可针对性调控局部免疫反应,例如在肠道维持菌群耐受、在肿瘤微环境抑制抗肿瘤免疫。
3. 体外诱导 Treg(iTreg)
借助体外培养体系,用特定抗原、细胞因子(如 TGF-β+IL-2)或小分子化合物诱导初始 CD4+T 细胞分化生成,表型与功能可通过培养条件精准调控,主要用于基础研究或细胞治疗领域(如自身免疫病的细胞干预)。
二、Treg 细胞的共性特征
1. 关键表型标志
各类 Treg 细胞均以CD4⁺CD25⁺Foxp3⁺ 为核心表型,其中转录因子 Foxp3 是 “核心开关”—— 不仅是 Treg 细胞分化成熟的关键调控分子,也是维持其免疫抑制功能的必需因子,Foxp3 表达缺失会导致 Treg 细胞功能完全丧失。
2. 核心功能定位
统一充当免疫系统的 “刹车装置”,通过维持免疫耐受、抑制过度免疫反应(如炎症反应、自身免疫应答、抗肿瘤免疫应答),保障免疫稳态平衡。
三、Treg 细胞的免疫抑制机制
各类 Treg 细胞主要通过三大途径实现免疫抑制,覆盖 “细胞因子调控”“直接分子互作” 与 “资源竞争”:
1. 分泌抑制性细胞因子:释放 IL-10、TGF-β 等细胞因子,广谱抑制效应 T 细胞(如 CD8 + 细胞毒性 T 细胞)活化与增殖,同时限制抗原呈递细胞(如树突状细胞)的功能。
2. 表面分子直接抑制:通过细胞表面的 CTLA-4 分子,竞争性结合抗原呈递细胞表面的 B7 分子,阻断效应 T 细胞通过 CD28-B7 通路获取活化信号;此外,还可通过 LAG-3 等分子直接接触抑制效应 T 细胞。
3. 竞争性消耗 IL-2:高表达 IL-2 受体 α 链(CD25),可优先结合微环境中的 IL-2(效应 T 细胞活化必需的细胞因子),通过 “资源剥夺” 抑制效应 T 细胞增殖。
四、Treg 细胞与疾病的关联
Treg 细胞功能异常(低下或亢进)会打破免疫平衡,进而诱发或加剧疾病:
1. 功能低下 / 缺失:无法有效抑制自身反应性 T 细胞,导致免疫系统攻击自身组织,引发自身免疫病,如 I 型糖尿病(胰岛 β 细胞被破坏)、类风湿关节炎(关节滑膜炎症)、系统性红斑狼疮等。
2. 功能亢进 / 被肿瘤利用:在肿瘤微环境中,Treg 细胞数量增多且功能增强,会强效抑制抗肿瘤免疫应答(如阻止 CD8+T 细胞杀伤肿瘤细胞),导致肿瘤免疫逃逸,促进肿瘤生长与转移。
Treg 细胞疗法:从免疫平衡调控到疾病治疗的多元应用
一、治疗自身免疫病与抗移植排斥:增强 Treg,重建免疫耐受
1. Treg 细胞移植疗法:体外扩增,精准回输
2. 低剂量 IL-2 疗法:体内选择性扩增 Treg
3. 诱导移植耐受:降低抗排异依赖
二、助力癌症免疫治疗:削弱肿瘤内 Treg,释放抗癌潜力
1. 免疫检查点抑制剂:阻断 Treg 的抑制通路
2. 联合治疗:协同提升抗癌疗效
Treg 细胞的发现,让我们读懂免疫系统的强大:它不只拥有对抗外源的 “攻击力”,更具备精妙调控的 “自我克制力” 与稳态平衡能力。从 1995 年坂口志文的孤勇探索,到 2025 年诺贝尔奖的荣光加冕,Treg 细胞的研究之路,本身就是科学探索精神最生动的注脚。
|
技术平台 |
核心技术能力 |
适配外周免疫 / Treg 细胞研究场景 |
|
Luminex 多因子检测平台 |
同步定量 10-100 种细胞因子、趋化因子,灵敏度达 pg/mL 级,支持血清、组织上清、细胞培养物等样本 |
1. 分析 Treg 细胞分泌的抑制性因子(IL-10、TGF-β、IL-35); 2. 检测外周免疫微环境中 Th1/Th2/Th17 因子(IFN-γ、IL-4、IL-17)平衡; 3. 量化炎症部位趋化因子(CCL22、CCR4)以解析 Treg 细胞迁移机制 |
|
单细胞测序平台 |
单细胞转录组、单细胞 TCR/BCR 测序,解析细胞异质性,识别免疫细胞亚型(如 tTreg、pTreg) |
1. 区分外周血 / 组织中 Treg 细胞亚型(胸腺来源 tTreg vs 外周诱导 pTreg); 2. 挖掘 Treg 细胞中 Foxp3 调控的下游基因网络; 3. 分析肿瘤微环境中 Treg 细胞的基因表达特征(如 CTLA-4、CD39 高表达亚型) |
|
流式细胞术平台 |
多色流式检测与细胞分选,支持细胞表面标志物(CD4、CD25、CTLA-4)及胞内因子(Foxp3、IL-10)分析 |
1. 精准分选 CD4+CD25+Foxp3+ Treg 细胞用于体外功能实验; 2. 量化外周血中 Treg 细胞比例及活化状态(如 CD127 低表达); 3. 检测 Treg 细胞与效应 T 细胞的共培养抑制效率 |
|
空间多组学平台(DSP) |
原位检测组织中细胞的空间分布、蛋白表达及基因水平,保留细胞邻域关系(如 Treg 与 DC 细胞互作) |
1. 定位炎症 / 肿瘤组织中 Treg 细胞的浸润区域(如肿瘤间质中 CCR8+Treg); 2. 分析 Treg 细胞与 CD8 + 效应 T 细胞的空间邻近性,评估免疫抑制微环境; 3. 原位验证 Treg 细胞中 Foxp3 与 IL-10 的共表达 |
|
超敏电化学发光(MSD) |
高特异性检测低丰度蛋白(如 Foxp3、磷酸化 STAT5) |
1. 定量检测 Treg 细胞中 Foxp3 蛋白表达量及修饰状态(如磷酸化调控其活性); 2. 验证外周免疫中低丰度细胞因子(如 IL-35); 3. 分析 Treg 细胞信号通路(如 TGF-β/Smad)关键蛋白表达 |
|
生物信息学分析平台 |
多组学数据整合(转录组、蛋白组),支持差异基因筛选、通路富集(如 Treg 细胞免疫抑制通路)、网络构建 |
1. 挖掘 Treg 细胞差异表达基因(如 Foxp3 靶基因); 2. 分析外周免疫紊乱相关通路(如 NF-κB、JAK-STAT)激活状态; 3. 构建 Treg 细胞与免疫微环境的因子互作网络 |
乐备实是国内专注于提供高质量蛋白检测以及组学分析服务的实验服务专家,自2018年成立以来,乐备实不断寻求突破,公司的服务技术平台已扩展到单细胞测序、空间多组学、流式检测、超敏电化学发光、Luminex多因子检测、抗体芯片、PCR Array、ELISA、Elispot、PLA蛋白互作、多色免疫组化、DSP空间多组学等30多个,建立起了一套涵盖基因、蛋白、细胞以及组织水平实验的完整检测体系。
我们可提供从样本运输、储存管理、样本制备、样本检测到检测数据分析的全流程服务。凭借严格的实验室管理流程、标准化实验室操作、原始数据储存体系以及实验项目管理系统,已经为超过3000家客户单位提供服务,年检测样本超过100万,受到了广大客户的信任与支持。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


