摘要:
嵌合抗原受体T细胞(CAR-T)治疗作为癌症免疫治疗领域的革命性技术,通过基因工程改造T细胞以特异性识别并杀伤靶细胞,已在血液恶性肿瘤治疗中取得里程碑式进展,并逐步向实体瘤、自身免疫病等难治性疾病领域拓展。
一、 CAR-T细胞治疗的核心机制与技术演化
(一)作用机制
CAR-T细胞的功能实现依赖于合成受体(CAR)介导的特异性识别与信号激活通路,其完整激活过程包含三个关键阶段:
1. 抗原识别:CAR的单链可变片段(scFv)区域与靶细胞表面抗原特异性结合,确保治疗的靶向性;
2. 信号转导:CAR胞内段的CD3ζ链免疫受体酪氨酸活化基序(ITAM)启动磷酸化级联反应,激活MAPK、PI3K-Akt及NF-κB等下游信号通路;
3. 效应阶段:激活后的CAR-T细胞通过穿孔素-颗粒酶途径或死亡受体介导的凋亡通路杀伤靶细胞,同时分泌IFN-γ等炎症因子,进一步增强局部免疫应答。
(二)技术演化历程
CAR-T技术历经五代迭代,每一代均针对前序版本的缺陷进行核心优化:
第一代(1989年):仅包含CD3ζ信号域,虽能启动T细胞激活,但缺乏共刺激信号,细胞增殖能力与持久性有限;
第二代(2002年):引入CD28或4-1BB共刺激域,显著提升CAR-T细胞的体外扩增效率、体内存活时间及杀伤活性;
第三代(2010年):整合双共刺激域(如CD28+4-1BB),进一步强化信号传导,增强细胞功能稳定性;
第四代(2015年):新增免疫调节功能模块,可分泌IL-12、IL-15等细胞因子或表达抗PD-1单链可变片段,有效重塑免疫抑制性肿瘤微环境;
第五代(2020年):引入细胞因子受体结构域(如截短的IL-2Rβ链)或JAK-STAT信号模块,实现CAR-T细胞的自主增殖与功能持续激活,同时整合逻辑门控构建体提升治疗精准性。
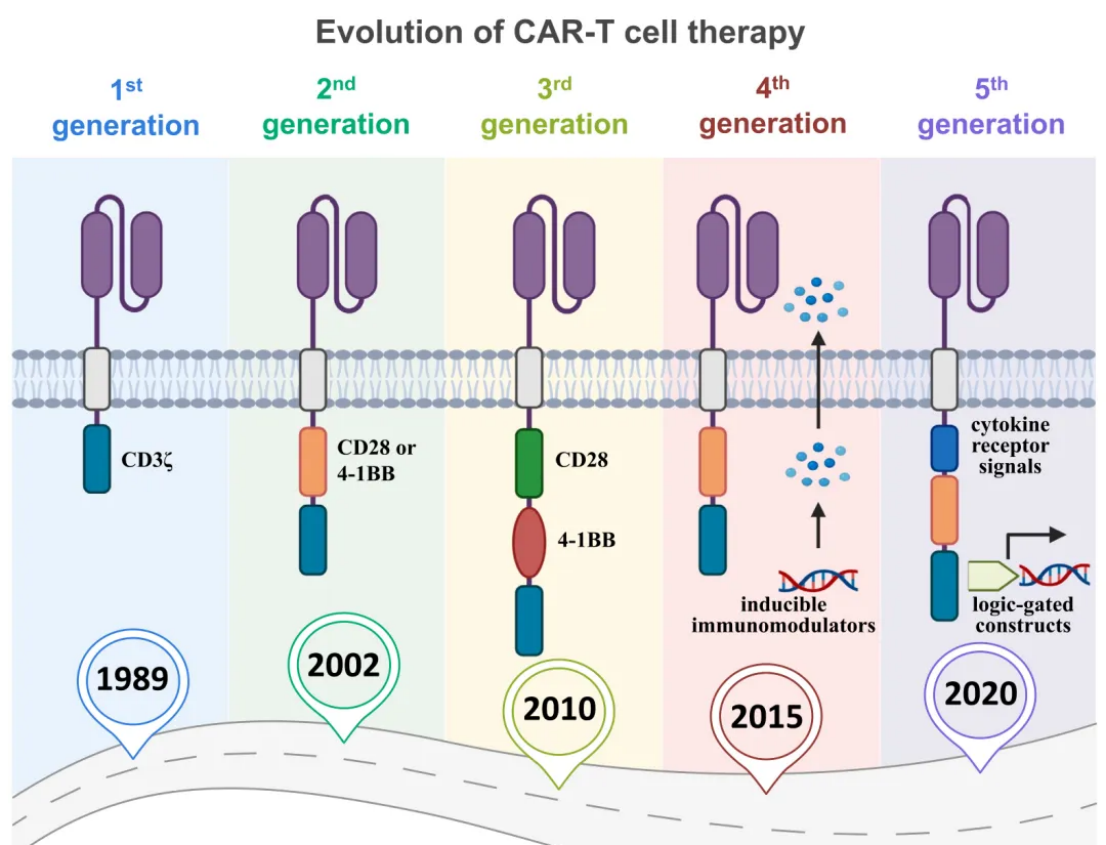
图1:各代CAR-T细胞疗法
二、 CAR-T细胞治疗面临的关键挑战
(一)毒性与安全性问题
CAR-T治疗的安全性风险主要包括:细胞因子释放综合征(CRS)、免疫效应细胞相关神经毒性综合征(ICANS)、脱靶毒性及继发性肿瘤风险。其中,CRS是最常见的急性不良反应,由IL-1、IL-6等炎症因子大量释放引发,在CD70-CAR-T临床试验中,67%的患者出现CRS,3-4级严重反应占3%,严重时可导致多器官功能障碍;ICANS表现为意识障碍、癫痫等症状,其发生与血脑屏障破坏及炎症因子浸润密切相关;脱靶毒性如CD19-CAR-T导致的长期B细胞发育不全,需通过免疫球蛋白替代治疗维持患者免疫功能;此外,病毒载体介导的基因整合可能诱发继发性T细胞恶性肿瘤,限制了治疗的长期安全性。
(二)实体瘤治疗瓶颈
相较于血液肿瘤,CAR-T细胞在实体瘤治疗中疗效受限,核心原因包括:
1. 免疫抑制性肿瘤微环境(TME):实体瘤微环境中存在髓源性抑制细胞(MDSC)、调节性T细胞(Treg)等抑制性细胞亚群,同时缺氧、酸中毒等理化条件会直接抑制CAR-T细胞的浸润与功能;
2. 抗原异质性与逃逸:实体瘤细胞表面靶抗原表达不均一,部分肿瘤细胞可通过下调或丢失靶抗原实现免疫逃逸,导致治疗不完全;
3. T细胞耗竭:持续的抗原刺激会诱导CAR-T细胞表达PD-1、CTLA-4等耗竭相关分子,导致细胞增殖能力下降、杀伤活性减弱。
(三)生产与可及性限制
当前CAR-T治疗的临床转化面临显著的生产与成本挑战:自体CAR-T细胞制备流程复杂,中位制备周期长达108天,且单次治疗成本超过40万美元;此外,41%的淋巴瘤患者因疾病进展迅速,无法在制备周期内接受治疗。这些因素严重限制了CAR-T治疗的普惠性,亟需开发标准化、低成本的生产技术。
三、 CAR-T细胞治疗的技术创新进展
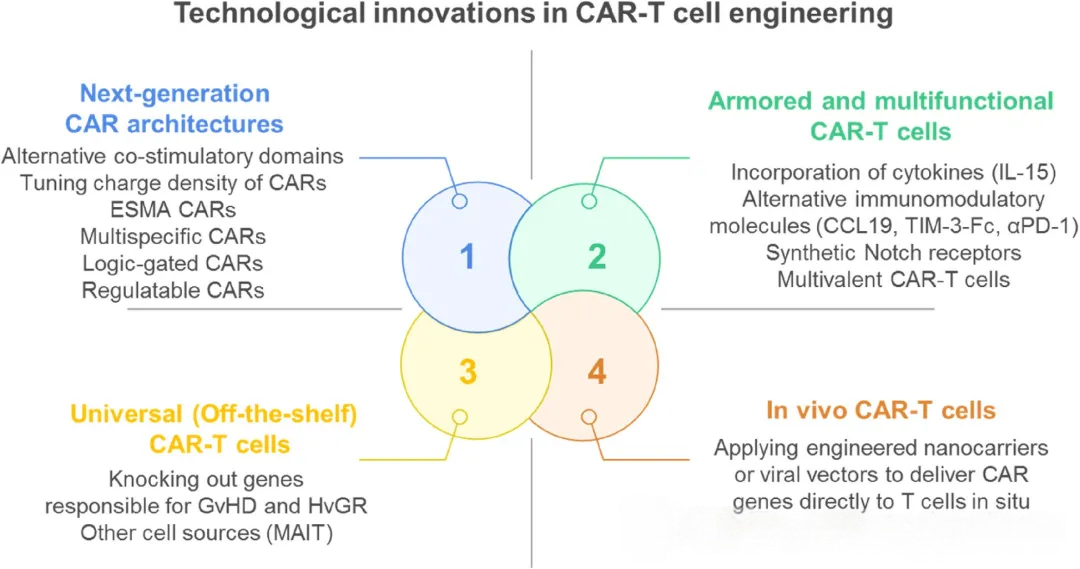
图2:CAR-T细胞工程中的技术创新
(一)新一代CAR结构优化
为提升治疗的精准性与安全性,研究者通过结构设计创新改造CAR分子:
- 信号优化:通过调控CAR胞内段电荷密度降低本底激活信号,增强细胞在体内的适应性; - 内源性信号激活CAR(ESMA-CAR):通过招募内源性信号分子,显著提升对三阴性乳腺癌等实体瘤的靶向杀伤活性;
- 逻辑门控CAR:如SynNotch受体系统,需同时识别肿瘤细胞表面两种抗原才能启动激活,有效降低脱靶毒性,尤其在神经毒性防控方面展现出优势。
(二)装甲与多功能CAR-T技术
通过赋予CAR-T细胞额外功能模块,增强其抗瘤活性与肿瘤微环境适应能力:
细胞因子武装:分泌IL-15、CCL19等细胞因子的CAR-T细胞,在胶质母细胞瘤模型中展现出更强的肿瘤浸润能力与长期存活优势;
多功能设计:如靶向HIV的M10 CAR-T细胞,兼具杀伤感染细胞、中和病毒颗粒及肿瘤归巢功能,为感染性疾病治疗提供了新思路;
抗耗竭工程:通过过表达c-Jun转录因子或敲除DGKα基因,可逆转CAR-T细胞的耗竭表型,恢复其增殖与杀伤功能。
(三)通用型(现货型)CAR-T技术
通用型CAR-T通过基因编辑技术打破自体细胞治疗的局限:利用CRISPR-Cas9技术敲除T细胞受体(TCR)及人类白细胞抗原(HLA)相关基因,显著降低移植物抗宿主病(GVHD)及宿主抗移植物反应(HvGR)风险;此外,模块化CAR平台如ELECTRIC CAR可实现多靶点协同识别,提升对异质性肿瘤的治疗效果,同时简化生产流程,为规模化应用奠定基础。
(四)体内CAR-T技术
体内CAR-T技术通过纳米颗粒或病毒载体直接在体内编程患者自身T细胞,无需体外细胞培养流程,极大简化了治疗环节。该技术的核心优势在于缩短治疗周期、降低生产成本,但目前仍面临预存免疫反应、基因组编辑安全性及体内剂量控制等挑战,需进一步优化载体设计与递送效率。
四、 CAR-T细胞治疗的临床突破
(一)血液恶性肿瘤
CAR-T细胞在血液恶性肿瘤治疗中已实现成熟转化:CD19-CAR-T在儿童及年轻成人复发性/难治性B细胞急性淋巴细胞白血病(B-ALL)的ELIANA临床试验中,客观缓解率(ORR)达82%;针对多发性骨髓瘤的BCMA-CAR-T治疗,ORR高达84.6%,双靶点CAR-T产品GC012F更是实现100%ORR,显著改善了患者预后。
(二)实体瘤
近年来,实体瘤CAR-T治疗取得多项关键突破,核心靶点及疗效如下:Claudin 18.2靶向CAR-T治疗胃癌的ORR达38.8%,治疗胰腺癌的疾病控制率(DCR)为70.8%;GD2靶向CAR-T在神经母细胞瘤治疗中ORR为60%-63%,3年总体生存率(OS)达60%;GPC3靶向CAR-T治疗肝癌的ORR为33%,需通过优化CRS管理提升治疗安全性;B7-H3靶向CAR-T经颅内给药治疗弥漫性内生型桥脑胶质瘤(DIPG),将患者中位生存期延长至10.7个月,为中枢神经系统肿瘤治疗提供了新策略。
(三)自身免疫病
CAR-T治疗已从肿瘤领域拓展至自身免疫病(AID)治疗:在系统性红斑狼疮患者中,CD19-CAR-T治疗实现100%临床缓解,15例患者均成功停药并维持缓解状态;通用型TyU19 CAR-T在免疫性肌病治疗中,有效逆转患者肌无力症状及组织纤维化,为自身免疫病的精准治疗开辟了新路径。
五、未来展望与发展方向
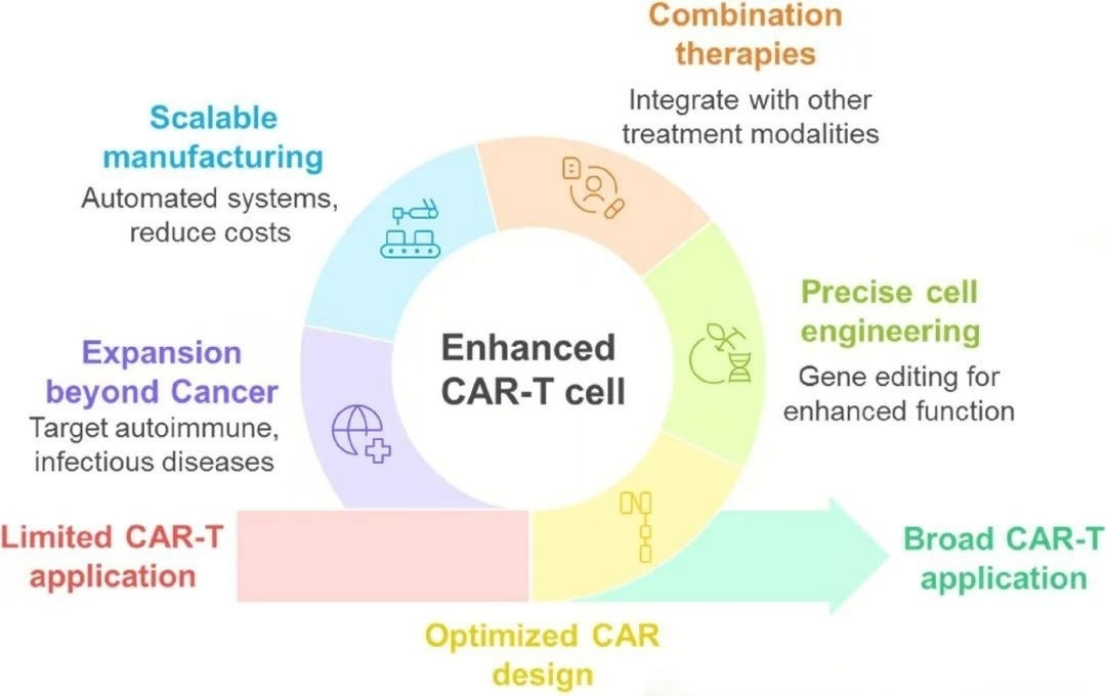
图3:CAR-T细胞治疗的未来前景和潜在策略
(一)CAR设计与细胞工程优化
未来CAR设计将更加注重多功能整合与微环境适应性:开发微环境激活型CAR(如MEAT细胞),仅在肿瘤特异性微环境中启动激活,进一步降低脱靶风险;整合细胞因子分泌、免疫检查点调控等多重功能模块,提升CAR-T细胞在复杂微环境中的存活与杀伤能力。精准基因编辑技术将持续赋能细胞工程,通过CRISPR技术敲除NR4A、CTLA-4等耗竭相关基因,或增强细胞代谢适应性,以抵抗肿瘤微环境的抑制作用。
(二)联合治疗策略
联合治疗是突破CAR-T治疗瓶颈的关键方向:与免疫检查点抑制剂(如抗PD-1抗体)联合使用,可有效逆转T细胞耗竭;结合溶瘤病毒或STING激动剂,能够重塑肿瘤微环境,将"冷肿瘤"转化为"热肿瘤",增强CAR-T细胞浸润;此外,CAR-T治疗与放疗、化疗的协同应用,有望进一步提升治疗效果,尤其在实体瘤的局部控制方面展现出潜力。
(三)规模化生产与成本控制
为提升CAR-T治疗的可及性,规模化生产技术将成为研发重点:自动化生物反应器(如CliniMACS Prodigy)的应用的可标准化生产流程,降低人为误差;非病毒载体(如转座子系统)替代传统病毒载体,可简化制备工艺并降低生产成本;通用型CAR-T的规模化生产将彻底改变当前自体治疗的局限,实现"现货供应",满足更多患者的治疗需求。
(四)非肿瘤领域应用拓展
CAR-T治疗的应用场景正从肿瘤向更多难治性疾病延伸:在感染性疾病领域,靶向HIV感染细胞的M10 CAR-T已展现出抗病毒潜力;在纤维化疾病治疗中,抗FAP-CAR-T可有效逆转肝纤维化,为慢性炎症相关疾病提供新的治疗策略;此外,CAR-T技术在自身免疫病、器官移植排斥反应等领域的应用研究也在持续推进,有望成为多领域疾病治疗的通用技术平台。
六、CAR-T细胞治疗科研服务
CAR-T细胞治疗作为基因治疗与免疫治疗的交叉融合技术,已在血液恶性肿瘤治疗中确立核心地位,并通过技术创新逐步突破实体瘤、自身免疫病等领域的治疗瓶颈。尽管当前仍面临毒性控制、生产可及性等挑战,但新一代CAR结构设计、通用型技术、体内工程及联合治疗策略的发展,正推动CAR-T治疗向更安全、高效、普惠的方向演进。
科研攻关,检测先行!LabEx 作为蛋白检测服务专家,以一站式生物标志物发现平台为 CAR-T 研究赋能。5000 + 核酸蛋白检测指标全覆盖,从单细胞转录组、DSP 空间转录组到多因子检测,贯穿 “筛选 - 验证 - 应用” 全流程,满足 CAR-T 机制探索、毒性监测、疗效标志物筛选等多元需求。
依托 30 + 专业检测平台,累计服务 3000 + 客户、检测 100 万 + 样本的成熟经验,LabEx 可提供高灵敏度、高重复性的数据支撑,搭配专业数据分析团队,助力解析 CAR-T 细胞激活、肿瘤微环境调控等核心科学问题。从基础研究到临床转化,LabEx 全程护航,让科研方向更清晰、成果转化更高效!
选择 LabEx,以精准检测赋能 CAR-T 技术迭代,共绘精准医疗新蓝图!












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


