一、趋化因子的概述
趋化因子是一类具有趋化活性的小分子分泌蛋白,在免疫细胞的定向迁移、炎症反应、组织发育及肿瘤发生发展等生理病理过程中发挥核心调控作用。这些蛋白质通常含有约70-130个氨基酸,其命名系统基于结构特征与功能进行分类,已成为免疫学和细胞生物学研究的重要领域。
二、趋化因子的分子特征与分类
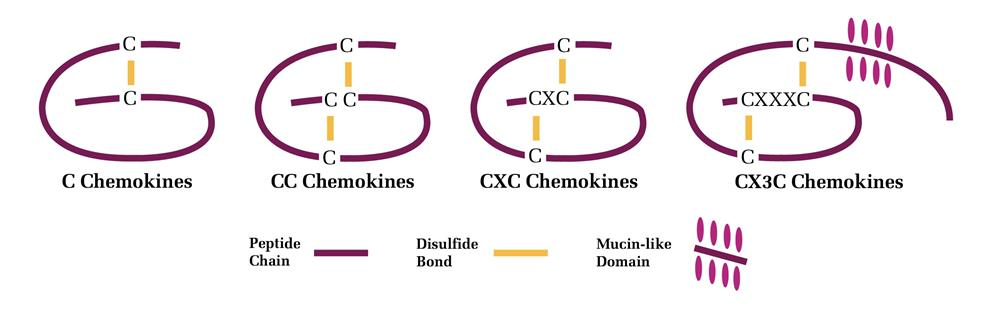
自2000年以来,对人与小鼠基因组的深入分析已全面鉴定了所有趋化因子基因。该家族分子的共同特征为含有四个保守的半胱氨酸残基,可形成两对二硫键(分别连接第1与第3、第2与第4位半胱氨酸)。依据氨基端前两个半胱氨酸残基的间隔模式,趋化因子被划分为四个主要亚家族:
CXC亚家族:前两个半胱氨酸残基之间间隔一个任意氨基酸。
CC亚家族:前两个半胱氨酸残基相邻排列。
CX3C亚家族:目前仅有一个成员(CX3CL1/fractalkine),其前两个半胱氨酸残基之间由三个氨基酸隔开。
(X)C亚家族:该亚家族成员缺少第1与第3位半胱氨酸残基。
此外,理论上可能存在一种“C(X)”亚家族,其特征为缺失前两个半胱氨酸残基而保留第3与第4位残基,但此类分子尚未在哺乳动物中发现。
三、趋化因子的翻译后调控机制
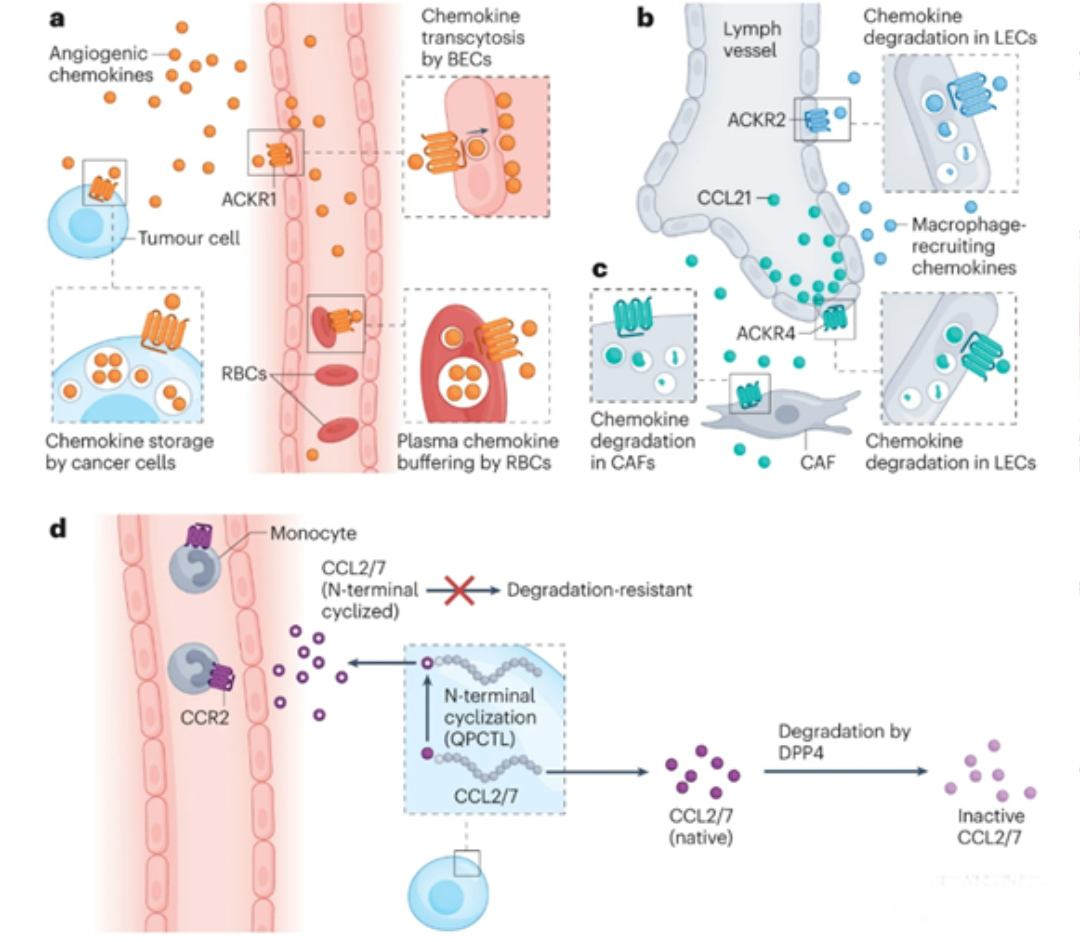
趋化因子的功能实现受到多层次精密调控。除转录水平控制外,其翻译后调控机制包括:RNA的可变剪接与稳定性调控、蛋白质的翻译后修饰(如糖基化)、分泌途径的选择性调控、与细胞外基质成分(特别是糖胺聚糖)的特异性结合,以及与非典型趋化因子受体的相互作用。这些调控机制共同决定了趋化因子的生物利用度、空间分布和功能特异性,使其能够在复杂的生理环境中实现精准的细胞定向引导。
四、趋化因子在癌症治疗中的双重角色
趋化因子及其受体系统在肿瘤发生发展及治疗中发挥着关键作用。一方面,它们可作为重要的生物标志物,用于辅助诊断癌症类型、揭示潜在的致癌机制以及评估患者预后。另一方面,趋化因子信号通路本身已成为极具潜力的治疗干预靶点。
当前,针对趋化因子的治疗策略主要集中在两大方向:
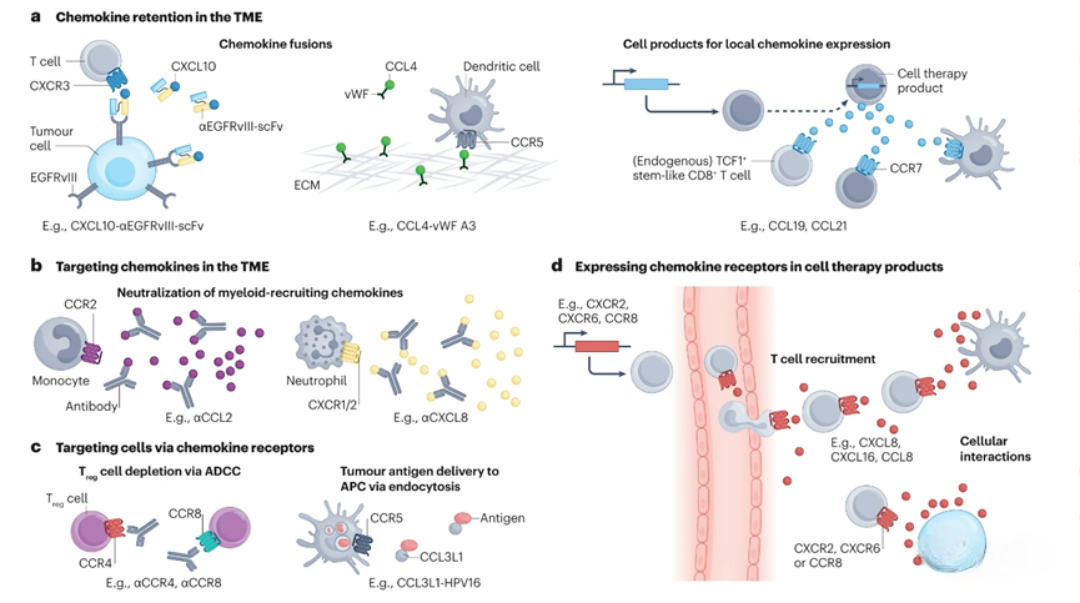
1. 调控肿瘤微环境中的趋化因子浓度与分布
通过主动增加肿瘤微环境内具有抗肿瘤活性的趋化因子水平,可以引导免疫细胞向肿瘤部位募集。例如,将特定趋化因子与能够靶向癌细胞表面抗原的抗体片段融合,可实现治疗性趋化因子在肿瘤部位的定向富集。另一种策略是利用溶瘤病毒作为基因递送载体,使其在肿瘤原位表达并释放趋化因子,从而增强特定效应免疫细胞在肿瘤微环境中的浸润。
2. 改造免疫细胞以增强其向肿瘤的归巢能力
在过继性细胞疗法中,趋化因子受体工程是解决CAR-T细胞等治疗性淋巴细胞肿瘤浸润不足的重要策略。例如,近期一项研究在靶向胶质瘤相关抗原的CAR-T细胞中,额外表达了CXCL8的受体CXCR1或CXCR2。实验结果表明,这两种受体均能显著增强CAR-T细胞在脑肿瘤部位的募集,有效降低肿瘤负荷,并延长荷瘤小鼠的生存期。需要指出的是,虽然该方法能够改善CAR-T细胞向肿瘤部位的归巢,但仍需联合其他策略以克服肿瘤微环境中的免疫抑制问题
五、CTACK/CCL27的特异性生物学功能
趋化因子配体27(CCL27),又称皮肤T细胞吸引趋化因子(CTACK),是CC趋化因子家族的成员。其编码基因位于人类第9号染色体,在皮肤基底角质形成细胞中表达最为丰富,同时在生殖腺、胸腺、胎盘等组织也有表达。在生理状态下,其在皮肤基底上层的表达水平较低,但在特应性皮炎、接触性皮炎和银屑病等皮肤炎症性疾病中表达显著上调。
CCL27通过与特异性受体CCR10结合,在引导记忆T淋巴细胞归巢至皮肤过程中发挥关键作用。动物实验表明,局部注射CCL27可引起注射部位淋巴细胞的特异性聚集,而使用CCL27中和抗体则能抑制这种聚集现象。其表达受到促炎因子(如TNF-α和IL-1)的正向调控以及糖皮质激素的负向调控。
值得注意的是,CCL27显示出高度的组织特异性,这一特性使其成为研究组织特异性免疫反应的理想模型,也为开发皮肤特异性疾病的靶向治疗提供了新的思路。在肿瘤领域,CCL27-CCR10轴在皮肤相关肿瘤(如黑色素瘤)的发生发展中的作用也受到越来越多的关注,可能成为未来联合治疗策略的重要组成部分。
六、CTACK/CCL27因子检测服务哪个公司提供?
LabEx为您提供专业、特异的CTACK/CCL27因子检测服务。CTACK/CCL27作为皮肤归巢T细胞关键的趋化因子,在调节淋巴细胞向皮肤组织的特异性迁移、介导皮肤炎症与免疫应答中扮演核心角色。
| 货号 | Panel名称 | 种属 | 检测指标 |
| LXLBH40-1 | 人趋化因子/细胞因子-40因子Panel | Human | 6Ckine/CCL21,BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin/CCL11,Eotaxin-2/CCL24,Eotaxin-3/CCL26,Fractalkine/CX3CL1,GCP-2/CXCL6,GM-CSF,GRO-α (Gro-a/KC/CXCL1),Gro-β/CXCL2,I-309/CCL1,IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-8/CXCL8,IL-10,IL-16,IP-10/CXCL10,I-TAC/CXCL11,MCP-1/CCL2,MCP-2/CCL8,MCP-3/CCL7,MCP-4/CCL13,MDC/CCL22,MIF,MIG/CXCL9,MIP-1α/CCL3,MIP-1δ/CCL15,MIP-3α/CCL20,MIP-3β/CCL19,MPIF-1/CCL23,SCYB16/CXCL16,SDF-1α+β/CXCL12,TARC/CCL17,TECK/CCL25,TNF-α |
| LXLBM31-1 | 小鼠趋化因子-31因子Panel | Mouse | BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin/CCL11,Eotaxin-2/CCL24,Fractalkine/CX3CL1,GM-CSF,I-309/CCL1,IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-10,IL-16,IP-10/CXCL10,I-TAC/CXCL11,KC/CXCL1,MCP-1/CCL2,MCP-3/CCL7,MCP-5/CCL12,MDC/CCL22,MIP-1α/CCL3,MIP-1β/CCL4,MIP-3α/CCL20,MIP-3β/CCL19,RANTES/CCL5,SCYB16/CXCL16,SDF-1α/CXCL12,TARC/CCL17,TNF-α |
| LXRLBH40-1 | 人趋化因子/细胞因子-40因子Panel | Human | GM-CSF,IFN-γ,IL-10,IL-16,IL-2,IL-4,IL-6,IL-8/CXCL8,MIF,SCYB16/CXCL16,TNF-α,MIP-1δ/CCL15,6Ckine/CCL21,BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin/CCL11,Eotaxin-2/CCL24,Eotaxin-3/CCL26,Fractalkine/CX3CL1,GCP-2/CXCL6,GRO-α (Gro-a/KC/CXCL1),Gro-β/CXCL2,I-309/CCL1,IL-1β,IP-10/CXCL10,I-TAC/CXCL11,MCP-1/CCL2,MCP-2/CCL8,MCP-3/CCL7,MCP-4/CCL13,MDC/CCL22,MIG/CXCL9,MIP-1α/CCL3,MIP-3α/CCL20,MIP-3β/CCL19,MPIF-1/CCL23,SDF-1α+β/CXCL12,TARC/CCL17,TECK/CCL25 |












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


