摘要
免疫检查点抑制剂虽已成为癌症治疗的重要手段,但临床上面临着响应率低与耐药性的严峻挑战,其核心瓶颈在于肿瘤微环境(TME)中复杂的免疫抑制状态。2025年11月,曹雪涛院士团队在《Immunity》期刊发表的研究首次揭示了肿瘤细胞的一种关键代谢途径——巨胞饮,在免疫逃逸中的全新作用。该研究通过高通量筛选鉴定出二氢乳清酸脱氢酶(DHODH) 是驱动肿瘤巨胞饮的核心因子。机制上,DHODH通过影响蛋白质的O-GlcNAc糖基化修饰,维持神经纤毛蛋白1(NRP1)的膜定位以促进巨胞饮;进而,巨胞饮摄取的蛋白质为肿瘤提供氨基酸,导致CIITA发生戊二酰化修饰,从而抑制MHC II类分子的表达,削弱肿瘤免疫原性。在抗PD1耐药的肿瘤模型中,靶向DHODH不仅能直接抑制肿瘤生长,更能重塑免疫微环境,显著增强抗PD1抗体的治疗效果,且该疗效依赖于CD4⁺和CD8⁺ T细胞。这项研究首次将细胞代谢、巨胞饮与肿瘤免疫逃逸直接联系起来,为克服免疫治疗耐药提供了极具潜力的新靶点和联合治疗策略。

一、研究背景:免疫治疗耐药的代谢新视角
肿瘤细胞如何在营养匮乏的微环境中存活并逃避免疫监视,是癌症研究的核心问题。近年来,肿瘤代谢重编程与免疫逃逸的关联备受关注。巨胞饮作用是肿瘤细胞摄取胞外营养物质(如蛋白质、脂质)的一种非选择性胞吞方式,已知能支持肿瘤在恶劣环境中的生长。然而,巨胞饮过程是否以及如何参与肿瘤的免疫逃逸,长期以来尚不明确。曹雪涛院士团队的最新研究正是以此为切入点,探索了驱动巨胞饮的关键分子及其在免疫抑制中的作用,为理解免疫治疗耐药机制和开发新型增敏策略提供了全新视角。
一、核心发现
(一)DHODH是驱动肿瘤细胞巨胞饮的必需因子
研究团队通过双轨筛选策略,首次将DHODH 鉴定为肿瘤巨胞饮的核心调控因子。
1. 双筛选策略锁定DHODH:
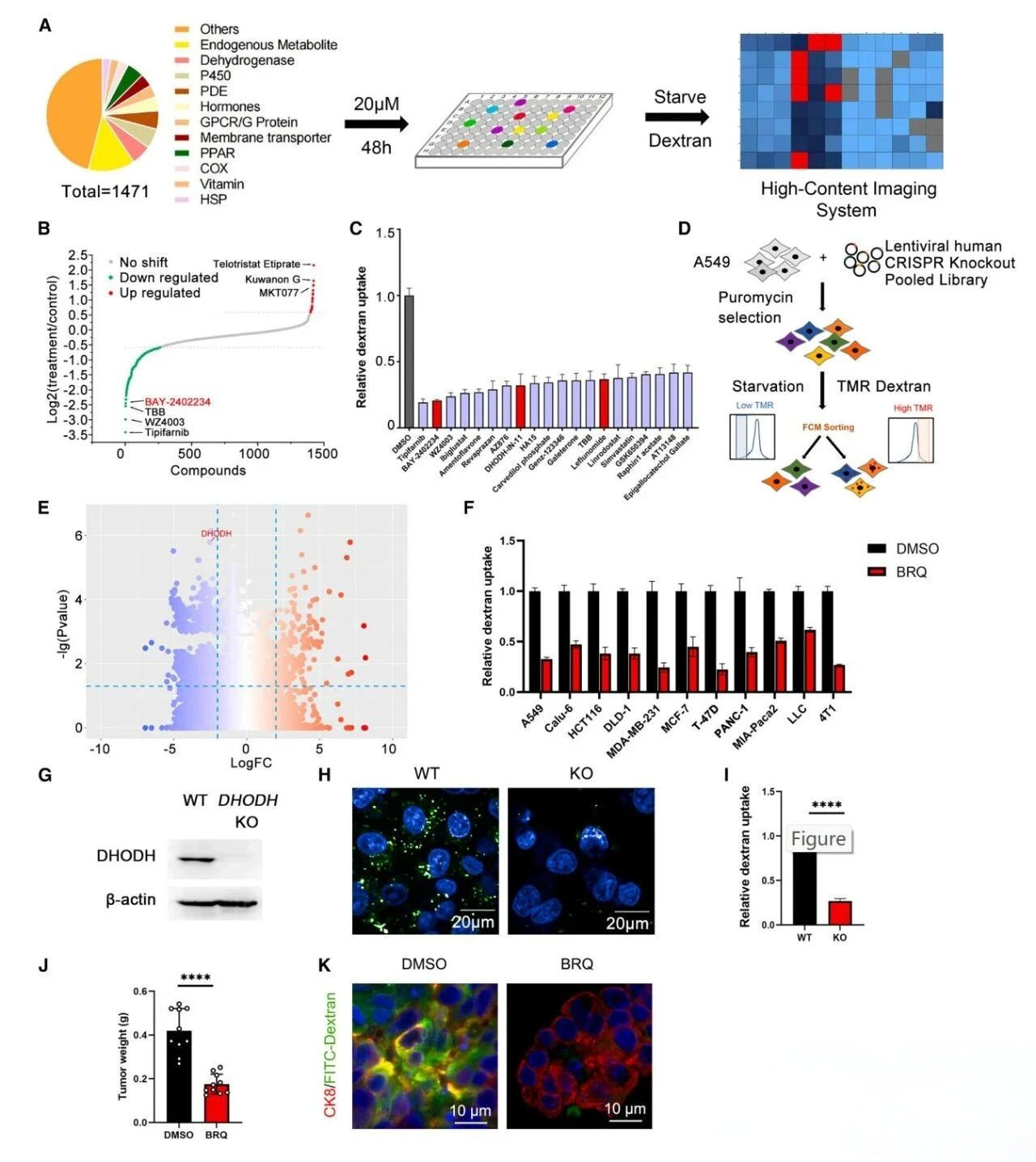
(1)代谢化合物库筛选:在肺癌(A549)、结直肠癌(DLD-1)等多种细胞系中,利用包含1471种代谢相关化合物的文库进行筛选,以细胞对荧光标记葡聚糖(巨胞饮底物)的摄取效率为指标。结果显示,三种不同的DHODH抑制剂(包括临床在研药物BAY2402234)能显著降低巨胞饮效率,在验证筛选中名列前茅。
(2)全基因组CRISPR-Cas9筛选:在A549细胞中构建基因敲除文库,并分选出巨胞饮能力低的细胞进行测序分析。结果同样表明,DHODH基因是富集度最高的候选基因之一。
Wang Y, Chai Y, et al. Inhibition of tumor cell macropinocytosis driver DHODH reverses immunosuppression and overcomes anti-PD1 resistance. Immunity. 2025 Oct 14;58(10):2456-2471.e6.
2. 功能验证:
(1)体外:使用DHODH抑制剂(BRQ、BAY2402234)或基因敲除DHODH,均能在多种人源和鼠源肿瘤细胞中显著降低巨胞饮能力,且不影响基础细胞活力。在模拟TME营养匮乏(缺乏亮氨酸,添加白蛋白)的条件下,抑制DHODH能有效阻断肿瘤细胞通过巨胞饮获取营养而存活增殖的能力。
(2)体内:在小鼠皮下移植瘤模型和MMTV-PyMT自发乳腺肿瘤模型中,敲低或抑制DHODH均能显著减缓肿瘤生长,并通过瘤内注射荧光葡聚糖证实,其体内抗肿瘤效果直接与肿瘤细胞巨胞饮能力的下降相关。
(二)DHODH通过调控NRP1的膜定位促进巨胞饮
为阐明DHODH调控巨胞饮的分子机制,研究者进行了深入的膜蛋白质组学分析。
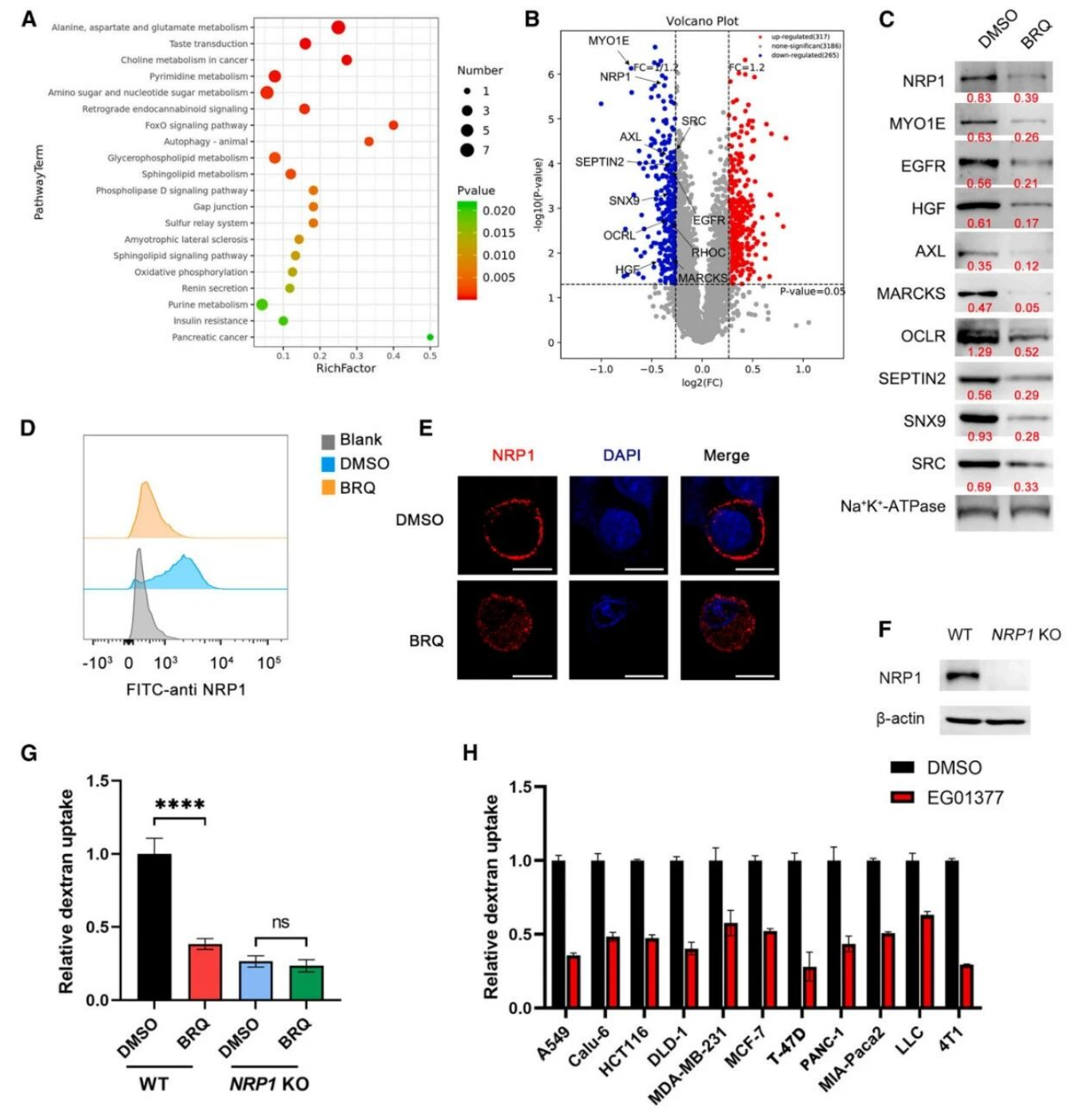
1. 锁定关键蛋白NRP1:结果发现,抑制DHODH后,多种与巨胞饮相关的蛋白(如AXL、EGFR)在细胞膜上的表达量下降。其中,神经纤毛蛋白1(NRP1) 的膜定位显著减少,但其总蛋白水平并未改变,提示DHODH影响的是NRP1的亚细胞定位而非其表达。
2. 确立NRP1在通路中的位置:功能实验表明,敲低NRP1本身即可抑制巨胞饮,且在此背景下使用DHODH抑制剂无法进一步抑制巨胞饮;而使用NRP1抑制剂同样能抑制巨胞饮。这些结果有力证明,DHODH通过作用于NRP1上游来调控巨胞饮过程。
Wang Y, Chai Y, et al. Inhibition of tumor cell macropinocytosis driver DHODH reverses immunosuppression and overcomes anti-PD1 resistance. Immunity. 2025 Oct 14;58(10):2456-2471.e6.
(三)揭示“DHODH-巨胞饮轴”通过CIITA戊二酰化抑制MHC II的免疫逃逸新机制
该研究的突破性在于,不仅阐明了DHODH如何驱动巨胞饮,更揭示了这一代谢通路如何与肿瘤的免疫原性直接关联。
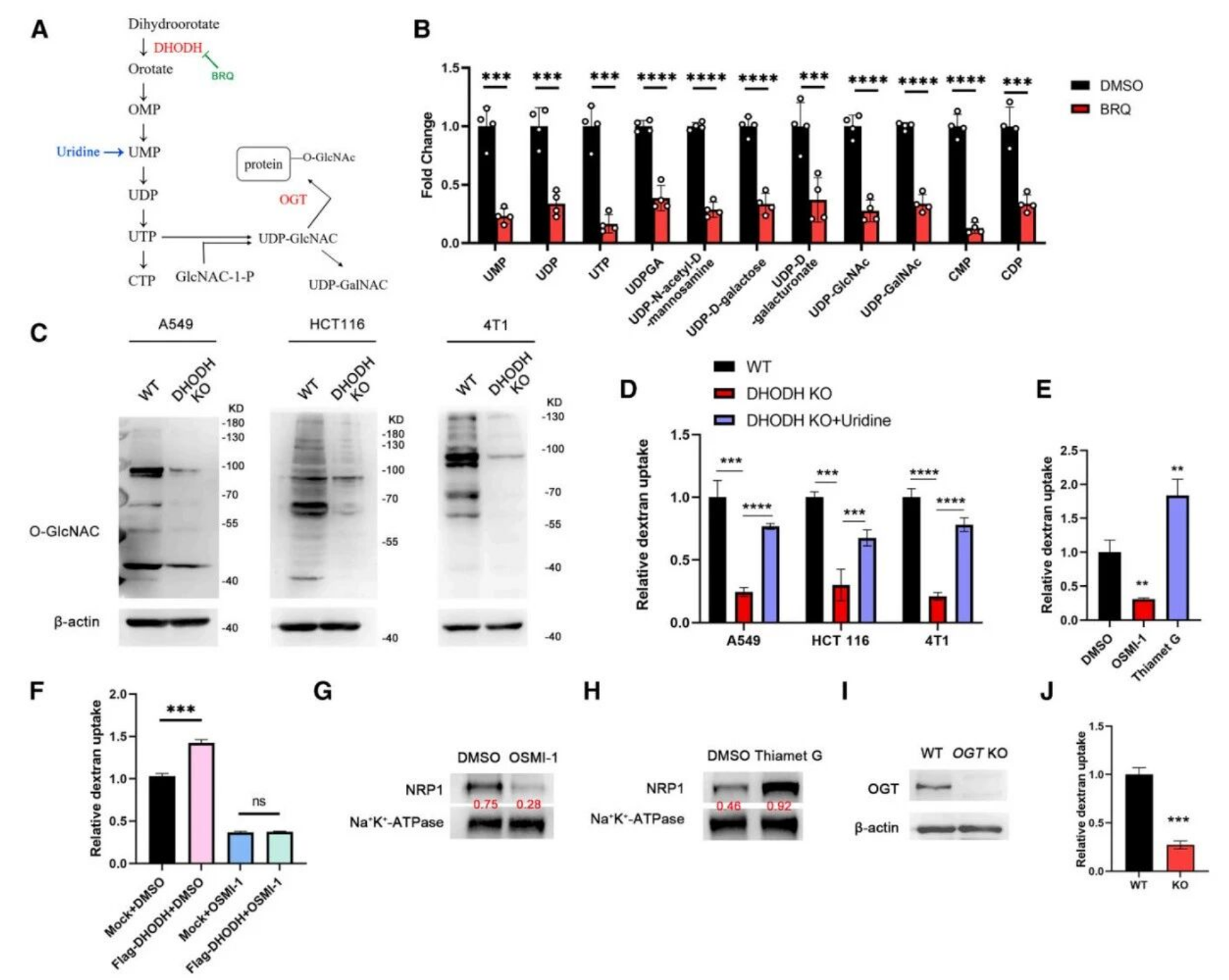
1. DHODH的代谢功能与蛋白修饰:DHODH是嘧啶合成通路的关键酶。研究发现,抑制DHODH会导致下游UDP-糖核苷酸(特别是UDP-GlcNAc)水平下降,进而降低蛋白质的O-GlcNAc糖基化修饰水平。通过外源补充尿苷(绕过DHODH作用)或直接干预O-GlcNAc转移酶(OGT),证实DHODH正是通过调控O-GlcNAc修饰来影响NRP1的膜定位和巨胞饮功能。
2. 连接巨胞饮与MHC II抑制:研究进一步追踪发现,活跃的DHODH-巨胞饮轴会为肿瘤细胞提供大量氨基酸(如赖氨酸、色氨酸),这些代谢物的积累促进了主要组织相容性复合体II类分子(MHC II)转录激活因子CIITA的戊二酰化修饰。这种修饰抑制了CIITA的活性,导致MHC II分子的转录被抑制,从而削弱了肿瘤细胞将抗原呈递给CD4⁺ T细胞的能力,最终实现免疫逃逸。
Wang Y, Chai Y, et al. Inhibition of tumor cell macropinocytosis driver DHODH reverses immunosuppression and overcomes anti-PD1 resistance. Immunity. 2025 Oct 14;58(10):2456-2471.e6.
(四)靶向DHODH逆转抗PD1耐药并重塑免疫微环境
基于上述机制,研究团队在具有天然抗PD1耐药性的4T1小鼠乳腺肿瘤模型中,评估了靶向DHODH的联合治疗潜力。
1. 联合治疗显著增效:单独使用抗PD1抗体对肿瘤生长无抑制作用,而单独使用DHODH抑制剂(BRQ)能部分抑制肿瘤。当BRQ与抗PD1抗体联合使用时,抑瘤效果最为显著,同时伴随着肿瘤细胞表面MHC II表达的上调。
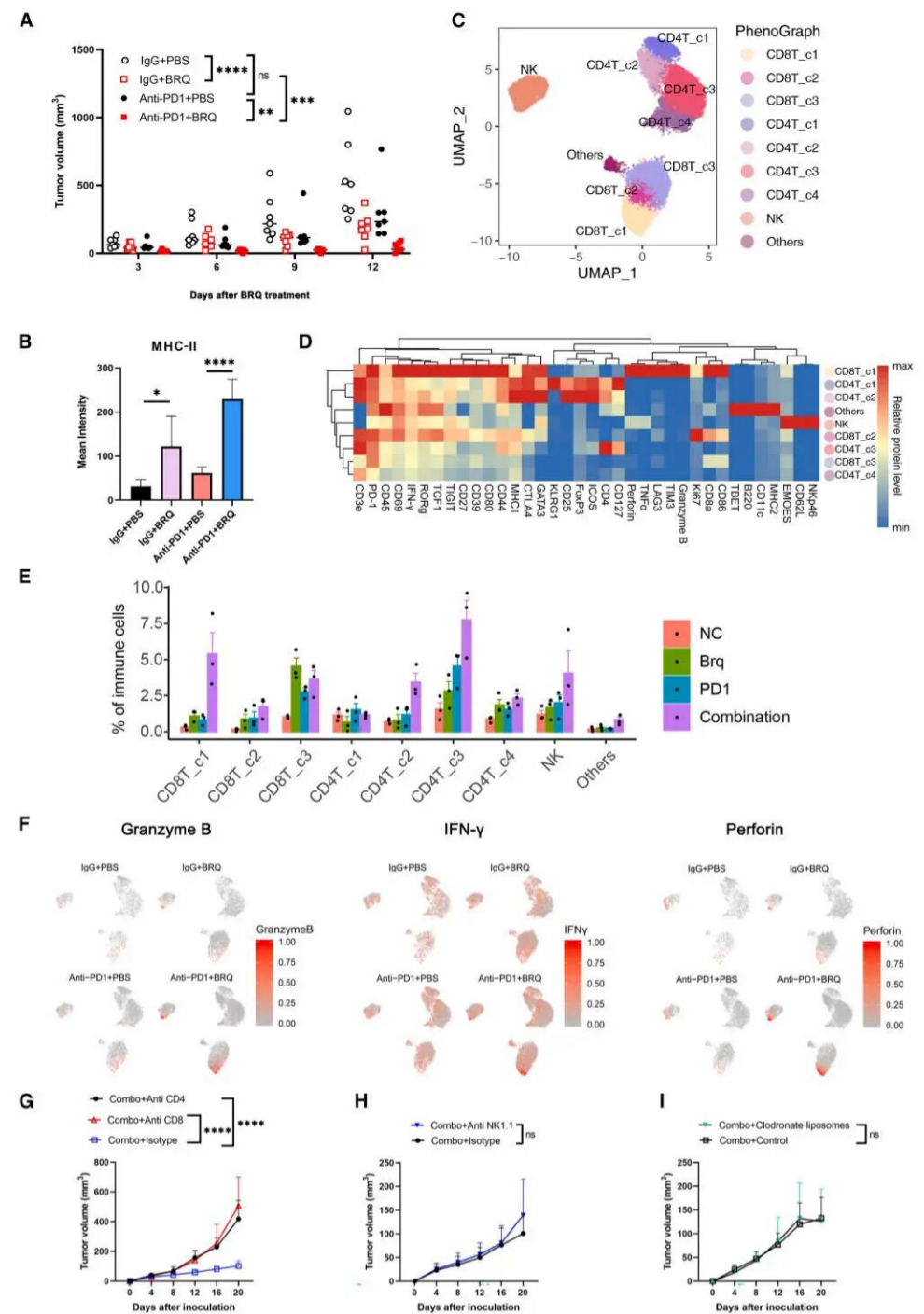
2. 免疫微环境重塑:通过质谱流式(CyTOF)分析发现,联合治疗显著重塑了肿瘤免疫微环境:
(1)T细胞:富集了具有抗肿瘤潜能的“终末耗竭CD8⁺ T细胞”和激活的效应记忆CD4⁺ T细胞。
(2)树突状细胞(DC):关键抗原呈递亚群——1型常规树突细胞(cDC1)显著增加。
(3)抑制性细胞:免疫抑制性的中性粒细胞亚群减少。
3. 疗效依赖于T细胞,靶点在肿瘤细胞:通过细胞耗竭实验证实,联合治疗的抑瘤效果完全依赖于CD4⁺和CD8⁺ T细胞,而非NK细胞或巨噬细胞。更重要的是,使用DHODH基因敲除的肿瘤细胞进行实验,发现BRQ的疗效消失,且这些肿瘤本身对抗PD1治疗的敏感性恢复。这明确证明,BRQ的治疗靶点正是肿瘤细胞自身的DHODH。
Wang Y, Chai Y, et al. Inhibition of tumor cell macropinocytosis driver DHODH reverses immunosuppression and overcomes anti-PD1 resistance. Immunity. 2025 Oct 14;58(10):2456-2471.e6.
三、总结与展望:意义、局限与未来方向
这项发表于《Immunity》的研究具有重要的科学意义和临床转化潜力。
(一)核心创新与意义
概念突破:首次将DHODH驱动的代谢过程与肿瘤巨胞饮及免疫逃逸直接联系起来,提出了“代谢-免疫”交叉调控的新范式。
机制新颖:完整阐明了 “DHODH–O-GlcNAc修饰–NRP1膜定位–巨胞饮–氨基酸积累–CIITA戊二酰化–MHC II抑制” 这一全新的信号轴。
治疗策略:为克服免疫检查点抑制剂耐药提供了极具前景的联合治疗策略,即靶向肿瘤细胞代谢(DHODH)以增强其免疫原性,进而协同免疫检查点阻断。DHODH和NRP1也有望成为预测免疫治疗疗效的生物标志物。
(二)研究局限与未来方向
1. 安全性考量:DHODH是全身广泛表达的代谢酶,系统性抑制可能带来潜在的毒副作用,需要开发更具肿瘤靶向性的递送系统或联合用药方案。
2. 机制细节:CIITA戊二酰化修饰如何精确调控其功能,以及DHODH是否还通过其他通路(如影响铁死亡)参与免疫调控,有待进一步研究。
3. 临床验证:该发现主要基于临床前模型,其在人类患者中的疗效和安全性仍需通过后续的临床试验进行验证。
综上所述,曹雪涛院士团队的这项研究不仅深化了我们对肿瘤免疫逃逸复杂性的理解,更为下一代免疫联合治疗策略的设计提供了坚实的理论基础和一个极具吸引力的药物靶点——DHODH。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


