人体免疫系统如何精准地区分“自己”与“非己”,并在清除病原的同时避免攻击自身组织,一直是免疫学研究的核心。作为免疫系统的“哨兵”,经典树突状细胞(cDC)在识别外来病原、启动免疫应答中的作用已被充分阐明。然而,在健康稳态下,这些DC细胞是处于“闲置”状态,还是主动参与维持对自身组织的耐受?这一问题长期悬而未决。
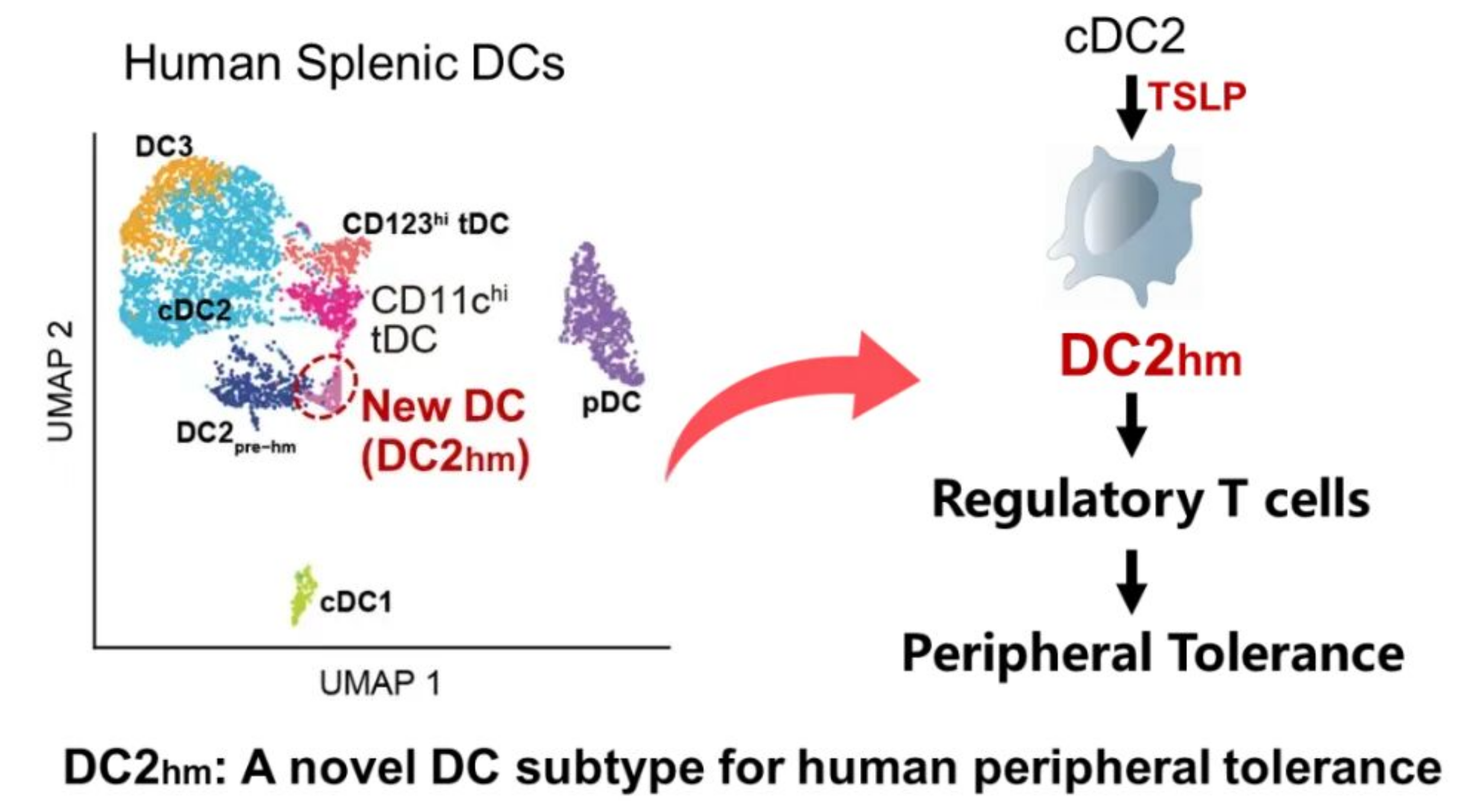
2026年2月18日,武汉大学医学研究院程亮课题组在《Immunity》期刊发表的一项研究,为这一谜题提供了突破性答案。该研究首次发现并命名了一类全新的、在人体稳态下发挥关键免疫耐受功能的DC细胞亚群——稳态成熟cDC2(homeostatically matured cDC2,简称DC2hm)。这一发现提出了外周免疫耐受维持的新理论,为理解自身免疫疾病的发生机制和开发治疗策略开辟了新方向。

一、新亚群的发现与定义:DC2hm
研究团队利用高分辨率的质谱流式技术,对健康成人的脾脏组织进行分析,意外发现了一群此前未被识别的DC细胞。这群细胞高表达多种与DC活化、成熟及迁移相关的分子(如CD80、CD40、LAMP3、CCR7),但值得注意的是,它们不仅存在于健康成人脾脏,在无菌环境下的胎儿脾脏中也同样存在,并表达cDC2谱系的特征性表面蛋白(CD1c、CLEC10A)。这表明,它们的成熟过程不依赖于外界微生物刺激,而是机体预设的稳态程序。因此,研究者将其命名为稳态成熟cDC2(DC2hm)。
通过整合单细胞ATAC-seq、RNA-seq及CITE-seq等多组学技术,研究团队进一步解析了DC2hm独特的染色质开放性图谱、转录谱及表面蛋白表达谱,从分子层面确立了其区别于传统cDC的独特身份。
二、特征性标志与独特属性:IL-7Rα与CCR7
为了能够精准识别和研究DC2hm,研究者对其表面蛋白谱进行了深度剖析。他们发现,DC2hm除高表达趋化因子受体CCR7外,还特异性高表达IL-7受体α链(IL-7Rα)及其下游信号分子STAT5。这一特征至关重要,因为经典的由病原体刺激产生的免疫原性成熟cDC虽然也高表达CCR7,但IL-7Rα水平极低。
这一差异使得IL-7Rα和CCR7双阳性成为区分DC2hm与其他成熟DC的关键表面标志,并成功建立了从人脾脏中高效分选DC2hm的方法。
三、形态与功能的转变:从“哨兵”到“管家”
DC2hm展现出与传统cDC截然不同的形态与功能特征:
形态学:DC2hm的细胞核呈规则的椭圆形(而非cDC典型的多形核),细胞表面的树突状突起也明显减少。
功能学:DC2hm的吞噬能力下降,接受病原体刺激后炎症因子的分泌水平也显著降低。
这些特征共同表明,DC2hm并非传统意义上的免疫“哨兵”,其生理功能不在于快速感应和传递病原警报,而可能另有他用。
四、核心功能:外周免疫耐受的“执行者”
为探究DC2hm的真实功能,研究者将其与初始CD4⁺ T细胞共培养。结果令人惊喜:在没有任何外源刺激的条件下,DC2hm便能高效诱导初始CD4⁺ T细胞分化为具有免疫抑制功能的调节性T细胞(Treg)。而经典的免疫原性DC则主要诱导产生效应Th1细胞。多重免疫组化染色进一步显示,DC2hm定位于脾脏白髓的T细胞区,并与Treg细胞高度共定位,暗示其在体内微环境中可能也发挥着诱导Treg的功能。
更深入的转录组比较发现,DC2hm与负责中枢耐受的胸腺髓质上皮细胞(mTEC)高度相似。它们不仅高表达驱动组织特异性抗原(TRA)表达的转录因子AIRE,还异位表达了来源于大脑、肝脏、胰岛等外周组织的多种自身抗原。这一关键发现提出了一个全新理论:DC2hm可能通过在外周淋巴器官中呈递这些组织特异性自身抗原,将遇到的自身反应性T细胞转化为Treg细胞,从而在机体最核心处“管家”式地维持外周免疫耐受,预防自身免疫病的发生。
五、分化调控机制:TSLP驱动的稳态成熟
既然DC2hm的分化不依赖微生物刺激,其背后的驱动因素是什么?鉴于DC2hm高表达TSLP(胸腺基质淋巴细胞生成素)受体的亚基IL-7Rα和TSLPR,研究者将目光投向了细胞因子TSLP。
体外实验证实,用TSLP刺激新鲜分离的cDC2,可以使其获得与DC2hm几乎一致的转录组特征和表面蛋白谱,并赋予其诱导Treg的能力。在免疫系统人源化小鼠模型中,TSLP处理同样能显著扩增脾脏中的人源DC2hm细胞,并伴随Treg比例上升。这证实TSLP是驱动人体cDC2向DC2hm稳态成熟的关键细胞因子,从而在体内外建立了从TSLP信号到DC2hm分化,再到Treg生成的完整调控轴线。
六、总结与展望
本研究首次发现并命名了人体稳态成熟DC细胞亚群DC2hm,系统阐明了其“TSLP驱动 → 获得mTEC样特征(表达AIRE和TRA)→ 诱导Treg生成 → 维持外周耐受”的全新功能范式。
这一发现不仅颠覆了人们对稳态下DC细胞功能的传统认知,将外周免疫耐受的执行者从传统的基质细胞拓展到了DC细胞,也为自身免疫病、过敏、器官移植排斥等的治疗提供了极具潜力的新靶点。未来,通过调控DC2hm或其分化通路,或许能开辟一条重塑免疫平衡、治疗相关疾病的全新路径。
乐备实多款现货Panel支持DC细胞研究,欢迎咨询~
| 乐备实官网货号 | 中文名称 | 技术平台 | 检测指标 |
| LXLBH10-1 | 人炎症10因子Panel | Luminex | IL-1 β/IL-1F2,IL-2,IL-4,IL-6 ,IL-8/CXCL8,IL-10,IL-12 p70,IL-13,TNF-α,IFN-γ |
| LXLBM10-1 | 小鼠炎症10因子Panel | Luminex | IL-1 β/IL-1F2,IL-2,IL-4,IL-5,IL-6 ,IL-10,IL-12p70,CXCL1/GRO/α/KC/CINC-1,IFN-γ,TNF-α |
| LXLBR10-1 | 大鼠炎症10因子Panel | Luminex | IL-1 β/IL-1F2,IL-2,IL-4,IL-5,IL-6 ,IL-10,IL-12p70,CXCL1/GRO/α/KC/CINC-1,IFN-γ,TNF-α |
| LXLBM23-1 | 小鼠细胞因子-23因子Panel | Luminex | Eotaxin/CCL11,G-CSF,GM-CSF,IFN-γ,IL-10,IL-12(p40),IL-12(p70),IL-13,IL-17A,IL-1α,IL-1β,IL-2,IL-3,IL-4,IL-5,IL-6,IL-9,GRO-α (Gro-a/KC/CXCL1),MCP-1/CCL2,MIP-1α/CCL3,MIP-1β,RANTES,TNF-α |
| LXLBR23-1 | 大鼠细胞因子-23因子Panel | Luminex | G-CSF,GM-CSF,GRO/KC,IFN-γ,IL-1α,IL-1β,IL-2,IL-4,IL-5,IL-6,IL-7,IL-10,IL-12 (p70),IL-13,IL-17A,IL-18,M-CSF,MCP-1,MIP-1α,MIP-3α,RANTES,TNF-α,VEGF |
| LXLBM31-1 | 小鼠趋化因子-31因子Panel | Luminex | BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin/CCL11,Eotaxin-2/CCL24,Fractalkine/CX3CL1,GM-CSF,I-309/CCL1,IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-10,IL-16,IP-10/CXCL10,I-TAC/CXCL11,KC/CXCL1,MCP-1/CCL2,MCP-3/CCL7,MCP-5/CCL12,MDC/CCL22,MIP-1α/CCL3,MIP-1β/CCL4,MIP-3α/CCL20,MIP-3β/CCL19,RANTES/CCL5,SCYB16/CXCL16,SDF-1α/CXCL12,TARC/CCL17,TNF-α |
| LXLBH40-1 | 人趋化因子/细胞因子-40因子Panel | Luminex | 6Ckine/CCL21,BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin/CCL11,Eotaxin-2/CCL24,Eotaxin-3/CCL26,Fractalkine/CX3CL1,GCP-2/CXCL6,GM-CSF,GRO-α (Gro-a/KC/CXCL1),Gro-β/CXCL2,I-309/CCL1,IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-8/CXCL8,IL-10,IL-16,IP-10/CXCL10,I-TAC/CXCL11,MCP-1/CCL2,MCP-2/CCL8,MCP-3/CCL7,MCP-4/CCL13,MDC/CCL22,MIF,MIG/CXCL9,MIP-1α/CCL3,MIP-1δ/CCL15,MIP-3α/CCL20,MIP-3β/CCL19,MPIF-1/CCL23,SCYB16/CXCL16,SDF-1α+β/CXCL12,TARC/CCL17,TECK/CCL25,TNF-α |












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


