摘要
二硫化物死亡作为一种新近发现的程序性细胞死亡通路,在肿瘤治疗领域展现出巨大潜力,但其肿瘤特异性诱导仍是当前面临的主要挑战。2026年2月24日,中国科学技术大学刘扬中团队与南京师范大学刘红科团队合作在《ACS Nano》上发表的一项研究,创新性地构建了一种基于铜触发生物正交反应的“肿瘤内点击化学工厂”系统。该系统通过肿瘤靶向递送铜配合物前药(Cu/rhein)与钌配合物前药(Ru–N₃),在肿瘤细胞内原位生成细胞毒性产物Ru-rhein。Ru-rhein通过下调葡萄糖转运蛋白1(GLUT1)诱导二硫化物死亡,同时释放的铜离子可协同触发铜死亡。体内外实验证实,该策略能高效且选择性地清除癌细胞,为肿瘤治疗提供了全新的双通路协同干预思路。

一、研究背景与科学问题
二硫化物死亡是一种由胞内二硫键异常积累驱动的调控性细胞死亡形式,其关键调控蛋白SLC7A11在多种肿瘤细胞中高表达,构成了肿瘤细胞的一个代谢脆弱点。在葡萄糖饥饿或NADPH耗竭状态下,高表达SLC7A11的肿瘤细胞由于胱氨酸还原受阻,导致二硫键在细胞骨架蛋白等处异常积累,最终引发细胞死亡。因此,选择性诱导肿瘤细胞发生二硫化物死亡成为一种前景广阔的治疗策略。然而,如何在肿瘤微环境中精准地启动这一死亡通路,同时避免对正常细胞的损伤,是转化的核心难题。生物正交化学,特别是铜催化的叠氮-炔烃环加成反应,为在活体内原位合成活性药物提供了可能,但其应用受限于如何确保两种反应组分在肿瘤部位的特异性富集与激活。
二、研究设计与核心策略
为解决上述问题,研究团队设计了一套精巧的“肿瘤内点击化学工厂”体系,其核心是两种经过特殊设计的低毒性前药及一种靶向递送系统。
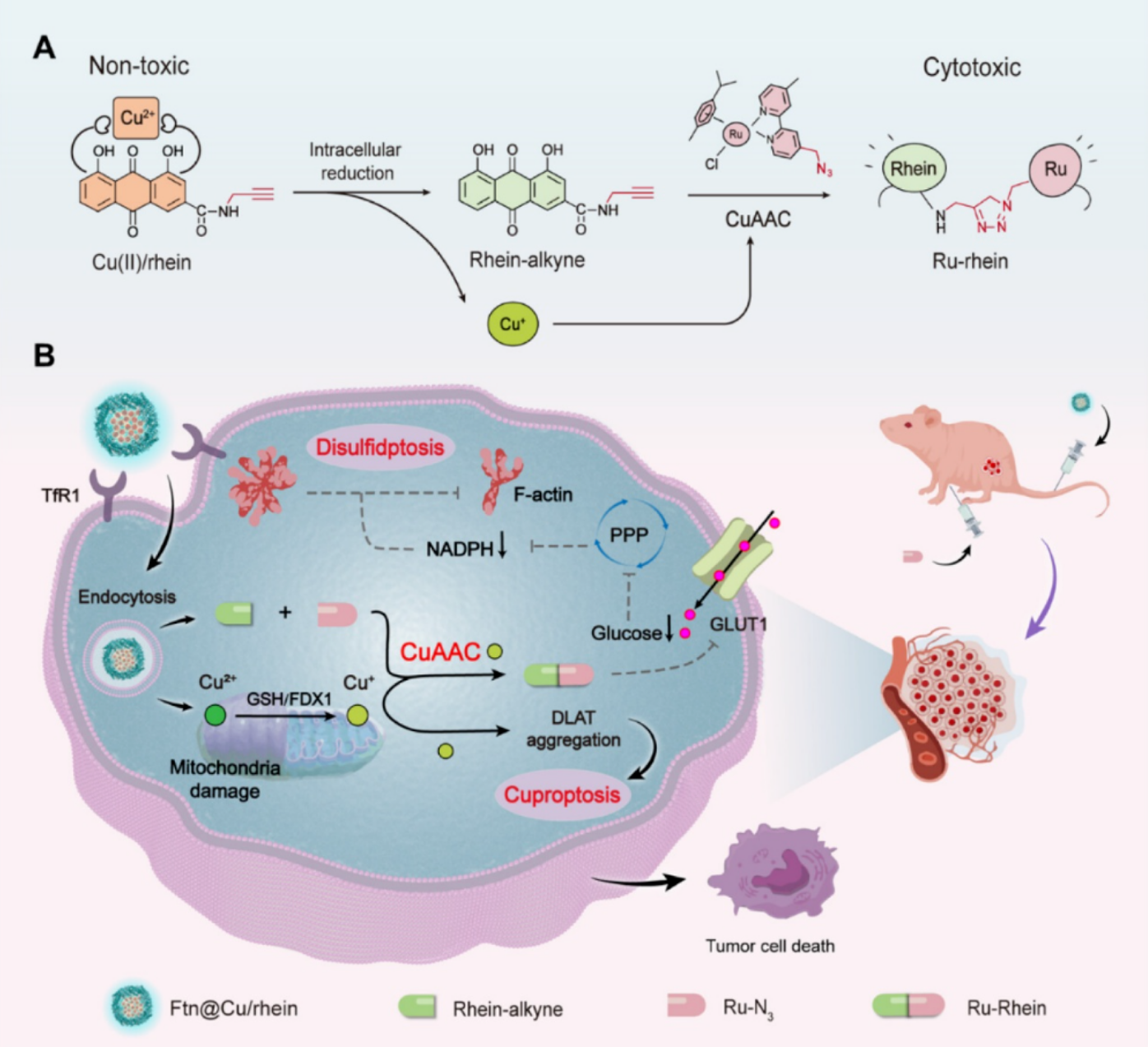
Ru-rhein和Cu/rhein的铜催化生物正交反应示意图
Yin Y, Yu W, et al. Tumor-Directed Disulfidptosis via Spatiotemporally Controlled Copper Bioorthogonal Activation. ACS Nano. 2026 Mar 10;20(9):7569-7588.
前药设计:两种前药分别为叠氮修饰的钌配合物(Ru–N₃)与炔烃修饰的大黄酸衍生物(大黄酸-炔烃)。二者单独存在时毒性较低。
催化剂递送:将作为催化剂的铜离子(Cu²⁺)与大黄酸-炔烃配位形成复合物(Cu/rhein),并将其封装在具有天然肿瘤靶向性的铁蛋白(Ftn)纳米笼中。这一设计确保了催化剂和其中一种前药能够共同被递送至肿瘤部位。
原位合成与激活:肿瘤靶向的铁蛋白纳米笼将Cu/rhein复合物特异性输送至肿瘤细胞内。在细胞内,Cu²⁺被还原为具有催化活性的Cu⁺,随即启动Cu⁺催化的叠氮-炔烃环加成反应,将同时存在于细胞内的Ru–N₃与大黄酸-炔烃连接,原位生成具有高细胞毒性的加合物Ru-rhein。
三、双重细胞死亡机制
该策略通过单一体系,协同触发了两种不同的程序性细胞死亡通路:
(一)二硫化物死亡的诱导
原位生成的Ru-rhein能够显著下调肿瘤细胞表面的葡萄糖转运蛋白1(GLUT1)表达。这导致细胞摄取葡萄糖的能力下降,胞内葡萄糖水平降低,进而严重抑制了磷酸戊糖途径,使还原型辅酶Ⅱ(NADPH)的再生受阻。NADPH的耗竭破坏了细胞对胱氨酸还原为半胱氨酸的过程,引发胞内二硫键的异常积累,最终特异性诱导高表达SLC7A11的肿瘤细胞发生二硫化物死亡。
(二)铜死亡的协同增强
递送入胞的Cu/rhein复合物在释放大黄酸-炔烃参与反应的同时,也导致了铜离子在细胞内的蓄积。这些铜离子能够直接靶向三羧酸循环中脂酰化的线粒体酶,引起其聚集和功能紊乱,从而独立地诱导肿瘤细胞发生铜死亡。这一过程不仅直接杀伤肿瘤,其引发的氧化还原失衡还可能进一步增强二硫化物死亡的效应。
三、体内外验证与结论
研究团队在细胞层面验证了上述机制,并在荷瘤小鼠模型中证实了该生物正交系统的体内治疗效果。结果显示,通过肿瘤靶向递送和原位生物正交激活,该策略能够有效抑制肿瘤生长,并展现出良好的生物安全性。该研究的创新性在于:
(一)策略创新
首次将生物正交化学与二硫化物死亡、铜死亡相结合,利用肿瘤内部的微环境触发药物合成与双重死亡通路激活。
(二)递送创新
利用铁蛋白纳米笼共递送铜催化剂和炔烃前体,解决了生物正交反应组分在体内难以同步富集于肿瘤的难题。
(三)机制协同
Ru-rhein诱导的二硫化物死亡与铜离子蓄积诱导的铜死亡相互独立又协同作用,增强了抗肿瘤效果并可能降低耐药性风险。
四、研究意义与展望
这项发表于《ACS Nano》的研究不仅为深入理解二硫化物死亡的调控机制提供了新的化学工具,更重要的是,它展示了一种通过“在需要的地方制造药物”的理念来克服传统治疗局限性的可行路径。通过在肿瘤内部时空可控地原位合成药物并协同诱导双重细胞死亡,该策略为开发下一代高选择性、高效低毒的肿瘤治疗方案奠定了坚实的科学基础。未来的研究可以进一步优化递送系统的靶向效率,并探索该平台与其他治疗方式(如免疫治疗)的联合应用潜力。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


