导语
传统观点认为,小分子药物主要通过被动扩散穿越细胞膜,其分子量通常需小于500道尔顿。这一“500道尔顿法则”极大地限制了可开发药物的分子范围。然而,近年来涌现的蛋白靶向降解嵌合体(PROTACs)等大分子药物(分子量常大于800道尔顿)却展现出出人意料的细胞通透性,其背后的机制长期未知。2025年4月17日,德克萨斯大学李宏宇、杜克大学林慧观、阿肯色州立大学秦志强等华人学者在《Cell》期刊在线发表的一项研究,首次揭开了这一谜团。该研究鉴定出跨膜蛋白CD36是介导多种PROTACs及大分子药物细胞内吞的关键受体,并提出了一种全新的“化学内吞药物(CEMC)”研发策略,有望革新传统药物研发范式。

一、研究背景:大分子药物渗透的未解之谜
PROTACs作为一种异双功能性分子,通过同时结合目标蛋白和E3泛素连接酶,诱导靶蛋白降解,为靶向“不可成药”蛋白提供了变革性机会。尽管其分子量大、结构复杂,但已有超过20种口服PROTACs进入临床试验。这提示,除了被动扩散,必然存在其他高效的细胞摄取机制。探索这一机制对于理解和开发大分子药物至关重要。
二、核心发现
(一)鉴定PROTACs的膜受体——CD36
为探究PROTACs进入细胞的途径,研究团队设计了一种三价生物素化化学探针(BRD-VHL-biotin)。通过质谱分析,他们在前列腺癌LNCaP细胞膜上捕获到与探针特异性结合最强的膜蛋白——分化簇36(CD36)。
进一步的验证实验证实了CD36与PROTAC的直接相互作用:
生物素pull-down实验:证实了PROTAC SIM1-Me能与CD36蛋白结合。
表面等离子共振(SPR)实验:定量显示SIM1-Me与纯化CD36蛋白具有高亲和力,甚至超过其天然配体棕榈酸。
这些结果强有力地表明,CD36是PROTAC分子进入细胞的一个重要且直接的膜靶点。
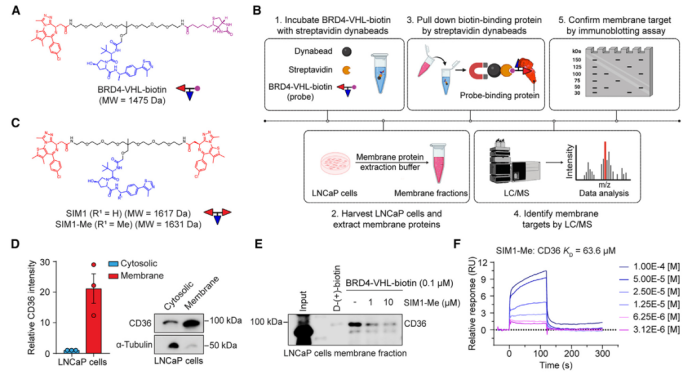
图1.CD36是PROTAC分子的一个重要膜靶点
(二)CD36通过EEA1/Rab5途径介导PROTAC内吞
研究团队进一步探究了CD36是否真正参与PROTAC的摄取过程。通过一系列细胞水平的功能获得与缺失实验,他们证实了CD36的关键作用:
功能缺失实验:在LNCaP细胞中敲低CD36表达后,PROTACs(如SIM1-Me和临床药物ARV-110)诱导的靶蛋白降解效果显著受抑制,细胞内药物浓度也明显下降。
功能获得实验:过表达CD36则增强了PROTACs的降解效果。
深入机制研究发现,这一过程依赖于经典的细胞内吞途径。敲低早期内体抗原1(EEA1) 或Rab5蛋白,同样能显著削弱PROTACs的细胞毒性,表明CD36介导的PROTACs摄取是通过EEA1/Rab5依赖的内吞作用实现的。
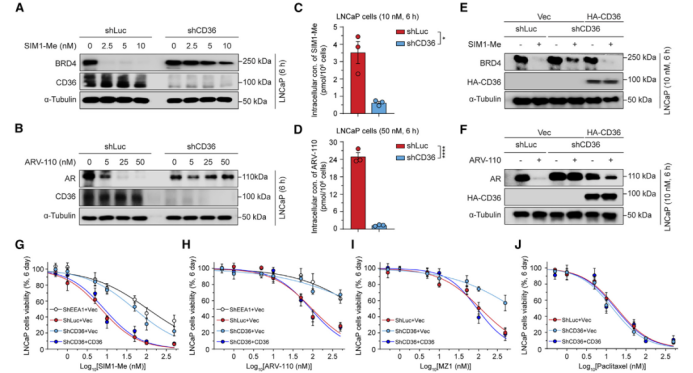
图2.PROTAC分子依赖CD36进入肿瘤细胞
(三)提出并验证“化学内吞药物(CEMC)”策略
基于CD36是PROTAC进入细胞的关键,研究团队开创性地提出了 “化学内吞药物(CEMC)”策略:通过化学修饰,增强药物分子与CD36的结合,从而提高其细胞摄取效率和药效。
(1)策略验证
以细胞通透性较差的PROTAC MZ1为模型,通过连接不同性质的片段,设计合成了一系列三价MZ1类似物。
结果显示,带有负电荷(如MZ1-C14-Na)或疏水性中性基团(如MZ1-C12-NB)的类似物,其CD36结合亲和力、BRD4降解活性以及细胞内摄取量均显著高于母体MZ1。
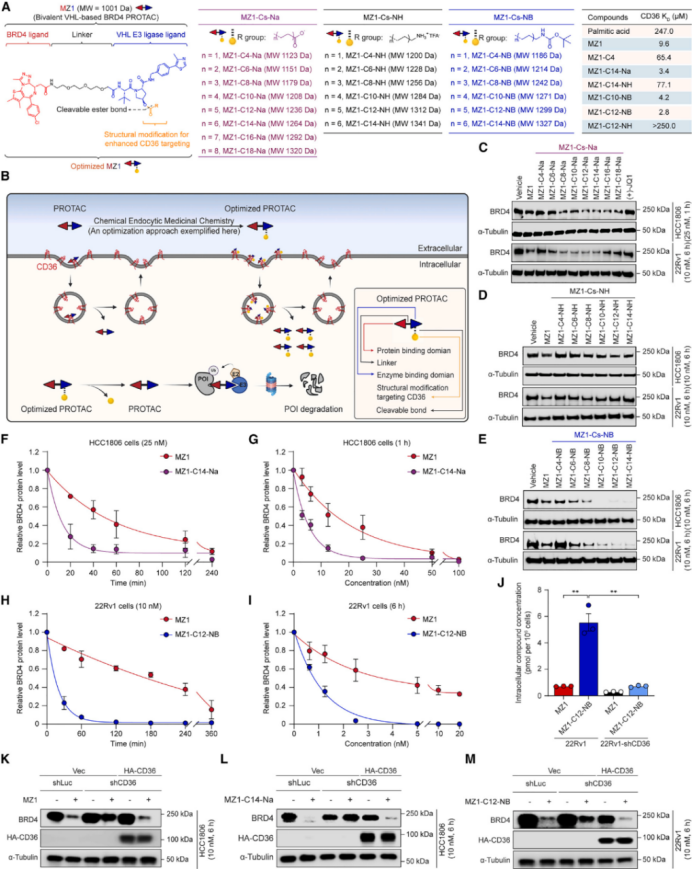
图3.CEMC策略增加PROTAC的细胞渗透性与靶蛋白降解活性
(2)普适性检验
该策略成功应用于其他PROTAC(如ARV-110)及多种大分子/强极性小分子药物(如雷帕霉素、navitoclax、阿霉素等)。
这些药物的摄取和毒性同样依赖CD36,且通过化学修饰增强与CD36的结合能提升其活性。这表明CD36介导的内吞可能是一个广泛的药物摄取机制。
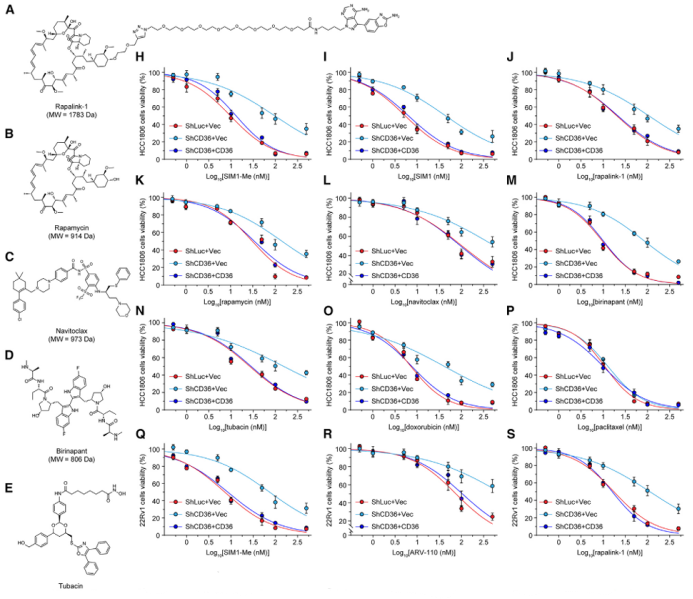
图4.CD36介导的内吞调节bRo5药物分子的吸收
(四)体内实验证实CEMC策略的抗肿瘤潜力
为验证该策略在体内的有效性,研究团队利用三阴性乳腺癌和前列腺癌细胞系构建了异种移植瘤小鼠模型。
分别用载体、母体PROTAC MZ1及优化后的类似物MZ1-C14-Na、MZ1-C12-NB处理荷瘤小鼠。
结果显示,与对照组和MZ1组相比,接受CEMC优化的MZ1类似物治疗的小鼠,其肿瘤生长受到更显著的抑制。
肿瘤组织的免疫组化分析也证实,优化后的类似物诱导了更强的BRD4蛋白降解。
这些动物实验为CD36介导内吞在PROTACs体内递送和药效发挥中的关键作用提供了有力证据,并直接证明了CEMC策略在提升抗肿瘤活性方面的巨大潜力。
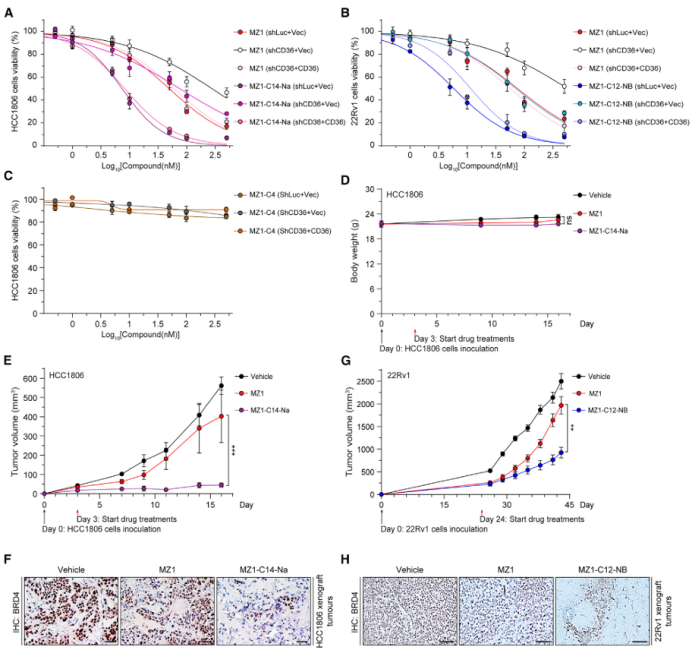
图5.CD36 的分子靶向增加 PROTAC 抗肿瘤活性
三、研究意义与展望
这项研究颠覆了“大分子难以跨膜”的传统认知,揭示了一个由CD36介导、EEA1/Rab5依赖的、广泛存在的药物内吞机制。它不仅解答了PROTACs如何进入细胞的长期疑问,更开辟了药物研发的新范式。
传统的药物开发专注于优化化合物的理化性质以实现被动扩散,需在渗透性、溶解度和稳定性间艰难平衡。而 “化学内吞药物(CEMC)”策略巧妙地利用细胞自身的膜受体介导内吞途径,为开发过去被认为“不可成药”或难以递送的大分子药物提供了全新思路。通过化学修饰增强药物与内吞受体(如CD36)的结合,有望在提升药效的同时,改善药物的整体药代动力学特性,为未来更多大分子药物(包括PROTACs)的成功开发铺平道路。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


