摘要
细胞迁移与侵袭是生物体内重要的生理和病理过程,尤其在肿瘤恶性进展中发挥关键作用。细胞迁移/侵袭实验是评估细胞运动能力的核心体外技术,为肿瘤学等领域的机制研究和干预效果评价提供重要实验依据。本文系统阐述细胞迁移与侵袭的生物学基础,详细介绍细胞划痕实验和Transwell小室检测两种主流实验方法的原理、操作流程、优缺点,并总结实验操作中的关键注意事项与优化策略,旨在为相关领域的科研工作提供标准化的实验参考。
一、细胞迁移与侵袭的生物学基础
细胞迁移是活细胞普遍存在的运动形式,指细胞接收迁移信号或感知物质浓度梯度后,通过头部伪足延伸、新黏附建立、细胞体尾部收缩的时空交替过程实现移动,是胚胎发育、血管生成、伤口愈合等正常生理过程的核心环节,同时也是肿瘤转移的关键步骤。转移性疾病是导致癌症患者死亡的主要原因,因此解析细胞迁移机制成为肿瘤研究的重要方向。
细胞侵袭是细胞迁移的特殊形式,与肿瘤的恶性浸润密切相关,指细胞在原位突破基底膜,通过分泌蛋白酶降解胞外基质(ECM)或基底膜基质层(BME),进而内渗进入血管、淋巴管并侵入新组织区域的过程。细胞侵袭不仅参与伤口修复、血管形成等生理过程,更在肿瘤细胞的远处转移中起决定性作用,其能力评估是肿瘤相关信号通路研究、靶向药物筛选的重要指标。
目前检测细胞迁移能力的主流方法为细胞划痕实验和Transwell小室检测,前者模拟单层细胞的2D平面迁移,后者可实现3D空间的迁移与侵袭能力检测,其中Transwell小室检测也是评估细胞侵袭能力的最常用手段。
二、细胞划痕实验
细胞划痕实验又称伤口愈合实验,是模拟体内细胞迁移的经典2D体外实验方法,因操作简便、成本低廉成为细胞迁移能力初筛的首选技术。
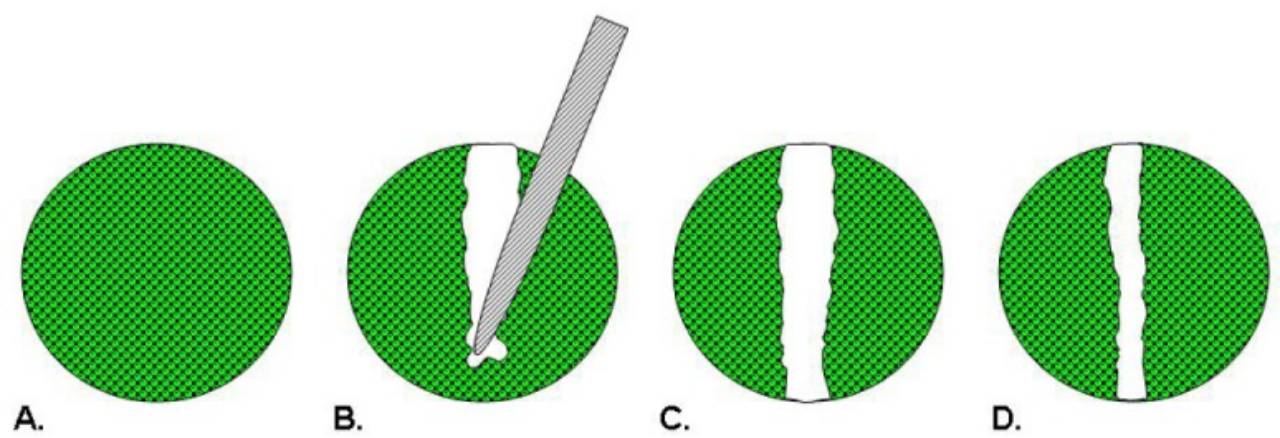
划痕实验示意图
Hulkower KI, Herber RL. Cell migration and invasion assays as tools for drug discovery. Pharmaceutics. 2011 Mar 11;3(1):107-24.
(一)实验原理
当培养的贴壁细胞融合成单层后,通过人工手段在细胞层制造无细胞的空白区域(划痕),划痕边缘的细胞会在趋化信号作用下逐渐向空白区域迁移,使划痕逐渐愈合,通过观察不同时间点划痕的愈合程度,可定量评估细胞的迁移能力。
(二)操作流程
实验全程遵循无菌操作原则,核心步骤为:
①培养板划线:在6孔板背面用马克笔绘制等距横线,作为后续观察的定位标记;
②铺板:将对数生长期的细胞接种至6孔板,培养至细胞融合度达90%以上;
③细胞划线:用无菌枪头沿培养板背面横线垂直划线,制造均匀划痕;
④清洗:用无血清培养基轻轻冲洗培养板2~3次,去除划落的细胞;
⑤细胞培养观察:加入无血清或低血清培养基,置于培养箱中培养,在设定时间点观察并拍照;
⑥结果分析:通过图像分析软件测量划痕宽度,计算划痕愈合率。
(三)实验要点
1. 培养板选择:常规实验优先选用6孔板,其定位线可提供10个固定监测点,减少实验误差;高通量初筛时可选用12孔板或24孔板。
2. 细胞接种:根据细胞贴壁率和生长速度调整接种浓度,保证实验终止时细胞密度适宜,避免过度增殖影响结果。
3. 培养基选择:采用无血清或血清浓度≤2%的培养基进行培养,降低细胞增殖对迁移实验的干扰。
(四)优缺点
优点:
①操作简便,无需特殊实验仪器;
②实验成本低,适合大批量样本的初筛;
③实验周期短,可快速获得结果。
缺点:
①手工划痕易出现宽度不均一,影响愈合度的准确评估;
②划线过程会对划痕周围细胞造成机械损伤,降低细胞活性;
③难以完全排除细胞增殖对实验结果的干扰,无法单独反映细胞的纯迁移能力。
三、Transwell小室检测
Transwell小室检测是基于微孔滤膜的细胞迁移与侵袭检测技术,可模拟细胞在体内3D微环境中的运动过程,既能检测细胞迁移能力,也是评估细胞侵袭能力的金标准,广泛应用于肿瘤学的深入研究。
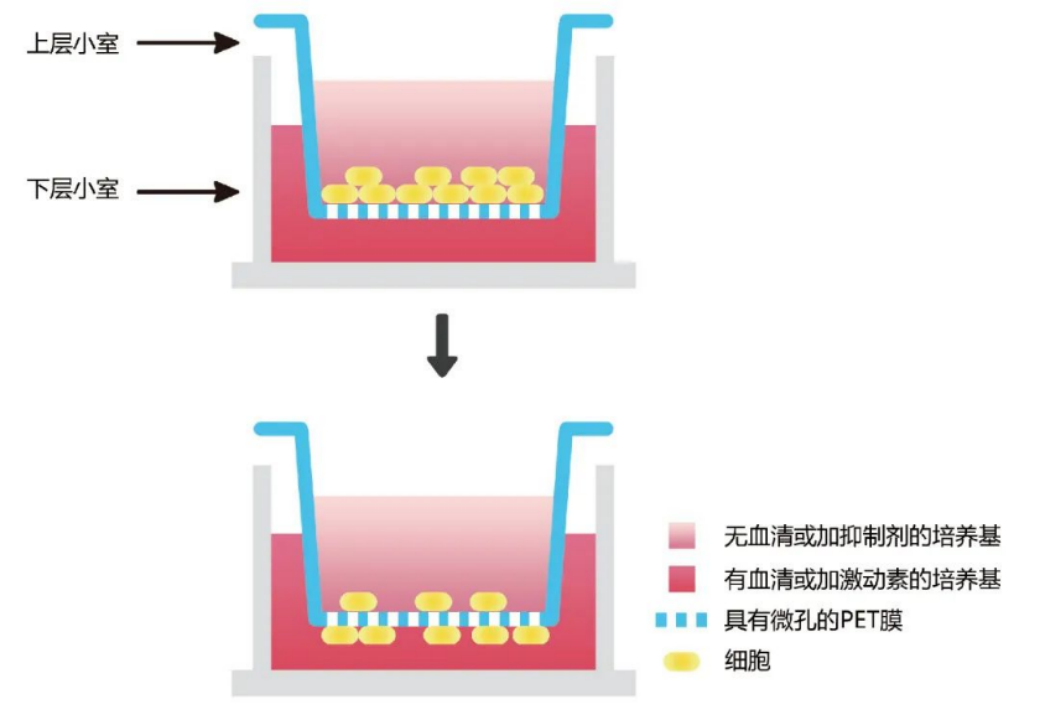
Transwell实验原理图
(一)实验原理
将Transwell小室放入培养板中,小室为上室,培养板孔为下室,上下室通过带有微孔的聚碳酸酯膜分隔。上室加入含待检测细胞的无血清培养基,下室加入含血清或趋化因子的完全培养基,利用营养梯度诱导细胞发生跨膜运动。通过对滤膜下表面的细胞进行染色计数,可定量判断细胞的迁移或侵袭能力;当检测侵袭能力时,需在滤膜上表面铺覆一层基质胶模拟体内ECM,细胞需先降解基质胶才能完成跨膜运动,更贴合体内肿瘤细胞的侵袭过程。
(二)实验分类及应用
根据滤膜孔径和处理方式的不同,Transwell小室检测可应用于多种研究场景,核心应用包括:
1. 共培养体系:选用孔径<3.0μm的滤膜,细胞无法穿膜,可将细胞A种于上室、细胞B种于下室,研究细胞B的分泌产物对细胞A的生物学影响。
2. 趋化性实验:选用适宜孔径的滤膜,通过计数下室细胞量,可分析细胞B分泌产物或外源性趋化因子对目标细胞的趋化作用。
3. 肿瘤细胞迁移实验:上室接种肿瘤细胞,下室加入胎牛血清(FBS)或特定趋化因子,通过跨膜细胞数反映肿瘤细胞的迁移能力。
4. 肿瘤细胞侵袭实验:在迁移实验的基础上,于上室滤膜表面铺覆Matrigel基质胶,细胞需分泌基质金属蛋白酶(MMPs)降解基质胶后才能跨膜,跨膜细胞数可反映肿瘤细胞的侵袭能力。
(三)操作流程
1. 细胞迁移实验流程
①细胞培养与处理:将目标细胞培养至对数生长期,根据实验设计进行药物处理、基因修饰等干预;
②Transwell小室准备:将小室放入24孔板中,无菌条件下平衡滤膜;
③制备细胞悬液:用无血清培养基重悬细胞,调整细胞浓度至适宜范围;
④接种细胞:将细胞悬液加入上室,下室加入完全培养基,置于培养箱培养;
⑤细胞固定:培养结束后,取出小室,用多聚甲醛固定滤膜上的细胞;
⑥细胞染色:用结晶紫等染料对固定后的细胞进行染色;
⑦封片与计数:擦去滤膜上表面未迁移的细胞,封片后在显微镜下观察并计数下表面的细胞数。
2. 细胞侵袭实验流程
与迁移实验相比,侵袭实验需增加包被基底膜和水化基底膜两个步骤:在细胞接种前,用Matrigel基质胶稀释液均匀包被滤膜上表面,置于培养箱中孵育形成凝胶层;随后用无血清培养基水化凝胶层,其余步骤与迁移实验一致。
(四)实验要点
1. 细胞状态:实验所用细胞需处于对数生长期,状态良好,避免细胞凋亡或衰老影响实验结果。
2. 气泡排除:放置小室时轻缓操作,避免滤膜下产生气泡,若出现气泡可轻拍底板侧面清除。
3. 细胞清理:固定后擦去滤膜上表面未迁移细胞时,需控制棉签力度,避免戳破滤膜或擦除下表面的跨膜细胞。 4. 细胞处理:对于穿膜能力较弱的细胞,可提前进行饥饿处理,增强细胞的趋化运动能力。
四、实验操作的通用注意事项与优化策略
细胞迁移与侵袭实验的结果易受操作细节影响,为保证实验的重复性和准确性,需遵循以下通用注意事项,并采用相应的优化策略:
1. 实验器具消毒:直尺、马克笔、枪头等实验器具使用前需经紫外照射消毒,避免微生物污染。
2. 细胞铺板标准化:根据细胞生长速度调整接种数量,保证每组细胞铺板密度一致且铺匀,减少组间误差。
3. 划痕操作优化:划线前保留原培养基,避免划落的细胞团块堆积在划痕边缘;用枪头划线时用力均匀、垂直稳定,保证划痕宽度一致;亦可使用culture Insert模具替代手工划痕,获得无细胞损伤的笔直划痕。
4. 定位观察与拍照:利用培养板定位线的交叉点作为固定监测点,0h拍照时标记位置,后续在相同位置观察拍照;拍照时避免露出马克笔线条,保证镜头清晰,切换镜头时及时更换标尺,便于后续图像分析。
5. 细胞增殖干扰排除:除使用无血清/低血清培养基外,可采用1μg/ml丝裂霉素处理细胞1h,抑制细胞分裂;需注意丝裂霉素可能会降低细胞迁移速度,实验中需设置对照。
6. 观察时间点选择:常规观察时间点为0、2、4、6、8、12、24h,不建议超过24h,避免细胞过度增殖造成实验假阳性。
7. 结果分析优化:采用长度法分析划痕实验结果时,由于细胞迁移并非齐头并进,需测量多条距离并取平均值,提高结果的准确性;Transwell实验需在显微镜下随机选取多个视野计数,取平均值作为最终结果。
五、实验应用与展望
细胞迁移与侵袭实验作为体外评估细胞运动能力的核心技术,已广泛应用于肿瘤学、细胞生物学、药理学等多个领域,尤其在肿瘤研究中,可用于评估基因修饰(过表达、敲低、敲除、点突变)、药物处理等干预手段对肿瘤细胞恶性表型的影响,为肿瘤靶向药物的筛选和作用机制研究提供重要实验数据。 随着实验技术的不断发展,细胞迁移与侵袭实验也在向标准化、精准化方向升级,如自动化划痕仪的应用解决了手工划痕的不均一问题,3D培养体系的结合使实验更贴近体内生理微环境。未来,结合单细胞测序、活细胞成像等技术,将进一步解析细胞迁移与侵袭的分子机制,为肿瘤转移的临床干预提供更精准的实验依据。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


