摘要
胃癌(Gastric Cancer, GC)具有高度的时空异质性,表现为肿瘤内部不同区域、原发与转移灶之间以及疾病进展过程中的动态演变。这种异质性严重干扰了关键生物标志物的准确检测,是导致靶向治疗和免疫治疗耐药的重要原因。本文系统综述了胃癌中包括HER2、PD-L1、MSI/MMR、EBV、CLDN18.2及FGFR2b在内的预测性生物标志物的异质性特征,分析了其对诊断准确性及临床治疗决策的影响。现有证据表明,克服肿瘤异质性对于提升胃癌精准治疗水平至关重要,未来亟需深化异质性机制研究、推进检测标准化并探索动态监测手段。
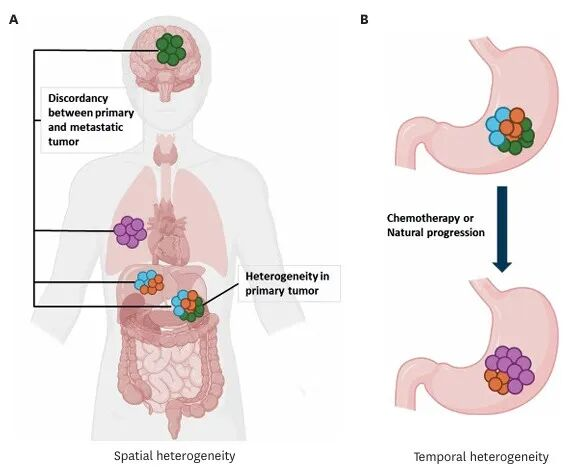
胃癌的时间和空间异质性示意图;A)空间异质性;B)时间异质性
一、引言
胃癌是全球发病率及死亡率均位居前列的恶性肿瘤,其治疗已步入分子分型指导下的精准医疗时代。人表皮生长因子受体2(HER2)、程序性死亡配体1(PD-L1)、微卫星不稳定性(MSI)等生物标志物的状态,直接决定了抗HER2靶向治疗、免疫检查点抑制剂等方案的适用性。然而,胃癌不仅是分子水平上的异质性疾病,更展现出显著的时空异质性。空间异质性指同一肿瘤不同区域(瘤内)以及原发灶与转移灶之间的分子特征差异;时间异质性则指在疾病自然进展或治疗压力(如化疗、靶向治疗)下,肿瘤的分子特征发生动态演变。这种异质性使得基于单次、单点的小型活检样本的检测结果,可能无法全面反映肿瘤的整体或实时特征,从而导致治疗决策偏差和耐药发生。2025年发表于 Journal of Gastric Cancer 的一篇题为“Spatial and Temporal Tumor Heterogeneity in Gastric Cancer: Discordance of Predictive Biomarkers”的综述
对此进行了深度阐述,本文基于该综述及相关研究,对胃癌关键预测性生物标志物的异质性及其临床意义进行系统梳理。

二、主要生物标志物的时空异质性
(一)HER2异质性
HER2是胃癌中研究最深入、异质性证据最确切的靶点。其异质性在不同层面均有体现:
肿瘤内异质性:HER2阳性在肿瘤内部并非均匀分布,同一标本中可同时存在HER2阳性和阴性区域。研究表明,HER2异质性的检出率介于33.3%至74.0%之间,且在免疫组化(IHC)2+的病例中异质性比例(70.5%)显著高于IHC 3+病例(42.9%)。
活检与手术标本的不一致:由于异质性,基于少量内镜活检标本的检测结果与后续手术切除标本的金标准结果存在不一致,不一致率报道为12.3%-27.8%。为确保检测准确性,权威指南推荐获取至少5块(理想为6-8块)活检组织。
原发灶与转移灶的不一致:原发肿瘤与配对转移淋巴结或远处转移灶之间的HER2状态也存在差异,不一致率为1%-14%。当聚焦于IHC 2+/3+或HER2扩增的病例时,这一比例可升至38.9%-62.9%,提示肿瘤在转移过程中可能发生克隆选择或演化。
时间异质性与获得性耐药:在抗HER2治疗(如曲妥珠单抗)的压力下,部分肿瘤会出现HER2表达的丢失,总体丢失率为29.2%-60.6%。初始IHC 2+的患者丢失风险更高。这种表达改变是获得性耐药的重要机制,并影响后续治疗选择(如对T-DM1的敏感性)。
HER2异质性具有明确的临床意义,表现为异质性肿瘤患者对曲妥珠单抗的治疗反应率更低,无进展生存期和总生存期更短。新型抗体药物偶联物(如T-DXd)因其“旁观者效应”,可能对HER2异质性肿瘤更具优势。
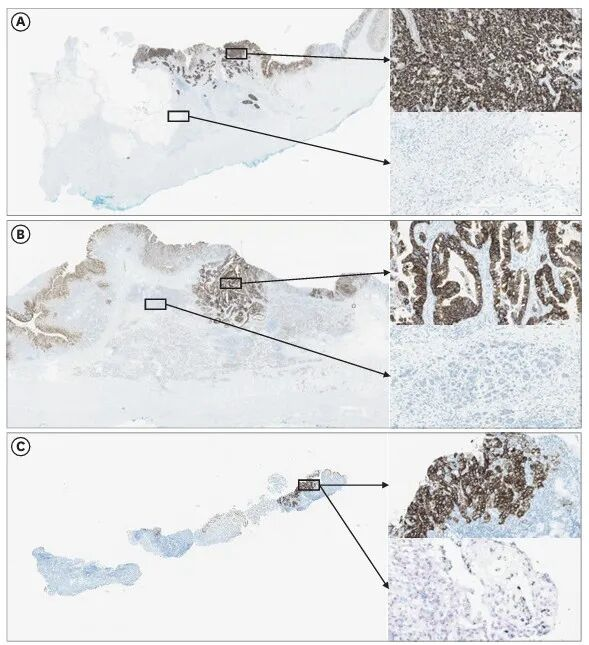
肿瘤内HER2异质性示意图。
A)一例HER2阳性病例:低分化腺癌区域呈3+评分,而低黏附性癌及黏液腺癌区域呈阴性;
(B) 一例HER2阳性病例:低级别组织学区域呈3+评分,高级别区域呈阴性;
(C)四块活检组织中仅一块显示HER2阳性,图示片段观察到HER2基因扩增现象。
(二)PD-L1异质性
PD-L1表达同样呈现显著的时空异质性。手术切除标本的PD-L1阳性率(47.3%)显著高于活检标本(32.1%),提示活检存在假阴性的风险。空间上,原发灶与转移灶之间的表达水平存在差异,有研究显示淋巴结转移灶的表达水平可能更高。时间上,化疗后可观察到PD-L1表达的动态变化,治疗前后样本的一致性约为50%-74.7%。因此,为确保免疫治疗决策的准确性,同样需要足够的活检样本(推荐4-5块),并建议在疾病进展时对转移或新发病灶进行重新检测。
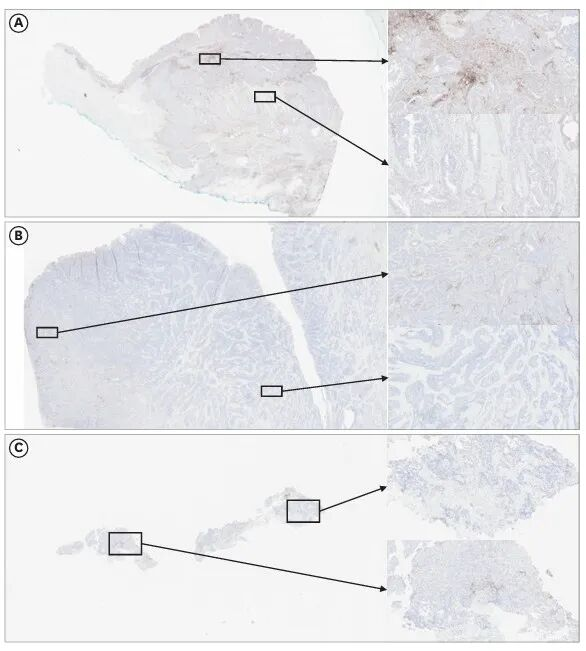
胃癌中观察到肿瘤内PD-L1异质性,A)PD-L1联合阳性评分(CPS)≥10区域;B和C)1≤CPS <5区域。
(三)MSI/MMR异质性
微卫星不稳定性(MSI)和错配修复(MMR)状态在胃癌中的瘤内异质性总体少见(<1%),但在MSI-H(高度不稳定性)病例中,异质性发生率可达8.9%。这种罕见的异质性可能导致对免疫治疗的反应不一。原发灶与转移灶之间的MSI/MMR状态也存在低发生率的不一致性,但因其直接关联免疫治疗疗效,不容忽视。
(四)其他新兴标志物的异质性
EBV:EBV编码RNA(EBER)原位杂交检测显示,典型EBV相关胃癌表现为弥漫性核阳性,状态高度一致。但少数异质性EBV阳性病例(在EBV阳性胃癌中占1.9%-18.2%)的存在,提示可能存在EBV感染丢失或混合克隆等机制。
CLDN18.2:CLDN18.2在胃癌中的表达高度异质,阳性率报道范围宽泛(14%-88%)。约23.8%-46.5%的胃癌病例呈阳性,其中31.0%-38.5%存在瘤内异质性表达。原发灶阳性率通常高于转移灶,且不同转移部位(如腹膜、肝)阳性率存在差异。
FGFR2b:FGFR2b过表达同样存在显著的瘤内异质性(阳性病例中达55.5%)和原发-转移灶不一致性(44.4%)。临床转化研究表明,仅具有高水平克隆性FGFR2扩增的肿瘤才能从FGFR抑制剂治疗中持续获益,而存在亚克隆异质性扩增的患者疗效不佳。
三、讨论与展望
本文系统综述了胃癌关键预测性生物标志物的时空异质性特征。从HER2到PD-L1,再到CLDN18.2、FGFR2b等新兴靶点,异质性是一个普遍存在的现象。这种异质性不仅是导致诊断偏差(如基于小活检的假阴性)的根源,更是靶向治疗和免疫治疗原发性或获得性耐药的核心机制之一。例如,HER2异质性直接关联曲妥珠单抗疗效不佳,而罕见的MSI/MMR异质性也可能导致免疫治疗耐药。
面对这一挑战,未来研究和临床实践需在以下方向重点突破:
1. 深化机制研究:阐明不同生物标志物时空异质性发生的分子基础,如克隆演化路径、肿瘤微环境的选择压力、治疗诱导的适应性改变等,为克服异质性提供理论靶点。
2. 推进检测标准化与优化:建立并统一各生物标志物的检测标准,包括明确的阳性判读标准、推荐的样本类型(如活检与手术标本的适用场景)及最低样本量要求。开发和验证能够捕捉瘤内异质性的检测技术,如多重免疫组化、数字病理和空间转录组学。
3. 探索动态监测手段:发展基于液体活检(如循环肿瘤DNA、循环肿瘤细胞)的微创或非侵入性动态监测技术,以实时追踪肿瘤的时空演变,及时发现生物标志物状态的改变,为治疗方案的动态调整提供依据。
总之,认识和克服胃癌的时空异质性,是实现从“静态”的分子分型到“动态”的精准治疗管理转变的关键,有望最终提升胃癌患者的个体化治疗水平和总体预后。
LabEx多款现货Panel支持胃癌标志物研究,欢迎咨询~
| 乐备实官网货号 | 中文名称 | 技术平台 | 检测指标 |
| LXMH10-1 | 人炎症10因子Panel | MSD | IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-8,IL-10,IL-12p70,IL-13,TNF-α |
| LXLBH10-1 | 人炎症10因子Panel | Luminex | IL-1 β/IL-1F2,IL-2,IL-4,IL-6 ,IL-8/CXCL8,IL-10,IL-12 p70,IL-13,TNF-α,IFN-γ |
| LXMM10-1 | 小鼠炎症10因子Panel | MSD | IFN-γ,IL-1β,IL-2,IL-4,IL-5,IL-6,IL-10,IL-12p70,KC/GRO,TNF-α |
| LXLBM10-1 | 小鼠炎症10因子Panel | Luminex | IL-1 β/IL-1F2,IL-2,IL-4,IL-5,IL-6 ,IL-10,IL-12p70,CXCL1/GRO/α/KC/CINC-1,IFN-γ,TNF-α |
| LXLBR10-1 | 大鼠炎症10因子Panel | Luminex | IL-1 β/IL-1F2,IL-2,IL-4,IL-5,IL-6 ,IL-10,IL-12p70,CXCL1/GRO/α/KC/CINC-1,IFN-γ,TNF-α |
| LXLBM23-1 | 小鼠细胞因子-23因子Panel | Luminex | Eotaxin/CCL11,G-CSF,GM-CSF,IFN-γ,IL-10,IL-12(p40),IL-12(p70),IL-13,IL-17A,IL-1α,IL-1β,IL-2,IL-3,IL-4,IL-5,IL-6,IL-9,GRO-α (Gro-a/KC/CXCL1),MCP-1/CCL2,MIP-1α/CCL3,MIP-1β,RANTES,TNF-α |
| LXLBR23-1 | 大鼠细胞因子-23因子Panel | Luminex | G-CSF,GM-CSF,GRO/KC,IFN-γ,IL-1α,IL-1β,IL-2,IL-4,IL-5,IL-6,IL-7,IL-10,IL-12 (p70),IL-13,IL-17A,IL-18,M-CSF,MCP-1,MIP-1α,MIP-3α,RANTES,TNF-α,VEGF |
| LXLBM31-1 | 小鼠趋化因子-31因子Panel | Luminex | BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin/CCL11,Eotaxin-2/CCL24,Fractalkine/CX3CL1,GM-CSF,I-309/CCL1,IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-10,IL-16,IP-10/CXCL10,I-TAC/CXCL11,KC/CXCL1,MCP-1/CCL2,MCP-3/CCL7,MCP-5/CCL12,MDC/CCL22,MIP-1α/CCL3,MIP-1β/CCL4,MIP-3α/CCL20,MIP-3β/CCL19,RANTES/CCL5,SCYB16/CXCL16,SDF-1α/CXCL12,TARC/CCL17,TNF-α |
| LXLBH37-1 | 人炎症37因子Panel | Luminex | APRIL/TNFSF13,BAFF/TNFSF13B,sCD30/TNFRSF8,sCD163,Chitinase 3-like 1,gp130/sIL-6Rβ,IFN-α2,IFN-β,IFN-γ,IL-2,sIL-6Rα,IL-8/CXCL8,IL-10,IL-11,IL-12(p40),IL-12(p70),IL-19,IL-20,IL-22,IL-26,IL-27(p28),IL-28A/IFN-λ2,IL-29/IFN-λ1,IL-32,IL-34,IL-35,LIGHT/TNFSF14,MMP-1,MMP-2,MMP-3,Osteocalcin,Osteopontin,Pentraxin-3,TNF-R1,TNF-R2,TSLP,TWEAK/TNFSF12 |












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


