衰弱(Frailty)作为全球日益严峻的公共卫生挑战,以多系统生理功能衰退、应激易感性增强为特征,已引发全球医疗保健体系的巨大负担。尽管历经数十年研究,当前仍缺乏普适的衰弱评估工具。现有方法如衰弱表型、衰弱指数等,多依赖问卷、功能测试或临床数据,需专业设备与人员,且存在验证一致性差、可扩展性受限、动态追踪困难等临床应用缺陷。更关键的是,衰弱的分子机制尚未明确,制约了老龄化背景下的精准干预策略开发。
2026年3月,浙江大学医学院团队联合复旦大学人工智能创新与产业研究院,在《Cell》子刊《Cell Metabolism》发表突破性研究。该研究基于英国生物样本库(UK Biobank)50,506名参与者的2911种血浆蛋白组学数据,首创“蛋白质组衰弱评分(PFS)”,并揭示衰弱相关蛋白质组失调的独特双峰模式——峰值分别出现在约50岁和63岁,对应代谢失调与免疫衰退两大关键阶段。
研究开发的PFS工具对13类疾病中的199种新发疾病(如心血管疾病、糖尿病并发症)展现出强预测能力,同时可响应84种可改变风险因素(如吸烟、饮食、运动)。通过差异表达-滑动窗口分析,研究证实50岁峰值关联代谢通路失调,提示代谢失调发展关键期;63岁峰值则指向免疫相关通路衰退,标志代谢衰弱向免疫炎症性衰弱的机制转变。这一发现首次将PFS确立为生物学衰老的新型标志物,并为衰弱干预锁定了关键时间窗口与分子靶标,为人口老龄化背景下的预防方案制定与针对性干预措施提供了科学依据。
本研究首次确立“蛋白质组衰弱评分(PFS)”可作为反映生物学衰老进程的新型标志物,为衰弱干预策略锁定了50岁与63岁两大关键时间窗口及精准分子靶标。

蛋白质组学为系统性探究健康状态蛋白质谱提供了独特视角,但现有衰弱相关蛋白质组研究多受限于小样本量(数百至数千例)或狭窄的蛋白覆盖范围,且观察性设计易受残余混杂因素和反向因果关系干扰,难以区分因果蛋白与伴随标志物。本研究通过扩展蛋白质组关联研究(PWAS)至英国生物样本库(UK Biobank)50,506名参与者的大规模队列,并结合孟德尔随机化(MR)等因果推断方法,突破了上述局限。
研究团队首先通过衰弱指数模拟衰弱状态,系统表征了衰弱相关的蛋白质组学特征及深层生物学机制。基于2911种血浆蛋白的大规模关联分析,鉴定出1339种与衰弱显著相关的蛋白质,其中胶原蛋白富集的细胞外基质和囊泡腔通路尤为突出。在独立队列TwinGene研究中,部分蛋白及通路关联得到复现验证。通过MR分析进一步锁定5种潜在因果蛋白:OXT、CPXM2与衰弱正相关,PYY、TPK1、IL6ST则呈负相关,为机制研究提供了直接靶点。
PFS工具不仅对13类疾病中的655种新发疾病(如心血管疾病、糖尿病并发症)展现出强预测性能,还可响应6大类99种可改变风险因素(如吸烟、饮食、运动)。通过稳定精简蛋白集构建的简约模型,其预测能力与完整模型相当,显著增强了临床转化潜力。团队开发的在线PFS计算工具进一步推动了该工具的实时应用。
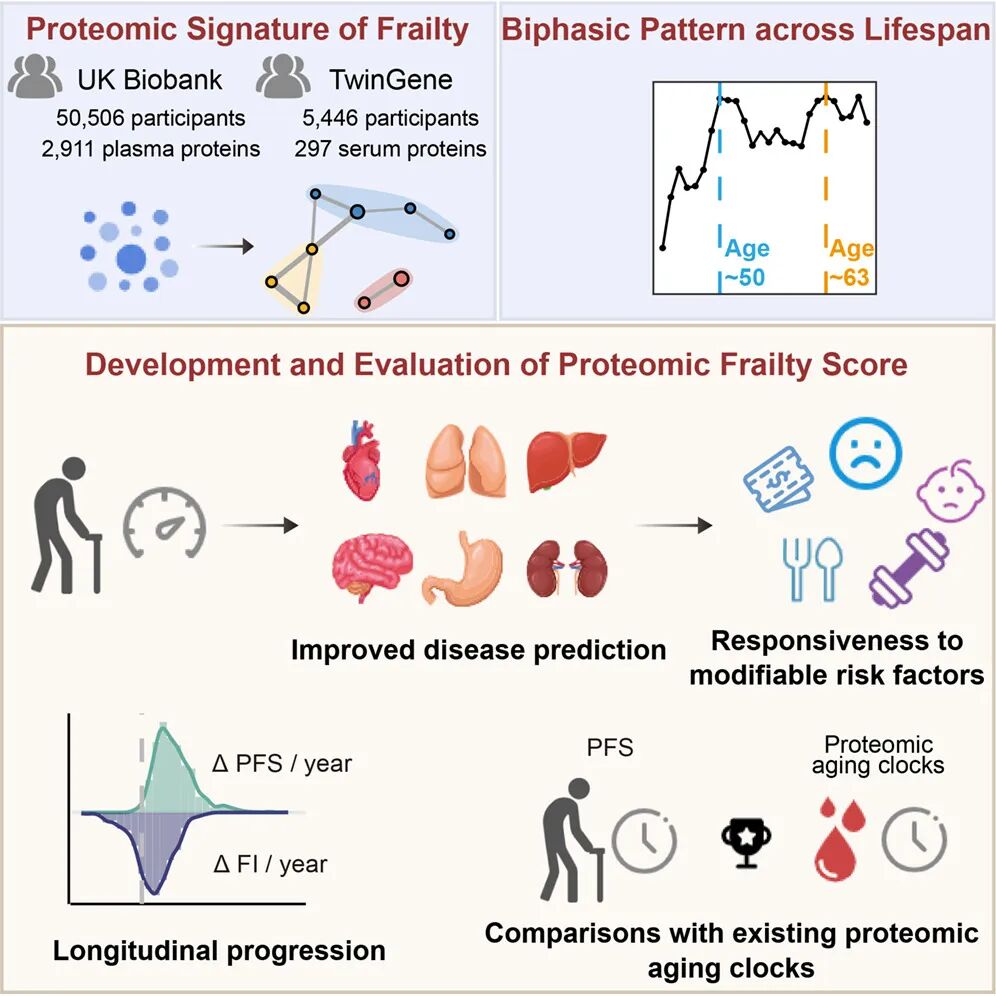
最终,通过差异表达-滑动窗口分析(DE-SWAN),研究揭示了衰弱相关蛋白质组在生命周期中的双峰分布模式:50岁峰值关联代谢通路失调,提示代谢失调发展的关键阶段;63岁峰值则指向免疫相关通路衰退,标志代谢衰弱向免疫炎症性衰弱的机制转变。这一动态变化模式的阐明,为及时采取预防措施及实施机制针对性干预提供了科学依据,填补了衰老过程中衰弱特异性血浆蛋白质组动态变化的知识空白。
本研究开发的“蛋白质组衰弱评分(PFS)”在疾病预测与风险响应方面展现出显著优势:其可对13个疾病分类中的199种新发疾病(涵盖心血管疾病、糖尿病并发症等)实现强预测,同时对84种可改变风险因素(如吸烟、饮食、运动等)具有广泛响应性。纵向追踪数据显示,随着年龄增长及基线衰弱程度的加深,PFS的进展速度呈加速趋势,这一动态特征为衰弱的早期预警与进展监测提供了量化工具。
本研究首次将PFS确立为反映生物学衰老进程的新型标志物,其意义不仅在于量化衰弱状态,更在于锁定了50岁与63岁两大关键时间窗口及对应的分子靶标(如代谢通路关键蛋白与免疫调节因子)。这一发现为衰弱的精准干预提供了科学依据——在50岁前通过生活方式干预(如饮食调整、规律运动)延缓代谢失调进展,在60岁后聚焦免疫调节与抗炎策略,从而实现全生命周期的衰弱预防与靶向治疗。PFS的提出,标志着衰弱研究从现象描述迈向机制解析与精准干预的新阶段。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


