在全球范围内,超重与肥胖的患病率呈快速攀升趋势,该流行病学现象显著升高了2型糖尿病(T2D)、心血管疾病及恶性肿瘤等多种严重疾病的发病风险。长期以来,肥胖的临床治疗手段相对有限,主要集中于饮食干预、运动调控等生活方式的规范化调整,其临床获益往往受个体依从性等因素限制,疗效存在明显局限。
胰高血糖素样肽-1(GLP-1)受体激动剂的临床应用,为超重与肥胖的临床管理带来了突破性变革。然而,在临床实践中,即使采用相同剂量的GLP-1类药物,不同个体的减重应答存在显著异质性:部分患者可获得显著减重效果,部分患者应答不佳,另有部分患者因难以耐受恶心、呕吐等药物不良反应而被迫终止治疗,这极大地限制了该类药物的临床应用价值。
2026年4月,国际顶刊《Nature》发表了一篇题为“Genetic predictors of GLP1 receptor agonist weight loss and side effects”(GLP-1受体激动剂减重效果及副作用的遗传预测因子)的研究论文,首次从全基因组层面系统揭示了影响GLP-1类药物疗效及不良反应的遗传机制,为该类药物的精准应用提供了重要理论依据。

该研究纳入近2.8万名接受GLP-1类药物(含司美格鲁肽与替尔泊肽)治疗的受试者,通过全基因组关联分析技术,首次明确识别出可直接预测药物减重效果及副作用风险的遗传因子。
临床数据显示,接受GLP-1受体激动剂治疗的患者,其体重减轻幅度存在显著个体差异。以司美格鲁肽疗效研究为例,受试者平均减重幅度为10.2%,其中4.9%的受试者减重比例超过25%,而32.2%的受试者减重比例不足5%,部分受试者甚至出现体重升高的情况。同时,受试者在药物相关副作用的发生情况上也存在明显异质性。因此,明确可预测个体对GLP-1类药物应答的相关因素,对指导临床治疗策略的制定具有重要临床意义,包括药物种类的选择、初始剂量的设定及剂量递增速率的优化等。
为深入阐明GLP-1类药物减重效果及副作用异质性的遗传学基础,研究团队针对27885名接受GLP-1受体激动剂治疗的受试者,开展了基于自述体重减轻情况及治疗相关副作用的全基因组关联研究(GWAS),为后续遗传预测因子的筛选提供了坚实的研究基础。
该研究中,所有受试者启动GLP-1类药物治疗前的体重指数(BMI)中位数为35.1 kg/m²,其中96.8%的受试者基线BMI≥25 kg/m²,符合超重及肥胖的诊断标准。受试者使用GLP-1类药物的中位治疗时长为8.3个月,治疗后受试者报告的BMI中位数下降4.1 kg/m²(对应体重减轻11.3 kg),等效体重减轻比例为11.7%。尽管替尔泊肽与司美格鲁肽的中位治疗时长相近(分别为8.1个月和8.4个月),但接受替尔泊肽治疗的受试者BMI下降幅度更为显著,分别为4.75 kg/m²和3.71 kg/m²,提示不同GLP-1类药物的减重效能存在差异。
核心发现一:与减重疗效相关的基因变异
研究团队在GLP1R基因(即司美格鲁肽等GLP-1类药物的作用靶点编码基因)上,精准定位到一个关键错义变异(rs10305420),该变异可显著调控GLP-1类药物的减重疗效,其作用特征如下:
(1)携带效应:携带该变异效应等位基因“T”的受试者,接受GLP-1类药物治疗后,平均额外减重0.76 kg,提示该等位基因可增强药物减重效能;
(2)累加效应:该基因变异的作用模式呈“加性效应”,即受试者若从父母双方均遗传获得该“增效”等位基因,其额外减重幅度可达到1.5 kg,体现出剂量依赖性的增效特征;
(3)跨人群一致性:该基因变异在欧洲人群中频率较高(约40%),但在拉丁裔、非洲裔等其他人群中,其增强GLP-1类药物疗效的趋势保持一致,提示该变异的预测价值具有跨人群适用性。
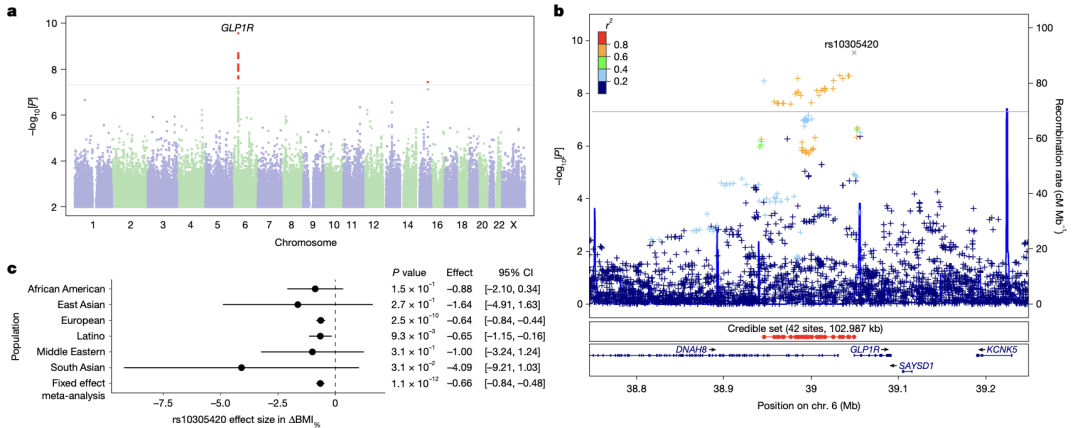
综上,个体的GLP1R基因型可在一定程度上预先决定其对GLP-1类药物的减重应答强度,为临床疗效的初步预测提供了重要遗传标志物。
核心发现二:与副作用风险相关的基因变异
除减重疗效外,研究团队还进一步锁定了与GLP-1类药物副作用相关的遗传根源,具体发现如下:
(1)GLP1R基因区域变异与恶心呕吐风险相关:GLP1R基因区域的相关变异与GLP-1类药物治疗后恶心、呕吐的发生风险存在广泛关联,提示药物作用靶点基因的变异可能直接影响不良反应的发生;
(2)GIPR基因变异与替尔泊肽呕吐风险显著相关:在接受替尔泊肽(GLP-1受体与GIP受体双重激动剂)治疗的人群中,GIPR基因的特定错义变异(rs1800437)与呕吐发生风险显著相关,携带该变异风险等位基因“C”的受试者,呕吐发生概率显著升高;
(3)双重风险等位基因叠加效应:若受试者同时在GLP1R和GIPR两个基因位点均携带风险等位基因,其接受替尔泊肽治疗后呕吐的发生风险较普通人群升高约14.8倍,明确了多基因变异叠加对不良反应风险的放大作用。
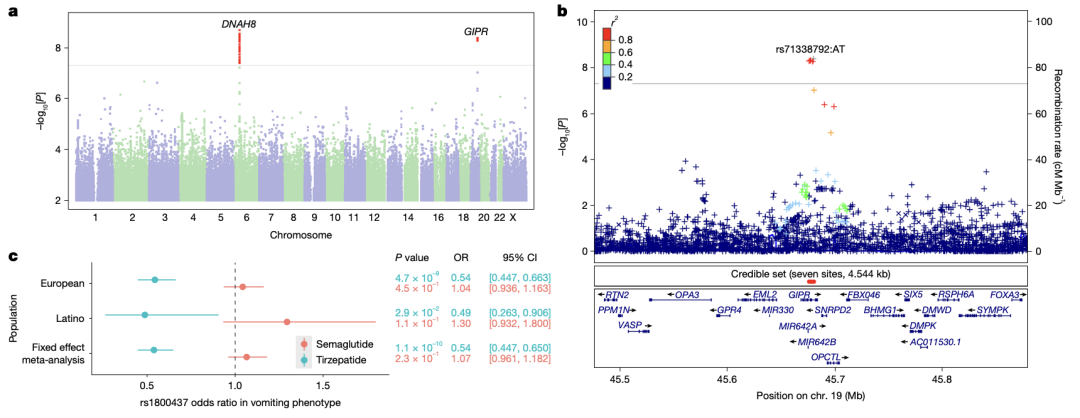
该发现清晰阐释了GLP-1类药物(单靶点与双靶点)治疗中,不同个体副作用表现存在显著差异的遗传学机制,为不良反应的精准预测提供了重要支撑。
总体而言,本研究通过大规模全基因组关联研究,系统揭示了GLP-1类药物治疗应答的遗传调控机制:编码司美格鲁肽、替尔泊肽作用靶点的GLP1R基因存在特定错义变异,与更优的减重疗效相关;同时,GLP1R及GIPR基因相关变异与GLP-1类药物所致恶心、呕吐等不良反应密切相关。该研究提示,未来在GLP-1类药物临床应用前,可通过简易基因检测评估受试者的潜在疗效及副作用风险,进而精准选择药物种类、优化初始剂量及剂量递增速度,真正实现安全、有效的“个性化减重治疗”。
深入探究GLP-1类药物治疗应答的遗传学基础具有重要临床价值。鉴于GLP-1类药物在减重疗效与副作用方面存在显著个体异质性,且二者可能存在内在关联(如恶心症状更明显的受试者可能获得更优减重效果),筛选可靠的治疗应答预测指标,可从治疗初始阶段精准预测个体治疗进程,为临床构建表型与基因型相结合的预测模型、推进精准医疗落地奠定坚实基础。
值得关注的是,《Nature》期刊同期发表题为“Genetics reveal why people respond differently to GLP - 1 weight - loss drugs”(遗传学揭示人们对GLP-1类减重药物应答存在差异的原因)的观点文章,高度评价本研究的学术价值,指出该研究从遗传学层面阐明了GLP-1类药物应答异质性的核心机制,GLP1R及GIPR基因变异为理解药物应答差异、识别不良反应高风险人群提供了重要理论视角。

肥胖、糖尿病等代谢疾病相关生物标志物因子检测服务哪里有?
LabEx为您提供专业、全面的肥胖、糖尿病等代谢疾病相关生物标志物因子检测服务。基于多重液相芯片(Luminex)、超敏电化学发光(MSD)及高灵敏度ELISA等先进平台,我们能够系统性地定量评估糖尿病发生、发展及并发症相关的多维度生物标志物谱,涵盖糖脂代谢指标(胰岛素、C肽、胰高血糖素、GLP-1)、炎症因子(IL-6、TNF-α、CRP)、脂肪因子(脂联素、瘦素)、氧化应激标志物及血管损伤相关因子等。
| 货号 | Panel名称 | 种属 | 检测指标 |
| LXLBH10-3 | 人代谢-10因子Panel检测服务 | Human | C-Peptide,Ghrelin,GIP,GLP-1,Glucagon,Insulin,Leptin,PAI-1,Resistin,Visfatin |
| LXRMH07-7 | 人代谢-7因子Panel1试剂盒 | Human | C-Peptide,GIP (total),GLP-1 (total),Glucagon,Insulin,Leptin,PYY (total) |
| LXRMH10-9 | 人代谢相关-10因子Panel 2试剂盒 | Human | BDNF,β-NGF,IL-1β,IL-6,IL-8,IL-10,Insulin,Leptin,MCP-1,TNF-α |
| LXRMH10-8 | 人代谢相关-10因子Panel 1试剂盒 | Human | Adiponectin,ApoA1,ApoC3,Clusterin,CRP,DPPIV,NGAL/LCN2,RBP4,SHBG,sTfR-1 |












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


