一、方法概述
GST pull-down技术是一种在体外条件下研究蛋白质间相互作用的常用实验方法。该技术首先将体外表达的谷胱甘肽S-转移酶(GST)融合蛋白固定在谷胱甘肽琼脂糖珠上。随后,将固定有GST融合蛋白的琼脂糖珠与细胞裂解液共同孵育,使裂解液中与GST融合蛋白相互作用的靶蛋白被特异性捕获。通过充分洗涤,去除未结合的杂蛋白后,采用洗脱液将结合于珠上的蛋白复合物解离下来,从而获得GST pull-down产物。
在检测与分析方面,利用空间蛋白互作(PLA)技术可对捕获的蛋白复合物进行原位验证,以明确已知蛋白之间的直接或间接相互作用;而结合质谱分析则能够鉴定与已知蛋白相互作用的未知蛋白。由于该方法操作简便、灵敏度高,已被广泛认可为验证酵母双杂交系统筛选结果的可靠体外验证手段。近年来,伴随蛋白质组学研究的不断深入,GST pull-down技术在该领域的应用日益受到重视。
二、技术原理
Pull-down技术的核心在于将目标蛋白质预先固定于某种固相基质(如琼脂糖凝胶)上。当细胞提取液流经该固相基质时,与固相化蛋白发生相互作用的配体蛋白可被特异性吸附,而未发生相互作用的蛋白则随洗脱液被冲洗去除。随后,通过改变洗脱液的组成或洗脱条件,可将被吸附的目标蛋白复合物回收。该技术能够识别并验证已知蛋白与被捕获蛋白或纯化相关蛋白之间的相互作用关系,亦可从体外转录或翻译系统中检测蛋白间的互作。
为提高Pull-down技术的效能,可将待纯化的蛋白以融合蛋白形式进行表达,即将“诱饵”蛋白与一种易于纯化的配体蛋白进行融合。谷胱甘肽-S-转移酶(GST)作为一种常用的融合标签,其融合蛋白可通过GST与谷胱甘肽之间的特异性相互作用,被吸附于固定有谷胱甘肽的色谱介质上。当细胞提取液流经该色谱柱时,即可捕获与“诱饵”蛋白相互作用的靶蛋白。
GST pull-down技术,即GST融合蛋白沉降法,其基本原理如下:利用谷胱甘肽亲和树脂将靶蛋白-GST融合蛋白亲和固化,使其作为与目的蛋白相互作用的固相支撑物,发挥“诱饵蛋白”的功能。当含有目标蛋白的溶液通过该亲和柱时,可有效捕获与之相互作用的“捕获蛋白”(即目标蛋白)。随后,通过SDS-PAGE电泳对洗脱后的结合物进行分析,即可验证两种蛋白之间的相互作用,或筛选相应的目标蛋白。无论是“诱饵蛋白”还是“捕获蛋白”,均可来源于细胞裂解物、纯化蛋白、重组表达系统以及体外转录翻译系统等多种制备方式。
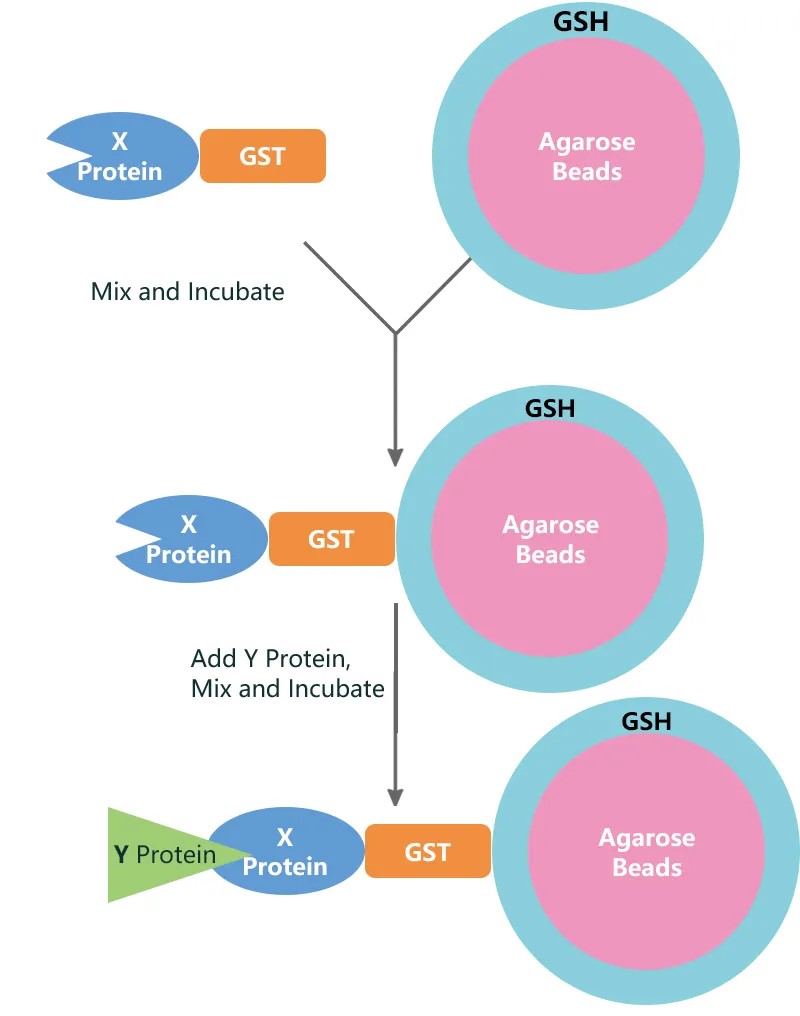
图1. GST pull-down实验原理示意图‘
’
三、实验流程
在GST pull-down实验中,抗体与抗原的结合方式可根据实验目的进行调整。一种方式是将抗体预先结合到蛋白A/G琼脂糖珠上,再与抗原混合。该方法尽管最终得率相对较低,但可避免抗体与目的蛋白共洗脱的问题。另一种方式则是先将抗体与蛋白样品混合,再加入蛋白A/G琼脂糖珠。该方法有助于获得高纯度的目的蛋白,但非特异性结合可能增加,且抗体与目的蛋白会同时被洗脱,可能对后续的蛋白质印迹检测产生干扰。整体实验流程主要包含以下三个步骤。
步骤一:制备GST融合蛋白
克隆目标蛋白质的亲和结合区域基因片段至GST融合表达载体中;将重组载体转化入大肠杆菌;在含有相应抗生素的LB培养基中过夜培养;收集菌体,通过超声破碎等方法裂解细胞,获得GST融合蛋白。
步骤二:制备细胞裂解液
选用适宜的细胞裂解缓冲液(如PBS缓冲液);在裂解缓冲液中加入蛋白酶抑制剂和磷酸酶抑制剂,以维持蛋白质的完整性。
步骤三:GST pull-down实验
将制备好的GST融合蛋白固定于亲和介质(如GST琼脂糖亲和树脂)上;将细胞裂解液与固定有GST融合蛋白的亲和介质共同孵育,使目标蛋白与GST融合蛋白发生特异性结合;通过洗涤步骤去除非特异性结合的蛋白质;使用洗脱缓冲液将结合的目标蛋白复合物洗脱下来;收集洗脱液,用于后续的蛋白质分析,如SDS-PAGE及质谱分析。
实验流程图:

四、常见问题及解决方法
1、IP、Co-IP与pull-down的区别
免疫沉淀(IP)和免疫共沉淀(Co-IP)通常以组织或细胞为实验材料,靶蛋白为内源性天然蛋白或在组织细胞中过表达的蛋白(可携带融合标签)。而pull-down实验中的诱饵蛋白一般通过重组表达获得。IP和Co-IP实验需要使用亲和力较高的一抗,选购时需关注相应的验证数据。
简而言之,IP用于捕获目的蛋白;Co-IP用于捕获目的蛋白及其相互作用蛋白;pull-down则利用融合标签的重组蛋白来捕获与之相互作用的蛋白。
2、如何区分蛋白表达于上清还是包涵体
蛋白可能以可溶形式表达于上清中,也可能以不溶形式表达于包涵体中。超声破碎菌体后,若菌液较为清亮、沉淀较少,表明表达的蛋白基本为可溶状态;若超声后菌液浑浊、离心后沉淀较多且沉淀颜色偏白,则蛋白主要表达于包涵体中。
3、蛋白表达于包涵体中是否可进行后续GST pull-down实验
包涵体是由翻译后的蛋白未能正确折叠而聚集形成的不溶聚集体。可使用高浓度尿素或盐酸胍使其变性、解聚,之后可尝试进行后续的pull-down实验。
4、GST融合蛋白表达量较低
应检查目标蛋白质的亲和结合区域基因片段是否正确克隆至表达载体中;优化大肠杆菌的培养条件,如温度、培养时间及培养基成分;亦可考虑采用其他表达系统,如哺乳动物细胞表达系统。
5、GST pull-down实验后目标蛋白质纯度较低
可通过增加洗涤步骤的次数,以去除非特异性结合的蛋白质;优化洗涤缓冲液的组成,如调整缓冲液浓度及pH值;也可考虑使用其他亲和介质材料,如Ni-NTA亲和树脂。
五、空间蛋白互作(PLA)技术哪里有?
LabEx为您提供前沿、精准的空间蛋白互作(PLA,邻位连接技术)检测服务。该技术能够在组织切片或细胞爬片上,以单分子分辨率实现对两种目标蛋白在空间位置上是否存在直接相互作用或共定位进行可视化检测与定量分析。PLA技术基于特异性抗体偶联的寡核苷酸探针,只有当两种目标蛋白在空间距离小于40nm时才会产生可检测的荧光信号,从而提供蛋白相互作用的原位证据。我们的服务涵盖从方案设计、探针选择与验证、样本制备(组织切片、细胞爬片)、PLA反应、荧光成像到信号计数与统计学分析的全流程。
| 货号 | Panel名称 |
| LX-PLA | PLA可视化蛋白互作服务 |
| LXR-PLA | PLA可视化蛋白互作试剂盒 |












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


