一、JAK/STAT 通路的发现与生物学地位
细胞因子作为一类由免疫原、有丝分裂原等刺激诱导产生的低分子量可溶性蛋白(8-30 KDa),通过细胞表面特异性受体调控细胞增殖、分化、免疫应答等多种生物学功能。在细胞因子激活的信号转导网络中,Janus 激酶 - 信号转导和转录激活因子(JAK-STAT)通路是研究最深入、作用最广泛的核心通路之一,被视为细胞功能调控的 “中心通信节点”。
JAK/STAT 通路的发现源于对干扰素(IFN)抗病毒机制的探索。1957 年干扰素被发现后,研究者逐步揭示出其通过诱导特定基因表达发挥抗病毒作用的分子基础,而 JAK/STAT 通路正是这一信号传递过程的关键介导者。随着研究深入,该通路被证实广泛参与细胞与组织发育、代谢调节、感染应答、炎症反应及肿瘤发生等生理病理过程,成为连接细胞外信号与细胞核基因表达的重要桥梁。美国国立卫生研究院(NIH)John J. O’Shea 教授团队在《Cell》发表的综述中,系统阐述了该通路在疾病中的作用及药物研发进展,凸显了其在基础研究与临床转化中的重要地位。

二、JAK/STAT 通路的核心组成与分子结构
2.1 JAK 激酶家族的结构特征
JAK(Janus 激酶)作为通路的核心激酶,属于非受体蛋白酪氨酸激酶家族,包含 JAK1、JAK2、JAK3 和酪氨酸激酶 2(TYK2)四个成员。其独特之处在于拥有两个高度相似的磷酸转移酶结构域:一个具备激酶活性,负责底物磷酸化;另一个则通过构象调控发挥自身活性调节功能。由于全长 JAK 蛋白结构复杂且稳定性差,长期以来其三维结构解析面临挑战,直至近年才获得 JAK1 与细胞因子受体胞内结构域结合的全长复合物结构,为理解其激活机制提供了关键结构生物学依据,这一突破也推动了JAK1 - 细胞因子受体复合物三维结构解析领域的研究深化。

2.2 STAT 家族的功能多样性
信号转导和转录激活蛋白(STATs)是一类兼具信号传递与转录调控双重功能的蛋白家族,在静息细胞中主要定位于细胞质。目前已鉴定出 7 个家族成员,包括 STAT1、STAT2、STAT3、STAT4、STAT5a、STAT5b 和 STAT6,分别由不同基因编码。作为 JAK 的关键底物,STAT 蛋白通过保守酪氨酸残基的磷酸化实现功能激活,其作用类似 “分子开关”,精准调控下游信号传递。
STAT 蛋白通过 SH2 结构域介导的相互作用形成同源或异源二聚体,其中 STAT1、STAT3 和 STAT5a 可形成平行或反平行构象的同源二聚体,而 STAT 四聚体则通过 N 端结构域的相互作用进一步增强 DNA 结合能力。值得注意的是,在 I 型和 III 型干扰素应答中,STAT1 与 STAT2 形成异源二聚体,再与 IRF9 结合形成 ISGF3 复合物,这一特殊组合是干扰素诱导基因表达的核心调控单元,体现了 STAT 家族功能的多样性。
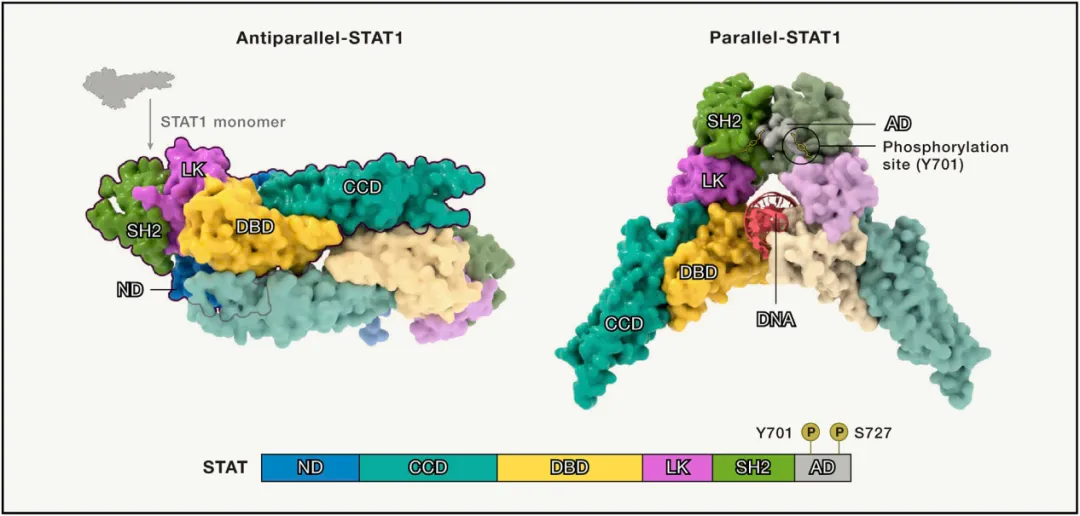
三、JAK/STAT 通路的激活机制与信号传递
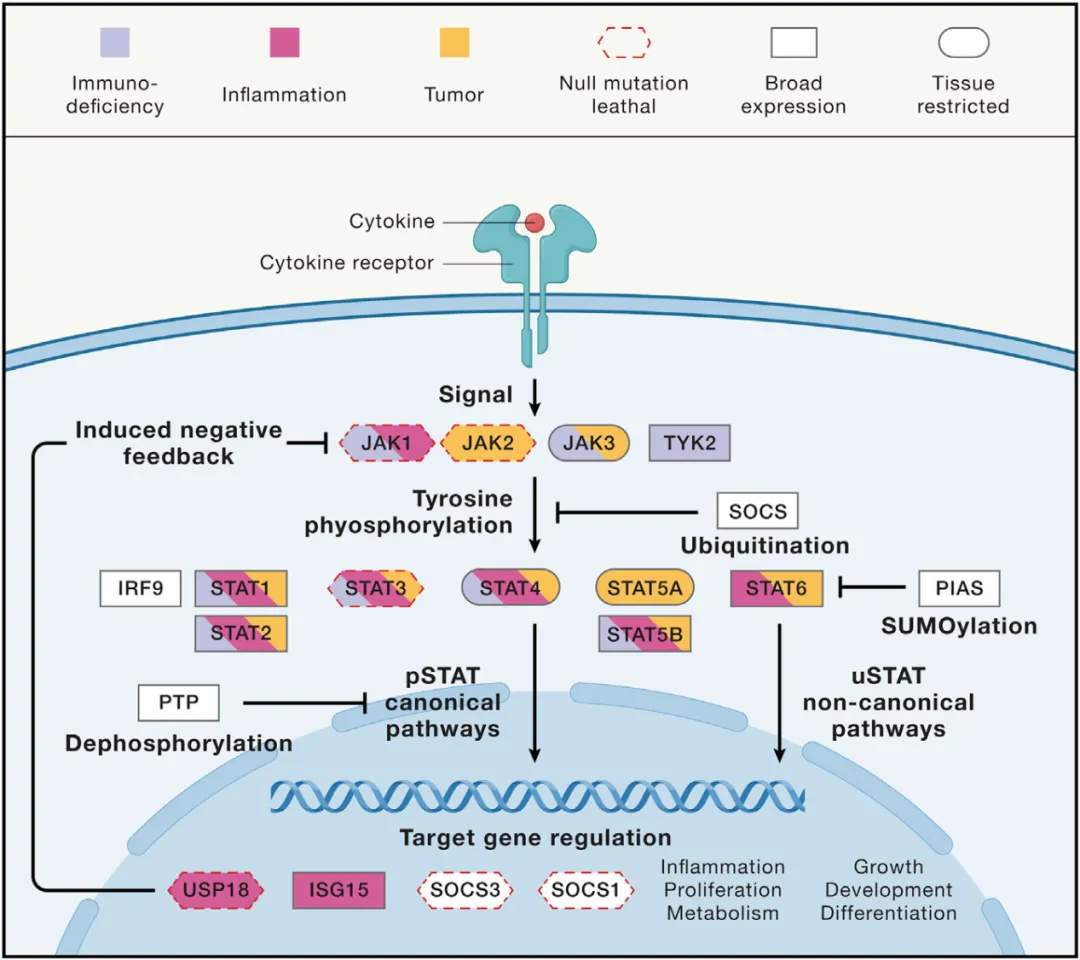
JAK/STAT 通路的激活始于细胞因子与受体的特异性结合。目前已知近 60 种细胞因子,包括白细胞介素(ILs)、集落刺激因子(CSF)、激素样细胞因子及生长因子等,均以 JAK/STAT 通路作为主要信号转导方式。细胞因子与受体结合后,引发受体构象变化,使胞内结构域相关的 JAK 激酶相互靠近并发生自身磷酸化激活,随后通过磷酸化修饰激活 STAT 蛋白。
通路激活存在两种主要模式:在典型途径中,磷酸化的 STAT(pSTAT)形成二聚体,通过核孔复合体转运至细胞核,与靶基因启动子或增强子区域的特定 DNA 序列结合,直接调控基因转录;在非典型途径中,未磷酸化的 STAT(uSTAT)也可形成二聚体进入细胞核发挥转录调控作用。其中,干扰素诱导 ISGF3 复合物激活 JAK/STAT 通路机制是典型途径中极具代表性的分支,其通过 STAT1-STAT2-IRF9 的特异性组装,精准介导干扰素相关的基因表达调控。此外,STAT 蛋白还可通过与表观遗传修饰因子、共激活因子及 RNA 聚合酶 II 的相互作用,参与增强子簇(super enhancer)介导的基因表达调控,在全基因组范围内对表观遗传过程产生广泛影响。
四、JAK/STAT 通路的负调控网络
为维持信号稳态,JAK/STAT 通路受到精密的负调控,主要涉及三类关键蛋白:蛋白酪氨酸磷酸酶(PTPs)、细胞因子信号传导抑制因子(SOCS)家族和活化 STATs 的蛋白抑制剂(PIAS)。
PTPs 通过去磷酸化作用终止信号,其中 SHP-1 是典型代表,其两个 SH2 结构域可特异性结合磷酸化的 JAK 或受体,通过催化去磷酸化抑制信号传递。SOCS 家族则通过三种机制发挥作用:一是通过 SH2 结构域与 JAK 结合直接抑制其激酶活性;二是通过 SOCS 框与延伸蛋白 B/C 及 cullin5 形成复合物,介导 JAK 的泛素化降解;三是竞争性结合受体磷酸酪氨酸位点,阻止 STAT 募集,这些多维度作用共同构成了SOCS 家族介导 JAK/STAT 通路负调控机制的核心内容。PIAS 家族则通过与活化的 STAT 二聚体结合,阻断其与 DNA 的相互作用,从而抑制转录激活功能。这一多层次负调控网络确保了通路信号的精准调控,避免过度激活导致的病理损伤。
五、JAK/STAT 通路与疾病及靶向药物研发
5.1 通路异常与疾病关联
JAK/STAT 通路的异常激活或调控失衡与多种疾病密切相关。在炎症与免疫性疾病中,细胞因子通过该通路的过度激活可引发慢性炎症反应;在肿瘤领域,JAK 和 STAT 的过度表达或活化常见于白血病、淋巴瘤及多种实体瘤,如 STAT1 在急性髓系白血病中呈组成型激活,STAT3 在霍奇金淋巴瘤、前列腺癌等肿瘤中持续活化促进细胞增殖与存活。此外,SOCS 家族基因的表观遗传沉默(如启动子甲基化)在白血病、肝癌中频发,导致通路抑制缺失,加剧肿瘤进展。
5.2 靶向药物开发进展
目前已有 10 种 JAK 抑制剂获批用于自身免疫性疾病和肿瘤治疗,其安全性与生物制剂相当,但存在血栓栓塞、脂质代谢异常等潜在风险。选择性 JAK 抑制剂及靶向蛋白降解技术的应用,有望提高药物特异性并减少不良反应。STAT 抑制剂的研发采用干扰 SH2 结构域介导的二聚化、DNA 结合或转录激活等策略,多种候选药物已进入临床试验阶段,但尚未有药物获批。此外,SOCS 肽模拟物在免疫调节和肿瘤模型中显示出良好潜力,为通路靶向治疗提供了新方向。
尽管 JAK/STAT 通路研究已取得显著进展,但细胞因子信号在通路中的放大机制仍有待阐明。深入解析通路的复杂调控网络,将为开发高特异性新药提供更多靶点,推动该领域基础研究向临床应用的转化,为相关疾病的治疗带来新希望。
乐备实是国内专注于提供高质量蛋白检测以及组学分析服务的实验服务专家,自2018年成立以来,乐备实不断寻求突破,公司的服务技术平台已扩展到单细胞测序、空间多组学、流式检测、超敏电化学发光、Luminex多因子检测、抗体芯片、PCR Array、ELISA、Elispot、多色免疫组化等30多个,建立起了一套涵盖基因、蛋白、细胞以及组织水平实验的完整检测体系。
我们可提供从样本运输、储存管理、样本制备、样本检测到检测数据分析的全流程服务。凭借严格的实验室管理流程、标准化实验室操作、原始数据储存体系以及实验项目管理系统,已经为超过3000家客户单位提供服务,年检测样本超过100万,受到了广大客户的信任与支持。











 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


