蛋白质 - 蛋白质相互作用(PPIs)是细胞信号传导、代谢调控及生理功能实现的核心分子基础,其空间动态变化直接影响细胞表型与疾病进程。精准解析 PPIs 的亚细胞定位及动态调控模式,对于阐明信号网络激活机制、揭示通路串扰规律具有重要意义。在众多检测技术中,邻近连接检测技术(PLA)凭借高灵敏度、原位分析能力及单分子分辨率等优势,已成为研究蛋白质互作的重要工具,为探索复杂生物系统中的 PPIs 提供了全新视角。
近年来,PLA 技术不断革新,衍生出顺序 PLA、环形 PLA(c-PLA)等改良方法,显著提升了检测严格性、兼容性及通量,使其在基础研究与临床转化中展现出广阔应用前景。本文将系统介绍 PLA 技术原理、衍生方法的技术优势及其在蛋白质互作研究中的核心应用,为深入理解这一技术的生物学价值提供参考。
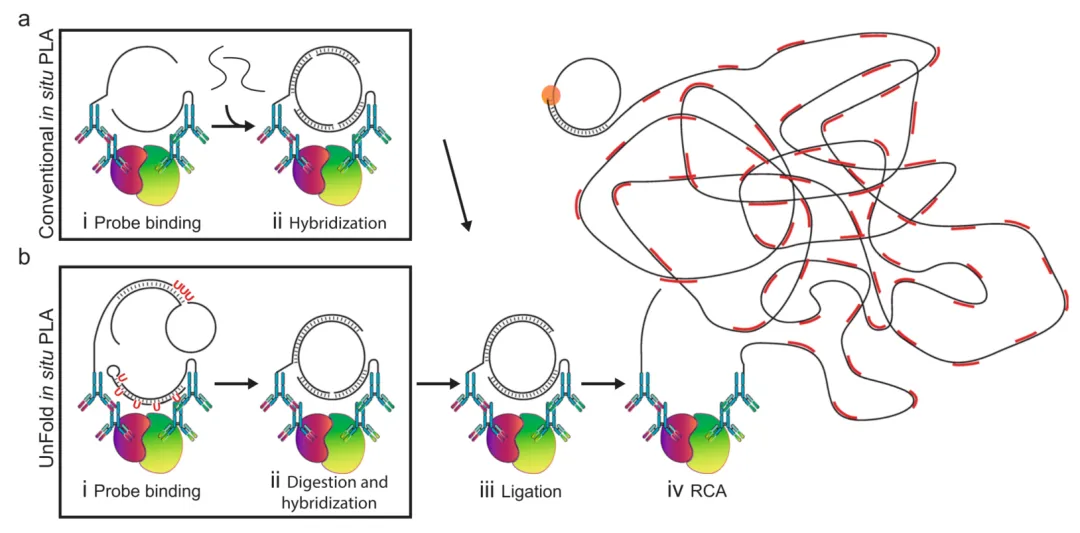
邻近连接检测技术(PLA)是一种将抗体特异性识别与 DNA 信号放大相结合的检测方法,其核心原理基于 “邻近效应” 实现蛋白质互作的可视化与量化。技术流程主要包括:首先,采用两种针对目标蛋白质不同表位的一抗(通常来自不同物种)特异性结合分析物;随后,与一抗结合的 PLA 探针(二抗偶联的 DNA 短链)通过抗原 - 抗体相互作用靠近,当两个目标蛋白质发生相互作用(距离通常小于 20-40nm)时,PLA 探针携带的 DNA 链可在连接酶作用下形成互补双链;最后,通过滚环扩增(RCA)技术对连接后的 DNA 进行信号放大,加入荧光标记的互补寡核苷酸探针后,在荧光显微镜下可观察到代表 PPIs 的明亮荧光斑点,每个斑点对应一对相互作用的蛋白质分子。
这种设计将蛋白质互作信号转化为可检测的 DNA 扩增信号,既保留了抗体检测的特异性,又通过 DNA 扩增实现了超高灵敏度,使低丰度 PPIs 的原位检测成为可能。
PLA 技术的显著优势体现在三个方面:
超高灵敏度:通过滚环扩增实现信号级联放大,检测限可达飞摩尔至纳摩尔级别,能够捕捉生理条件下低丰度蛋白质的微弱相互作用,克服了传统免疫共沉淀技术对高丰度蛋白的依赖。
亚细胞水平空间分辨:无需破坏细胞结构,可在原位保留蛋白质的天然构象与亚细胞定位信息,精准确定 PPIs 在细胞核、细胞质、细胞器等亚结构中的分布模式,为解析信号通路的区域化调控提供直接证据,这一特性也使PLA 技术亚细胞水平蛋白互作原位检测成为研究细胞局部信号网络的关键手段。
强兼容性与多功能整合:可与免疫荧光、流式细胞术、共聚焦显微镜等技术联用,实现蛋白质定位与互作的同步分析;同时适用于细胞培养物、组织切片、临床样本等多种材料,为基础研究向临床转化搭建桥梁。
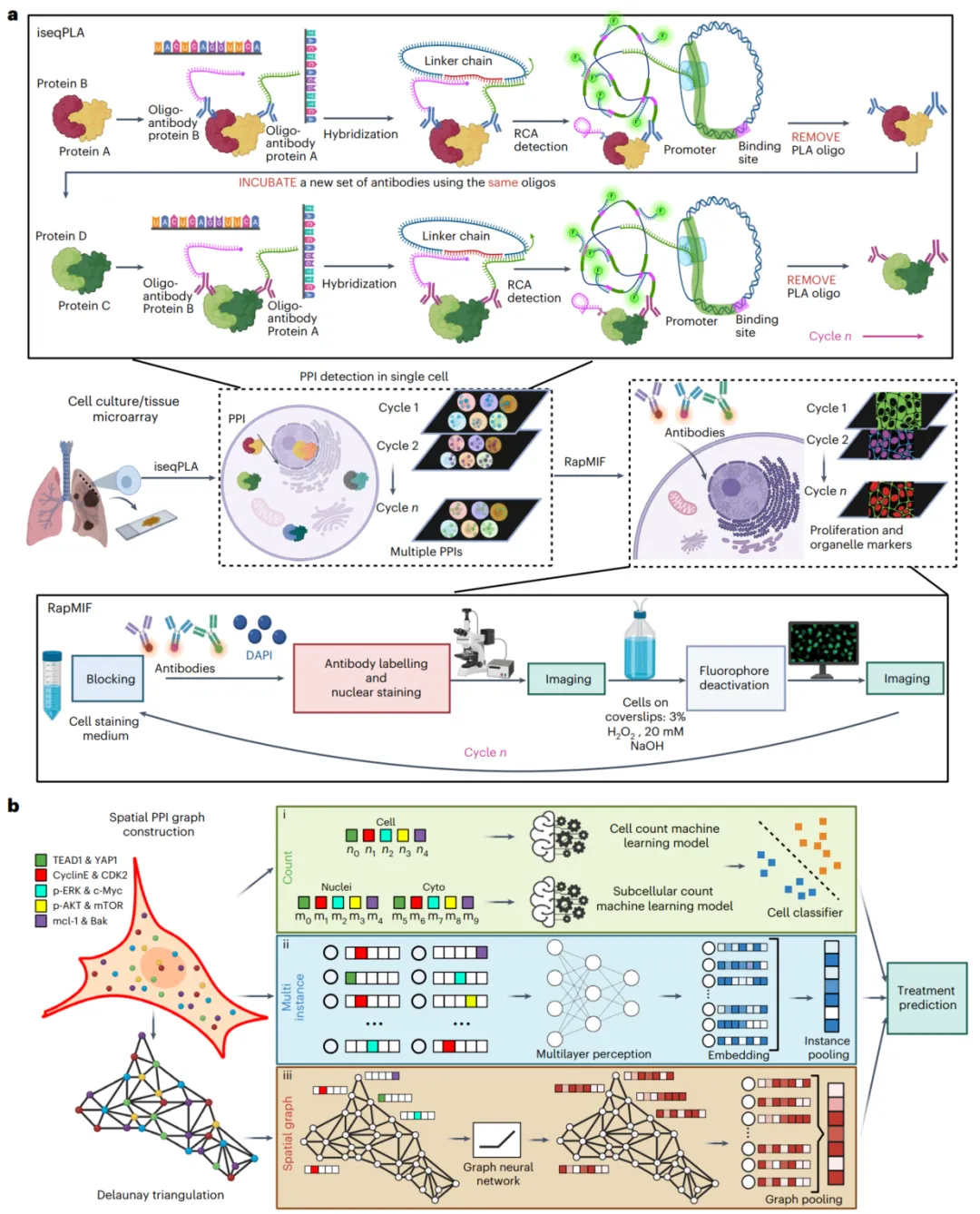
顺序邻近连接检测技术通过多轮 PLA 反应的组合应用,实现了对复杂信号网络中多重 PPIs 的系统分析。研究者利用该方法成功对表皮生长因子受体(EGFR)突变的非小细胞肺癌模型中 47 种蛋白质的相互作用进行了高通量检测,结合免疫荧光技术明确了 PPIs 在亚细胞结构中的共定位特征,充分验证了顺序 PLA 高通量解析肿瘤蛋白互作网络的技术价值。
该技术能够动态追踪药物干预下 PPIs 的时空变化:在酪氨酸激酶抑制剂奥希替尼处理后,可完整重建 EGFR 通路相关 PPIs 的亚细胞分布重塑过程,揭示药物对信号网络的调控机制。基于空间分辨 PPIs 数据构建的图卷积网络,能够准确预测单细胞的药物处理状态,为通过 PPIs 模式解析细胞功能状态提供了新的分析范式,推动了靶向蛋白质互作组的药物设计研究。
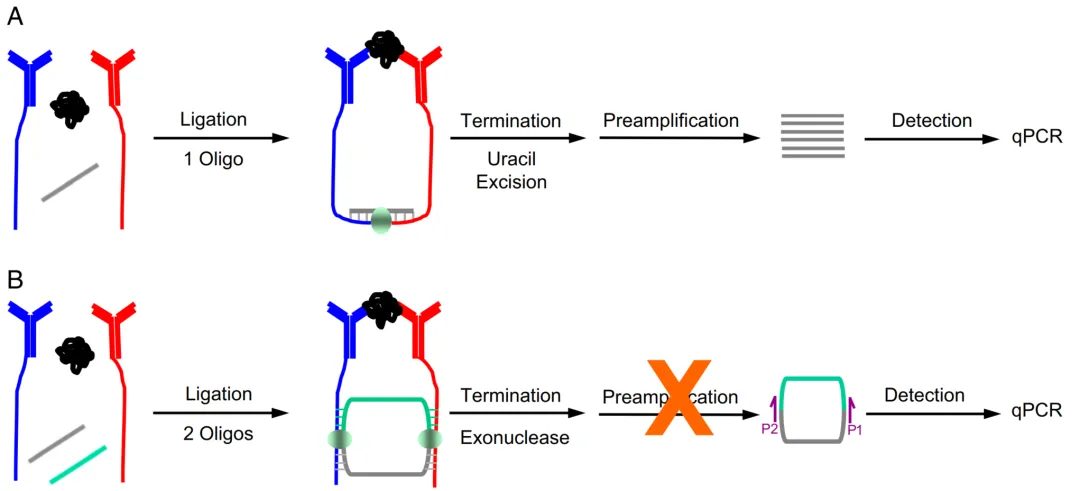
环形邻近连接检测技术(c-PLA)通过优化反应设计,在检测严格性与操作便捷性上实现了突破。与传统 PLA 不同,c-PLA 中两个邻近探针结合分析物后,可引导游离寡核苷酸形成环形 DNA 分子,而非线性双链。这一环形结构设计显著降低了随机背景连接事件,通过酶促反应可高效去除未环化的 DNA,大幅提升了检测信噪比;同时,环形结构增强了抗原 - 探针复合物的稳定性,使检测结果的重现性得到改善。
c-PLA 的独特优势还体现在对低亲和力试剂的兼容性上:面对亲和力较低的抗体时,c-PLA 可通过增加探针浓度提高结合效率,同时避免背景信号升高,解决了传统 PLA 在低亲和力抗体应用中信号弱、背景高的难题。在缓冲液和人体血浆样本中,c-PLA 的灵敏度显著优于传统方法,为临床样本中 PPIs 的检测提供了更可靠的技术选择。
在肿瘤研究中,PLA 技术为解析癌蛋白互作网络提供了关键工具。在淋巴瘤模型中,PLA 可清晰检测癌蛋白 MYC 与抗凋亡蛋白 BCL-2 的相互作用,揭示二者协同促进肿瘤细胞存活的分子机制;在非小细胞肺癌中,通过分析 EGFR 突变细胞中 EGFR 与下游效应分子(如 KRAS、PI3K)的 PPIs 动态变化,可阐明酪氨酸激酶抑制剂耐药的潜在机制,为开发联合治疗策略提供依据。PLA 技术能够在临床组织样本中保留 PPIs 的空间分布信息,使患者特异性互作模式与临床预后的关联分析成为可能。
PLA 技术在药物研发中可用于验证靶点互作及评估药物干预效果,PLA 技术药物干预蛋白互作疗效评估已成为靶向治疗研究的重要手段。在靶向治疗研究中,通过对比药物处理前后 PPIs 的荧光斑点数量与分布变化,可直接反映抑制剂对目标互作的阻断效率。在奥希替尼处理的 EGFR 突变肺癌细胞中,PLA 可实时追踪 EGFR 二聚化水平的降低及下游信号通路 PPIs 的解体过程,为优化药物剂量、预测耐药风险提供量化指标。
在罕见病研究中,PLA 技术结合单分子成像可解析基因突变导致的蛋白质互作异常。对于因蛋白质结合域突变引发的罕见遗传病,PLA 能够在单细胞水平检测突变蛋白与野生型蛋白在互作效率、亚细胞定位上的差异,为阐明致病机制提供直接证据。在神经退行性疾病中,PLA 可用于研究异常聚集蛋白(如 tau 蛋白、α- 突触核蛋白)的互作模式,揭示疾病进展的分子基础。
PLA 技术及其衍生方法的不断创新,为蛋白质互作研究提供了更强大的工具。未来,随着高通量 PLA 技术的发展,有望实现单细胞水平上数百种 PPIs 的并行分析,推动蛋白质互作组学的精准解析;结合超分辨显微镜技术,可进一步突破光学衍射极限,在纳米尺度上揭示 PPIs 的动态组装过程。c-PLA 等改良方法在临床样本检测中的应用,将促进 PPIs 作为新型生物标志物在疾病诊断与预后评估中的转化。
作为解析蛋白质互作的核心技术,PLA 正从基础研究向临床应用快速推进,其在信号网络解析、药物研发及精准医疗中的价值将不断凸显,为深入理解生命活动规律及疾病防治提供有力支撑。
乐备实是国内专注于提供高质量蛋白检测以及组学分析服务的实验服务专家,自2018年成立以来,乐备实不断寻求突破,公司的服务技术平台已扩展到单细胞测序、空间多组学、流式检测、超敏电化学发光、Luminex多因子检测、抗体芯片、PCR Array、ELISA、Elispot、多色免疫组化等30多个,建立起了一套涵盖基因、蛋白、细胞以及组织水平实验的完整检测体系。
我们可提供从样本运输、储存管理、样本制备、样本检测到检测数据分析的全流程服务。凭借严格的实验室管理流程、标准化实验室操作、原始数据储存体系以及实验项目管理系统,已经为超过3000家客户单位提供服务,年检测样本超过100万,受到了广大客户的信任与支持。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


