一、免疫平衡:免疫应答与免疫耐受的动态调节
适应性免疫系统的精准功能依赖于免疫应答与免疫耐受的动态平衡,这不仅体现在促炎与抗炎效应的协调,更表现为对 “异己” 抗原的激活与 “自身” 抗原的无反应性之间的切换。免疫应答能清除病原体和肿瘤细胞,免疫耐受可避免自身免疫攻击,二者相互制约,共同维持机体稳态。
免疫耐受的建立涉及多种细胞和机制,从免疫细胞发育到外周功能调控,均精细筛选和抑制自身反应性淋巴细胞。T 细胞、B 细胞是免疫耐受的基础,调节性 T 细胞(Treg)主动维持外周耐受,树突状细胞(DC)则作为抗原呈递枢纽调控免疫应答方向,它们的功能及调控机制构成了适应性免疫系统稳态的核心网络。
二、T 细胞与 B 细胞:适应性免疫耐受的基础构建
T淋巴细胞的定义和主要功能是什么?核心细胞,负责细胞免疫和辅助体液免疫。T 细胞和 B 细胞通过中枢和外周耐受机制,维系免疫耐受基础。
(一)中枢耐受:淋巴细胞发育中的 “质量筛选”
中枢耐受是淋巴细胞发育早期的第一道屏障,分别发生在 T 细胞的胸腺发育和 B 细胞的骨髓成熟过程。记忆性淋巴细胞的功能和意义何在?长期存活,介导更快更强的二次免疫应答。
B 细胞在骨髓发育时,未成熟 B 细胞经 BCR 的 VDJ 重排形成多样抗原识别库,约 75% 的早期未成熟 B 细胞有自身反应性,其中 1/3 通过二次 Ig 基因重排(受体编辑)降低自身反应性,无法修正的则启动凋亡,减少成熟 B 细胞中自身反应性克隆比例。
T 细胞在胸腺经历 TCR 基因重排后,需经阳性和阴性选择。阳性选择确保其识别自身 MHC 分子,阴性选择清除对自身抗原 - MHC 复合物高亲和力的克隆。不识别 MHC 或高亲和力结合的 T 细胞凋亡,仅低亲和力结合的存活并分化为成熟 CD4⁺或 CD8⁺T 细胞,降低对自身组织的攻击性。
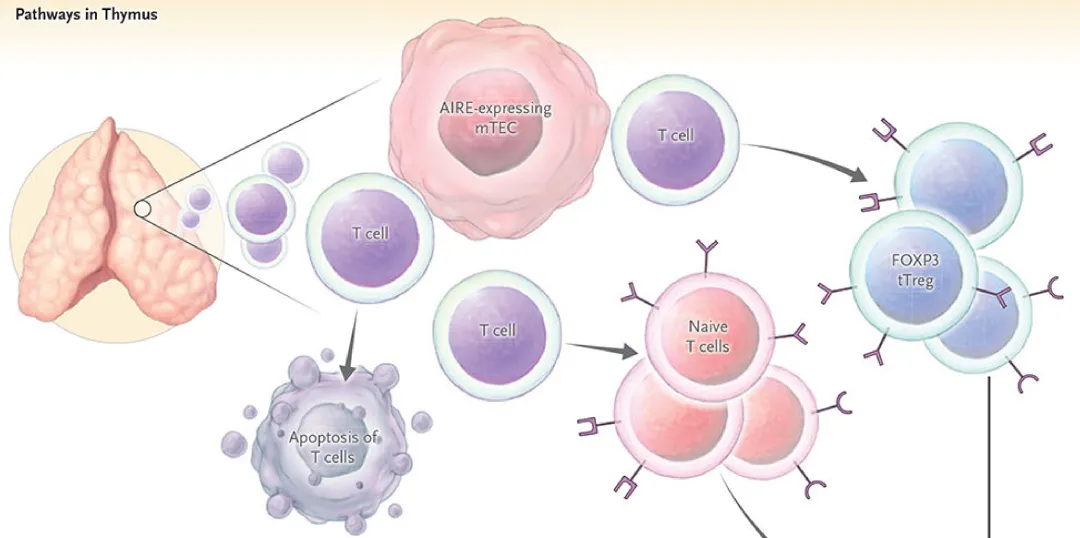
(二)外周耐受:中枢筛选后的 “补救机制”
约 25%-40% 的自身反应性 T 细胞和 40% 的自身反应性 B 细胞会逃逸中枢筛选,外周耐受成为重要补救措施。
T 细胞激活需三个信号:TCR 与 MHC - 抗原肽结合(第一信号)、共刺激受体与共刺激分子结合(第二信号)、细胞因子与受体结合(第三信号)。仅存第一信号或跳过前两信号直接激活第三信号,会诱导 T 细胞无反应性,表现为功能失活、增殖受抑且无法分泌 IL-2。重复抗原刺激、IL-10 作用及共抑制信号激活,也能巩固外周耐受。
B 细胞激活需 BCR 与抗原结合(第一信号)、TLR 信号(第二信号)、Th 细胞共刺激(第三信号)。缺乏第二或第三信号时,即使 BCR 与自身抗原高亲和力结合,也会诱导其克隆缺失或无反应性,抑制自身反应性 B 细胞活化。
抗原水平影响淋巴细胞命运:高水平诱导无反应性,低水平易触发凋亡。且 T、B 细胞无反应性非永久,抗原刺激消除后功能可部分恢复,与慢性感染或肿瘤中淋巴细胞耗竭相关。
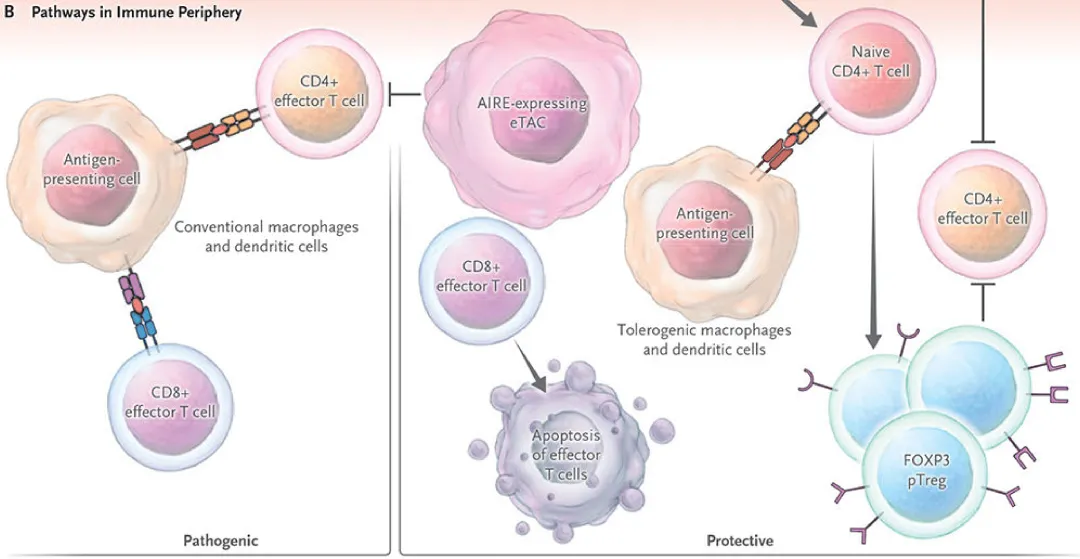
三、调节性 T 细胞:外周耐受的主动调控者
调节性 T 细胞(Treg)通过主动抑制效应性免疫细胞活性,维持外周免疫耐受,主要亚群有 Foxp3⁺Treg 和 Foxp3⁻Treg(如 Tr1 细胞)。
Foxp3⁺Treg 特征性表达 Foxp3,胸腺成熟后迁移至外周,识别自身抗原抑制效应性 T 细胞活化。其通过与效应性 T 细胞直接接触,竞争性结合 APC 表面共刺激分子,分泌 IL-10、TGF-β 等抗炎因子,抑制 T 细胞增殖与细胞因子分泌。
Foxp3⁻Treg(以 Tr1 为代表)通过分泌细胞因子和表达抑制性分子发挥作用。产生大量 IL-10 和 TGF-β 抑制 T 细胞功能;表达穿孔素和颗粒酶 B 杀伤 APC;高表达 CTLA-4、PD-1 接触抑制 T 细胞;表达 CD39 降解 ATP 为腺苷间接抑制免疫反应,在黏膜组织耐受维持中作用重要。
Treg 功能具可塑性,数量和活性异常会致耐受失衡。Foxp3⁺Treg 功能缺陷引发自身免疫病,肿瘤微环境中 Treg 富集抑制抗肿瘤免疫,精准调控其功能是治疗自身免疫病和肿瘤的重要策略。
四、树突状细胞:免疫耐受的 “枢纽” 调节者
树突状细胞(DC)是功能最强的抗原呈递细胞,既是免疫应答启动关键,也是免疫耐受调控中心介质,全程参与 T、B 细胞分化等调控。传统认为 DC 成熟状态决定功能,未成熟诱导耐受,成熟启动应答。但近年研究表明,诱导耐受需 DC 进入 “耐受性成熟” 状态,与独特转录程序相关:下调共刺激分子,上调共抑制分子;减少促炎因子,增加抗炎分子;增强抗炎代谢产物生成,赋予其诱导 T 细胞无反应性或分化为调节性 T 细胞的能力。
不同 DC 亚群功能有差异:浆细胞样 DC(pDC)稳态下分布于血液和淋巴组织,激活 T 细胞能力弱,可诱导 Treg 分化;传统 DC(cDC)能递呈抗原,促进 Foxp3⁺Treg 和 Tr1 分化;单核细胞衍生 DC 参与免疫调节,在耐受中具体作用待深入研究。调控 DC 向耐受性表型分化,是开发免疫治疗策略的重要切入点,在自身免疫病、器官移植排斥防治中前景广阔。
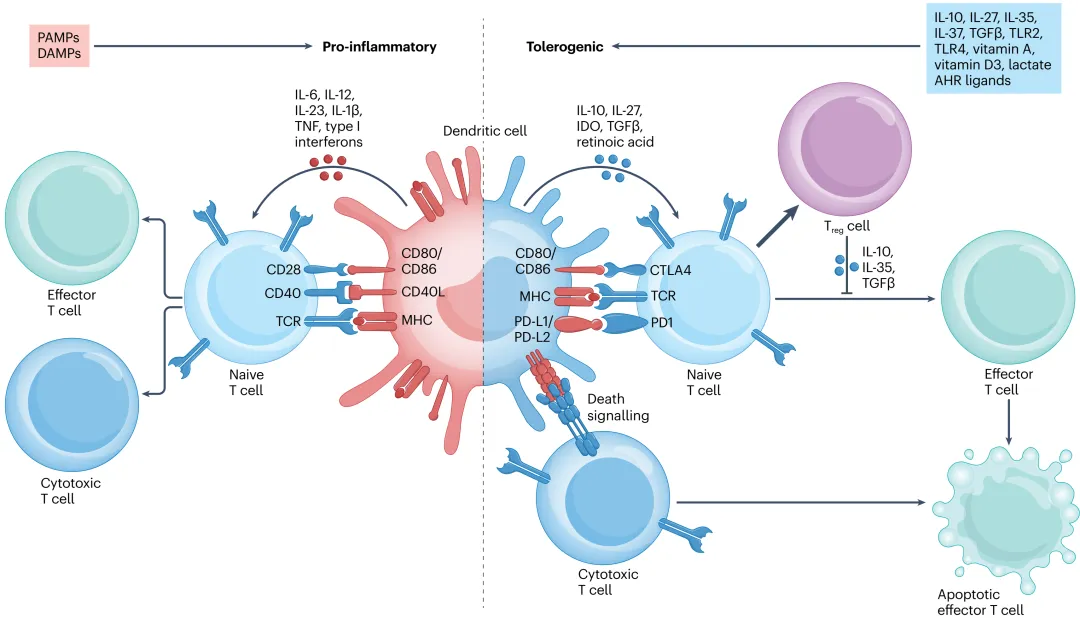
五、总结与展望
T 细胞、B 细胞、Treg 和 DC 通过功能协作,构建多层次免疫耐受网络,同时保障对病原体的应答。T、B 细胞的中枢筛选与外周无反应性是耐受基础,Treg 主动维持外周稳态,DC 整合信号决定应答方向。
这些细胞的调控机制为疾病治疗提供靶点:增强免疫应答可治感染和肿瘤,诱导免疫耐受对自身免疫病等至关重要。未来深入解析细胞互作网络及调控机制,将推动免疫治疗优化,为维持免疫平衡、防治相关疾病提供精准理论和方案。
乐备实是国内专注于提供高质量蛋白检测以及组学分析服务的实验服务专家,自2018年成立以来,乐备实不断寻求突破,公司的服务技术平台已扩展到单细胞测序、空间多组学、流式检测、超敏电化学发光、Luminex多因子检测、抗体芯片、PCR Array、ELISA、Elispot、多色免疫组化等30多个,建立起了一套涵盖基因、蛋白、细胞以及组织水平实验的完整检测体系。
我们可提供从样本运输、储存管理、样本制备、样本检测到检测数据分析的全流程服务。凭借严格的实验室管理流程、标准化实验室操作、原始数据储存体系以及实验项目管理系统,已经为超过3000家客户单位提供服务,年检测样本超过100万,受到了广大客户的信任与支持。











 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


