一、引言
中国仓鼠卵巢(CHO)细胞因其具备快速增殖能力和对重组蛋白高度准确的翻译后修饰功能,已成为生产治疗性重组蛋白最重要的哺乳动物表达系统。然而,该细胞系统存在能量代谢效率较低的显著缺陷,主要表现为葡萄糖主要通过糖酵解途径代谢为丙酮酸,其中绝大部分(≥90%)进一步转化为乳酸,仅少量丙酮酸进入三羧酸循环(TCA循环)进行高效产能。培养过程中乳酸的大量积累不仅抑制细胞生长与产物合成,还显著增加工艺放大难度,因此深入理解乳酸生成机制并探索其调控策略,已成为细胞培养工程领域的重点研究方向。本文系统阐述CHO细胞中乳酸生成的代谢途径及其功能作用,并综述当前主要调控策略。
二、乳酸生成的代谢途径
乳酸的定义及其在细胞代谢中的生成途径:乳酸是糖酵解的终产物,在缺氧或特定代谢状态下由乳酸脱氢酶催化丙酮酸转化生成,并可形成酸性微环境。乳酸在CHO细胞中的生物合成主要依赖三大代谢路径:糖酵解途径、谷氨酰胺分解代谢及氨基酸分解代谢(图一)。葡萄糖是乳酸最主要的碳源前体,经糖酵解生成丙酮酸。为满足快速生长所需能量与还原力,细胞将大量丙酮酸还原为乳酸,此现象即“有氧糖酵效”或Warburg效应。该代谢模式虽可快速产生ATP,却导致碳流效率低下和乳酸积聚。
此外,谷氨酰胺及其他氨基酸的分解代谢也为乳酸合成提供另一重要来源。在细胞代谢这类底物时,会发生脱氨和转氨等反应,产生中间代谢物如丙氨酸,其可进一步经转氨基作用形成丙酮酸,并最终转化为乳酸。这一路径尤其在葡萄糖受限或进入静止期后更显重要。
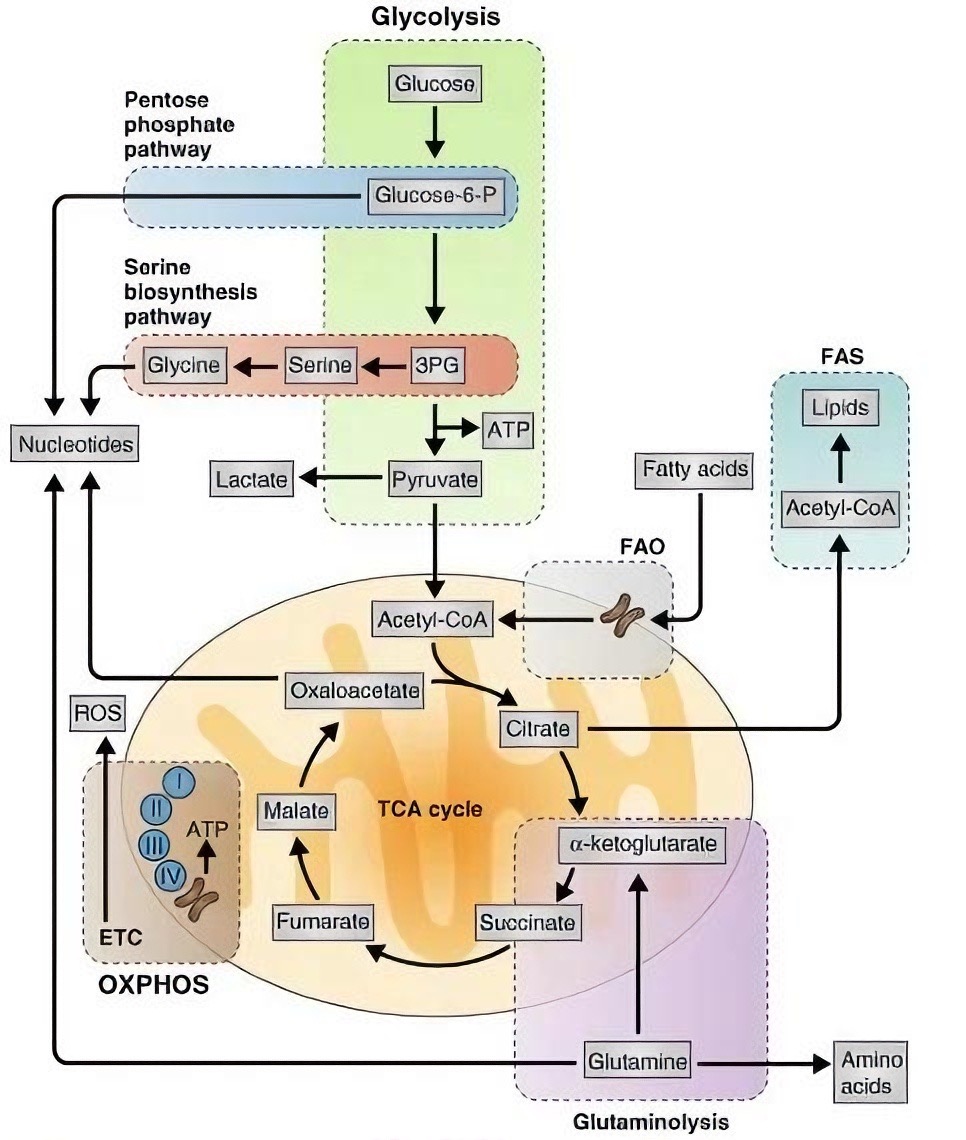
图一:乳酸的生产途径
三、乳酸积累对细胞培养的影响
乳酸的过度积累会引起培养环境pH值下降,进而影响细胞生理状态与功能。高乳酸环境会抑制糖酵解关键酶活性,阻碍细胞正常生长,降低目标蛋白(如单克隆抗体)的表达水平。此外,乳酸也干扰线粒体代谢功能,削弱氧化磷酸化效率,进一步强化糖酵解优势,形成正反馈循环,加剧乳酸堆积。因此,控制乳酸生成、促进其再消耗,是优化CHO细胞培养过程、提高重组蛋白产率的关键环节。乳酸在肿瘤免疫抑制与神经能量供应中的双重影响:乳酸不仅可抑制抗肿瘤免疫反应,促进恶性进展,还能作为重要能量底物参与神经系统的代谢支持。
四、乳酸代谢的调控策略
1. 细胞株改造与筛选
乳酸脱氢酶(LDH)是催化丙酮酸与乳酸相互转化的关键酶,其活性直接影响乳酸生成速率。利用RNA干扰或CRISPR/Cas9等基因编辑技术下调LDH表达,可显著降低乳酸积累,提高抗体产量。另一方面,调控丙酮酸脱氢酶激酶(PDHKs)表达以增强丙酮酸脱氢酶复合体(PDC)活性,有助于将丙酮酸导入线粒体进入TCA循环,从而减少乳酸生成并促进既有乳酸消耗(图二)。
在克隆筛选方面,由于外源基因在CHO基因组中的整合具有随机性,不同克隆的代谢特征差异显著。通过评估乳酸生成与消耗动态,可筛选出具有“乳酸转消耗”表型的高性能克隆,即培养前期适度生成乳酸,中后期高效消耗乳酸,最终实现乳酸净减少。
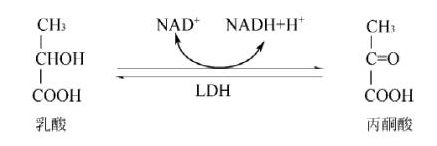
图二:乳酸和丙酮酸相互转换途径
2. 控制葡萄糖供给与碳源替代
控制葡萄糖浓度是实践中降低乳酸积累最直接的手段。通常将葡萄糖维持在较低水平(如0.5–5 g/L,依细胞表型调整),以避免糖酵解通量过高。此外,采用替代碳源策略也可有效调控乳酸代谢。例如,以半乳糖部分替代葡萄糖,可因半乳糖吸收速率较低(Km值较高)而延缓碳代谢流,促使细胞在葡萄糖耗竭后重新利用乳酸,并改善后期乳酸代谢。其他碳源如果糖、甘露糖等也有类似效果,但需注意其对蛋白糖基化修饰(如G0F、G1F、G2F等糖型)的潜在影响,应在工艺优化中综合考量。
3. 促进乳酸再利用
理想情况下,CHO细胞应能在培养中后期将乳酸作为碳源加以利用。促进乳酸消耗的核心在于增强线粒体氧化代谢能力。研究表明,补加铜离子可提升细胞色素C氧化酶Ⅱ(SCO2)的活性——该酶是线粒体电子传递链的关键组分,铜作为其辅因子有助于提高呼吸链效率,推动丙酮酸进入TCA循环,从而促进乳酸向丙酮酸转化并进一步降解。
4. 培养基设计与补料策略优化
培养基组成显著影响乳酸代谢格局。通过系统筛选基础与补料培养基配方,优化碳氮源种类、浓度及比例,可构建低乳酸积累风险的培养体系。此外,补料策略也极为重要:相比批次或间歇补料,采用连续或频次较高的低量补料方式,能更好地维持代谢稳态,避免营养过剩引发糖酵解爆发,从而有效控制乳酸生成。
五、总结与展望
乳酸代谢是CHO细胞能量代谢网络中的关键环节,其生成与消耗动态直接影响细胞生长、产物合成与工艺稳健性。降低乳酸积累需从系统代谢角度出发,结合基因工程、代谢调控、培养基优化及过程策略等多层次手段,推动碳流向高效产能途径迁移。未来研究应更深入解析乳酸调控的分子机制,尤其是线粒体功能与糖酵解通量之间的协调机制,为进一步理性优化CHO细胞生产性能提供理论支撑。
乐备实是国内专注于提供高质量蛋白检测以及组学分析服务的实验服务专家,自2018年成立以来,乐备实不断寻求突破,公司的服务技术平台已扩展到单细胞测序、空间多组学、流式检测、超敏电化学发光、Luminex多因子检测、抗体芯片、PCR Array、ELISA、Elispot、多色免疫组化等30多个,建立起了一套涵盖基因、蛋白、细胞以及组织水平实验的完整检测体系。
我们可提供从样本运输、储存管理、样本制备、样本检测到检测数据分析的全流程服务。凭借严格的实验室管理流程、标准化实验室操作、原始数据储存体系以及实验项目管理系统,已经为超过3000家客户单位提供服务,年检测样本超过100万,受到了广大客户的信任与支持。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


