一、CRISPR系统为何能成为基因编辑的核心工具?
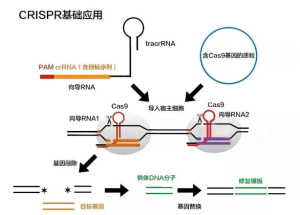
CRISPR基因编辑技术的核心在于其独特的分子机制。作为细菌和古菌适应性免疫系统的重要组成部分,CRISPR系统通过RNA引导的核酸内切酶活性,实现了对特定DNA序列的精准识别和切割。Cas9蛋白作为该系统中最具代表性的核酸酶,在与向导RNA形成复合物后,能够根据RNA序列特异性识别并结合靶DNA,随后通过其核酸内切酶活性在特定位点产生双链断裂。这种基于RNA-DNA互补配对的靶向机制,赋予了CRISPR系统高度的灵活性和可编程性。
在基因组编辑效率方面,CRISPR系统展现出显著优势。相较于早期的锌指核酸酶和转录激活因子样效应物核酸酶技术,CRISPR系统具有设计简单、操作便捷、编辑效率高等特点。研究者只需设计相应的向导RNA序列,即可实现对特定基因位点的靶向编辑。这种简化的操作流程大幅降低了基因编辑的技术门槛,使得该技术得以在各类实验室中广泛应用。
在靶向特异性方面,CRISPR系统虽然存在一定的脱靶风险,但通过多种策略可以有效提高编辑精度。包括优化向导RNA设计算法、使用高保真Cas9变体、开发双切口酶策略等。这些技术改进显著降低了非特异性切割事件的发生频率,使CRISPR系统在需要高精确度的应用场景中更加可靠。
二、CRISPR系统如何实现精准基因组修饰?
CRISPR系统的精准基因组修饰能力主要依赖于细胞自身的DNA修复机制。当Cas9蛋白在靶位点产生双链断裂后,细胞会启动两种主要修复途径:非同源末端连接和同源定向修复。这两种修复机制为不同类型的基因组编辑提供了基础。
非同源末端连接通常导致基因功能丧失,适用于基因敲除研究。该修复过程往往引入小的插入或缺失,从而破坏基因的编码序列或调控元件。研究者可以利用这一特性,通过设计多个向导RNA同时靶向同一基因的不同区域,提高基因敲除效率。在功能基因组筛选中,这种基于CRISPR的基因敲除技术已被广泛应用于基因功能研究。
同源定向修复则为精确基因修饰提供了可能。通过提供包含特定序列的同源修复模板,研究人员可以引导细胞在断裂位点进行精准的序列替换或插入。这一技术不仅可用于纠正致病基因突变,还可用于基因功能研究中的特定氨基酸替换、报告基因整合等应用。近年来,通过优化修复模板设计和改进递送策略,同源定向修复的效率已得到显著提升。
三、CRISPR技术在疾病治疗中有何应用前景?
在遗传性疾病治疗领域,CRISPR技术展现出巨大潜力。通过精确纠正致病基因突变,该技术为单基因遗传病的根治提供了新的可能。例如,在β-地中海贫血和镰状细胞病等血红蛋白疾病中,通过编辑造血干细胞中的相关基因,已有研究报道取得了显著的治疗效果。这些进展为临床应用奠定了基础,但仍需进一步优化编辑效率和安全性。
在肿瘤免疫治疗方面,CRISPR技术通过改造T细胞的基因组成,能够增强其抗肿瘤活性。通过敲除免疫检查点基因或引入特异性肿瘤识别受体,可以显著提升T细胞对肿瘤细胞的识别和杀伤能力。目前,基于CRISPR的CAR-T细胞疗法已在多种血液系统恶性肿瘤中显示出良好的治疗效果。
在传染病防治领域,CRISPR技术也展现出独特价值。通过设计针对病毒基因组的向导RNA,可以在感染细胞中特异性切割病毒DNA或RNA,从而抑制病毒复制。此外,利用CRISPR系统开发快速、灵敏的病原体检测方法,为传染病监测提供了新的技术选择。这些应用不仅拓展了CRISPR技术的使用范围,也为传染病防控提供了新的工具。
四、CRISPR技术面临哪些技术挑战与安全性考量?
脱靶效应仍然是CRISPR技术面临的主要挑战之一。即使在优化设计的情况下,Cas9蛋白仍可能在某些非靶位点产生切割,导致非预期的基因突变。为应对这一挑战,研究者已开发出多种策略,包括使用高保真Cas9变体、优化向导RNA设计、开发基于核酸酶失活Cas9的碱基编辑器等。这些技术改进显著提高了CRISPR系统的特异性。
递送效率与组织特异性是临床应用中的另一关键问题。有效的体内基因编辑需要将CRISPR组分高效递送至目标细胞,并在特定组织或细胞类型中发挥功能。目前,病毒载体和非病毒载体各有优势和局限:病毒载体通常具有较高的转导效率,但可能引起免疫反应;非病毒载体虽然安全性更好,但递送效率往往较低。开发新型递送系统,提高靶向性和安全性,是推动CRISPR技术临床应用的重要方向。
免疫原性反应是CRISPR治疗需要特别关注的问题。由于Cas9蛋白来源于细菌,人体内可能存在预先存在的免疫反应,这可能导致治疗效果降低或引发不良免疫反应。为克服这一障碍,研究人员正在探索多种策略,包括使用人源化Cas9蛋白、开发免疫原性较低的Cas9变体,以及通过短暂表达或局部递送减少免疫暴露。
五、CRISPR系统的技术创新方向何在?
新型CRISPR工具的不断涌现,极大拓展了基因编辑的应用范围。碱基编辑技术能够在不断裂DNA双链的情况下,实现特定碱基的精确转换,为纠正点突变提供了更安全的替代方案。该技术通过将失活的Cas9与碱基脱氨酶融合,在不产生双链断裂的情况下完成碱基编辑,显著降低了插入缺失等副产物的产生。
引导编辑器代表了CRISPR技术的又一重要突破。该系统结合了Cas9切口酶活性和逆转录酶功能,能够实现精确的DNA序列插入、删除和替换。与传统同源定向修复相比,引导编辑不依赖细胞自身的同源修复机制,编辑效率更高且副产物更少,为基因组工程提供了新的工具选择。
表观基因组编辑是CRISPR技术的又一重要拓展。通过将催化失活的Cas9与表观修饰酶融合,可以在不改变DNA序列的情况下,调控特定基因的表达水平。这种表观遗传编辑具有可逆性,为研究表观调控机制和治疗表观遗传相关疾病提供了有力工具。
六、基因编辑技术将如何影响生命科学研究范式?
CRISPR技术正在深刻改变基础研究的方法论。其高通量筛选能力使得在全基因组范围内研究基因功能成为可能。通过构建全基因组范围的CRISPR文库,研究人员可以系统性地探索基因与表型之间的关系,发现新的药物靶点和疾病机制。这种系统生物学方法为理解复杂生命过程提供了前所未有的视角。
在合成生物学领域,CRISPR技术为实现复杂的基因线路设计提供了关键工具。通过精确调控多个基因的表达时序和水平,研究人员可以构建具有特定功能的合成生物系统。这些系统在生物制造、环境修复、疾病治疗等领域具有广阔应用前景,展示了合成生物学的巨大潜力。
伦理与监管框架的完善对于CRISPR技术的健康发展至关重要。随着技术的不断进步,建立适当的伦理准则和监管体系,平衡技术创新与社会责任,已成为国际社会的共识。特别是在人类生殖细胞编辑等敏感领域,需要建立全球性的科学规范和伦理标准,确保技术发展符合人类共同利益。
综上所述,CRISPR基因编辑技术正在重塑生命科学研究的基本范式,并为疾病治疗提供了新的可能性。随着技术的不断发展和完善,其在基础研究和临床应用中的价值将进一步凸显。然而,技术发展必须与伦理考量并重,确保基因编辑技术的安全和负责任的应用,最终造福人类社会。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


