一、IL-7及其受体系统的生物学特征
白细胞介素-7(IL-7)是IL-2细胞因子超家族成员,为T淋巴细胞和B淋巴细胞发育所必需的关键因子。该细胞因子主要由骨髓基质细胞、胸腺上皮细胞及特定非造血细胞产生,通过自分泌与旁分泌方式在初级淋巴器官微环境中发挥功能。
IL-7受体(IL-7R)由独特的α链(CD127)与γ链(γc)组成异二聚体。其中γ链为IL-2、IL-4、IL-9、IL-15和IL-21受体所共享,而IL-7Rα的表达则呈现严格的细胞类型特异性与时空调控模式。这种受体组成决定了IL-7信号的转导特性及其生物学效应的多样性。
二、IL-7信号通路与下游效应
IL-7与受体结合后,主要通过JAK1/JAK3-STAT5通路传递信号。磷酸化的STAT5转位至细胞核,调控包括细胞周期、代谢和存活相关的基因转录程序。同时,该通路还激活PI3K-AKT和MAPK信号分支,形成复杂的调控网络。
核心生物学效应包括:
1.促进抗凋亡蛋白BCL-2和MCL1的表达
2.抑制促凋亡分子BAX、BIM、BAD的活性
3.下调细胞周期抑制蛋白p27
4.参与胸腺细胞T细胞受体基因重排的表观遗传调控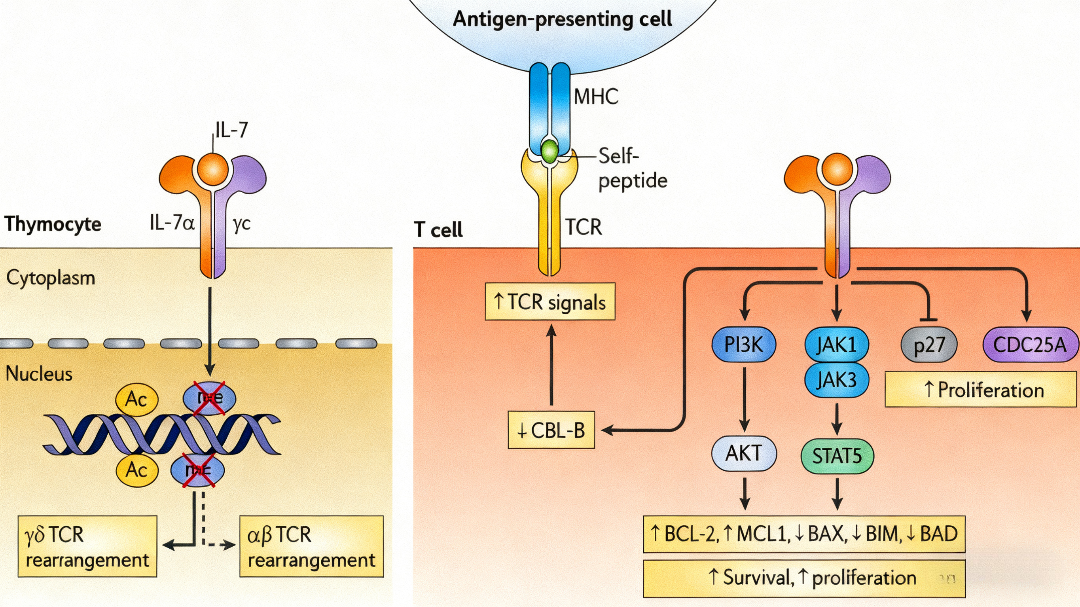
三、IL-7R的表达调控与细胞发育谱系
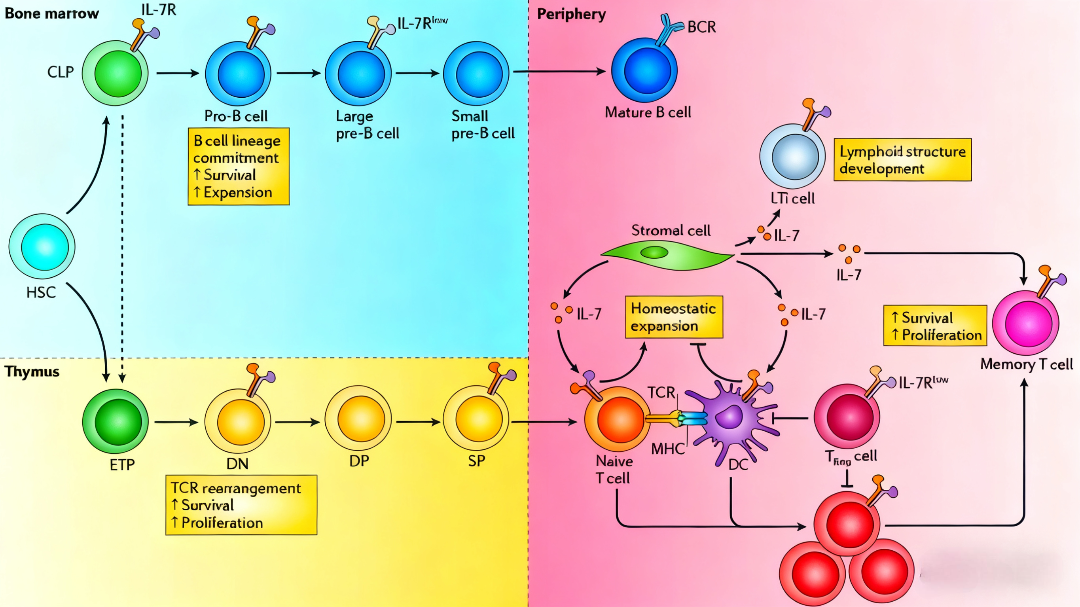
1. B细胞发育阶段
共同淋巴祖细胞(CLP)阶段开始表达IL-7Rα
原B细胞和前B细胞阶段维持高表达
成熟B细胞阶段表达下调
2. T细胞发育阶段
早期胸腺祖细胞(ETP)不表达IL-7Rα
双阴性(DN)胸腺细胞开始表达并依赖IL-7信号
双阳性(DP)阶段表达下调
单阳性(SP)胸腺细胞重新表达
3. 外周T细胞亚群
初始T细胞高表达IL-7Rα
效应T细胞通常下调表达
记忆T细胞前体维持IL-7Rα表达,依赖IL-7维持生存与稳态
4. 其他免疫细胞
淋巴组织诱导细胞(LTi)
特定树突状细胞亚群
四、IL-7在肿瘤免疫中的复杂作用
1. 抗肿瘤免疫增强作用
多项临床前研究表明,外源性IL-7可通过以下机制增强抗肿瘤免疫:
促进胸腺输出和T细胞发育,增加T细胞库多样性
增强CD8+细胞毒性T淋巴细胞的扩增与效应功能
促进记忆T细胞的形成与维持
改善T细胞受体信号转导能力
在胶质瘤、黑色素瘤、淋巴瘤等模型中显示抗肿瘤活性
2. 潜在的促肿瘤风险
部分研究提示IL-7在某些肿瘤微环境中可能具有不利影响:
通过上调BCL-2家族蛋白促进肿瘤细胞存活
调节细胞周期蛋白加速肿瘤增殖
在膀胱癌等模型中可能与侵袭迁移表型相关
在特定实体瘤中可能存在免疫抑制微环境的复杂调控
这种双重作用可能与IL-7浓度、作用时长、肿瘤类型及微环境特性密切相关。
五、IL-7家族其他成员的功能扩展
除IL-7外,该家族还包括胸腺基质淋巴细胞生成素(TSLP),其受体由TSLPR与IL-7Rα链组成。TSLP主要在屏障组织(如皮肤、肺、肠道)上皮细胞中产生,在2型免疫应答、过敏反应和上皮屏障功能维护中发挥关键作用。TSLP信号同样通过JAK-STAT通路转导,但与IL-7具有不同的细胞特异性与生物学效应。
六、IL-7靶向治疗的临床转化
1. 重组IL-7蛋白治疗
NT-I7(efineptakin alfa)作为长效重组IL-7-Fc融合蛋白,已在多形性胶质母细胞瘤中获得孤儿药资格。其临床优势包括:
延长体内半衰期,减少给药频率
选择性扩增T细胞而不显著影响调节性T细胞
增强肿瘤浸润淋巴细胞数量与功能
2. 其他治疗策略
IL-7Rα靶向抗体:调节IL-7信号强度
JAK激酶抑制剂:调控下游信号通路
联合治疗策略:与免疫检查点抑制剂、CAR-T细胞疗法等联合应用
七、临床挑战与未来方向
1. 剂量与时机优化
IL-7治疗存在明显的剂量效应关系,过高剂量可能导致免疫病理或促进自身免疫反应。治疗时机的选择也至关重要,在免疫重建阶段与免疫效应阶段的干预策略需区别对待。
2. 生物标志物开发
迫切需要建立预测IL-7治疗反应的生物标志物体系,包括:
IL-7Rα表达水平与信号转导状态
T细胞受体库多样性评估
肿瘤微环境免疫特征分析
3. 安全性与耐受性
需关注IL-7治疗可能引发的细胞因子释放综合征、自身免疫现象及感染风险增加等不良反应。
八、IL-7细胞因子检测服务哪个公司提供?
IL-7作为免疫系统发育与稳态的关键调节因子,在肿瘤免疫治疗中展现出重要潜力。其复杂的功能网络提示,精准调控IL-7信号强度、作用时机及靶向细胞群体,将是实现治疗获益最大化的关键。
| 货号 | Panel名称 | 种属 | 检测指标 |
| LXLTH34-1 | 人细胞因子/趋化因子-34因子Panel | Human | GM-CSF,IFN gamma,IL-1 beta,IL-2,IL-4,IL-5,IL-6,IL-8,IL-12p70,IL-13,IL-18,TNF alpha,IL-9,IL-10,IL-17A (CTLA-8),IL-21,IL-22,IL-23,IL-27,IFN alpha,IL-1 alpha,IL-1RA,IL-7,IL-15,IL-31,TNF beta,Eotaxin (CCL11),GRO alpha (CXCL1),IP-10 (CXCL10),MCP-1 (CCL2),MIP-1 alpha (CCL3),MIP-1 beta (CCL4),RANTES (CCL5),SDF-1 alpha |
| LXLBH27-1 | 人细胞因子-27因子Panel | Human | G-CSF,GM-CSF,IFN-γ,IL-10,IL-12(p70),IL-13,IL-17A,IL-1β,IL-2,IL-4,IL-5,IL-6,IL-7,IL-8/CXCL8,MCP-1/CCL2,MIP-1β,TNF-α,IL-1Rα,IL-9,IL-15,FGF-basic,Eotaxin/CCL11,IP-10/CXCL10,MIP-1α/CCL3,PDGF-BB,RANTES,VEGF-A |
| LXLBH48-1 | 人细胞因子-48因子Panel | Human | β-NGF,CTACK/CCL27,Eotaxin/CCL11,FGF-basic,G-CSF,GM-CSF,GRO-α (Gro-a/KC/CXCL1),HGF,IFN-α2,IFN-γ,IL-1α,IL-1Rα,IL-2Rα,IL-1β,IL-2,IL-3,IL-4,IL-5,IL-6,IL-7,IL-8/CXCL8,IL-9,IL-10,IL-12(p40),IL-12(p70),IL-13,IL-15,IL-16,IL-17A,IL-18,IP-10/CXCL10,LIF,M-CSF,MCP-1/CCL2,MCP-3/CCL7,MIG,MIP-1α/CCL3,MIP-1β,MIF,PDGF-BB,RANTES,SCF,SCGF-β,SDF-1α,TRAIL,TNF-α,TNF-β,VEGF-A |
| LXLBR23-1 | 大鼠细胞因子-23因子Panel | Mouse | G-CSF,GM-CSF,GRO/KC,IFN-γ,IL-1α,IL-1β,IL-2,IL-4,IL-5,IL-6,IL-7,IL-10,IL-12 (p70),IL-13,IL-17A,IL-18,M-CSF,MCP-1,MIP-1α,MIP-3α,RANTES,TNF-α,VEGF |












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


