在免疫系统的复杂调控网络中,白细胞介素-2(IL-2)无疑是核心枢纽之一。自1976年被发现并命名为“T细胞生长因子”以来,IL-2凭借其既能驱动免疫攻击、又能维持免疫耐受的“双面性”,成为连接基础免疫学与临床治疗的关键分子。它通过精密的受体分级系统、多层次的信号通路调控,在抗肿瘤、抗感染与自身免疫平衡中发挥着不可替代的作用,同时也为免疫治疗的创新提供了丰富的靶点与思路。
一、 分子基础:受体结构决定功能特异性
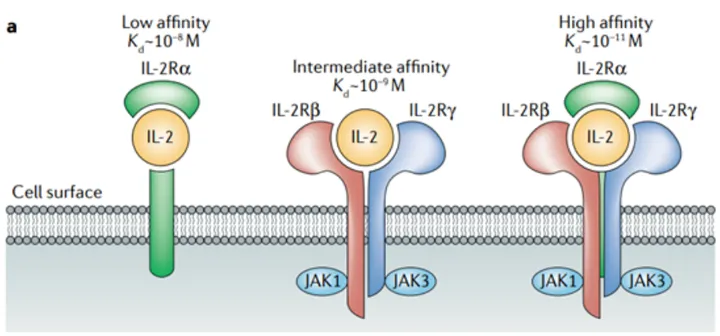
IL-2的功能实现,首先依赖于其与细胞表面受体(IL-2R)的特异性结合,而IL-2R的“分级设计”是其功能分化的核心基础。IL-2R由α链(CD25)、β链(CD122)和γ链(CD132,又称γc)三种亚基组成,三者以不同组合形成低、中、高三种亲和力受体,分别对应不同免疫细胞的功能需求(见下表)。
| 受体类型 | 亚基组成 | 亲和力(Kd) | 主要表达细胞 | 核心功能 |
| 低亲和力受体 | 仅 α 链(CD25) | 10⁻⁷~10⁻⁶ M | 部分活化免疫细胞 | “捕获” IL-2,形成局部细胞因子库 |
| 中亲和力受体 | β 链 +γ 链(CD122+CD132) | 10⁻⁹ M | 静息效应 T 细胞(Teff)、NK 细胞、记忆 T 细胞(Tmem) | 响应中高浓度 IL-2,启动免疫激活 |
| 高亲和力受体 | α 链 +β 链 +γ 链(CD25+CD122+CD132) | 10⁻¹¹ M | 调节性 T 细胞(Treg)、活化 T 细胞 | 响应低浓度 IL-2,维持 Treg 存活与功能 |
这种分级结构的精妙之处在于:高亲和力受体仅在Treg表面稳定表达,即使体内IL-2浓度极低(10-100 U/mL),也能高效捕获信号,确保免疫耐受的基础;而中亲和力受体主要分布于效应免疫细胞,需较高浓度IL-2(>100 U/mL)才能激活,避免免疫反应过度激活。例如,静息状态下的CD8+ T细胞仅表达中亲和力受体,当感染或肿瘤发生时,局部IL-2浓度升高,才会启动其增殖与细胞毒性功能,实现“按需激活”。
二、 信号调控:三条核心通路构建免疫平衡网络
IL-2与受体结合后,通过激活JAK-STAT、PI3K-AKT-mTOR、MAPK-ERK三条核心信号通路,实现对T细胞命运的精准调控,三条通路既独立作用又相互协同,共同维持免疫激活与耐受的动态平衡。
(一)JAK-STAT通路:免疫耐受的“守护者”
IL-2结合受体后,首先诱导β链与γ链的细胞质结构域聚合,激活关联的JAK1(结合β链)与JAK3(结合γ链)激酶。磷酸化的JAK进而使STAT5蛋白磷酸化,形成二聚体后入核,调控关键基因表达:一方面,促进Treg特异性转录因子Foxp3的稳定表达,增强Treg的免疫抑制功能;另一方面,上调抗凋亡蛋白Bcl-2,延长Treg的存活时间。研究证实,STAT5缺陷小鼠会因Treg发育障碍引发严重自身免疫病,直接证明该通路是免疫耐受的核心保障。
(二)PI3K-AKT-mTOR通路:效应T细胞的“动力源”
该通路主要负责为效应T细胞的活化提供代谢支持。IL-2激活PI3K后,通过下游AKT激酶激活mTORC1复合物,启动糖酵解代谢重编程——原本依赖氧化磷酸化的静息T细胞,会快速切换为糖酵解为主的代谢模式,为细胞增殖、颗粒酶B与IFN-γ等细胞毒性分子的合成提供能量。同时,AKT还会抑制Foxo转录因子,阻断其向Treg分化的潜能,确保效应T细胞“专注”于免疫攻击。例如,高剂量IL-2治疗黑色素瘤时,正是通过强力激活该通路,使肿瘤浸润Teff大量扩增,提升杀伤效率。
(三)MAPK-ERK通路:免疫激活的“放大器”
ERK通路的核心作用是形成正反馈循环,增强IL-2的免疫激活效应。IL-2诱导ERK磷酸化后,会促进c-Fos与c-Jun蛋白形成AP-1转录复合体,上调IL-2Rα(CD25)的表达——这使得活化T细胞能更快组装高亲和力受体,进一步增强对IL-2的响应。此外,ERK还能通过磷酸化表观调控因子EZH2,抑制Polycomb复合体的组蛋白甲基转移酶活性,使效应基因(如IFN-γ、颗粒酶B)的染色质处于开放状态,为快速表达做好准备。
三、 功能特性:浓度梯度决定“免疫双面性”
IL-2的“双面性”本质是浓度依赖性功能选择:不同浓度的IL-2会优先激活不同免疫细胞亚群,实现“精准调控”,这一特性也成为其临床应用的核心依据。
(一)高浓度IL-2:抗肿瘤与抗感染的“利器”
当体内IL-2浓度超过100 U/mL时(如感染急性期或高剂量IL-2治疗),会优先结合效应T细胞与NK细胞的中亲和力受体,启动强力免疫攻击:CD8+ T细胞大量增殖,分泌IFN-γ与颗粒酶B,增强对肿瘤细胞或感染细胞的杀伤;NK细胞的细胞毒性活性提升,直接清除异常细胞。临床中,高剂量IL-2(60万IU/kg)已获批用于治疗转移性黑色素瘤与肾细胞癌,客观缓解率达16%,部分患者可获得长期缓解。但高浓度IL-2也会引发严重副作用,如血管渗漏综合征(VLS)——过量激活的免疫细胞会释放大量炎症因子,破坏血管内皮屏障,导致组织水肿与低血压,需在严密监护下使用。
(二)低浓度IL-2:自身免疫病的“调节剂”
当IL-2浓度处于10-100 U/mL时,会优先被Treg的高亲和力受体捕获,选择性增强免疫耐受。例如,在系统性红斑狼疮(SLE)患者中,低剂量IL-2(1-1.5万IU/d)治疗可使外周血Treg比例从3%提升至8%,显著降低疾病活动度;在1型糖尿病患者中,低剂量IL-2能减少自身反应性T细胞对胰岛β细胞的攻击,延缓病情进展。这种“低剂量靶向Treg”的策略,避免了对效应免疫细胞的过度抑制,成为自身免疫病治疗的新方向。
(三)脉冲式IL-2:免疫记忆的“维持者”
生理状态下,IL-2的分泌呈周期性脉冲模式,这种模式能有效维持记忆T细胞的存活。当IL-2以脉冲形式刺激时,会与IL-7、IL-15协同作用,激活记忆T细胞的代谢重编程——既不引发过度增殖,又能维持其对病原体的“记忆”。例如,在慢性病毒感染(如HIV)中,脉冲式IL-2治疗可提升记忆T细胞的数量与功能,增强对病毒的长期控制。
四、 IL-2因子检测服务哪里有?
IL-2作为免疫系统的“双面因子”,其分子机制的解析不仅深化了我们对免疫稳态的理解,也为临床治疗提供了多维度的靶点。从传统高剂量治疗肿瘤、低剂量调控自身免疫,到工程化变体与靶向递送技术的创新,IL-2的应用正从“广谱调控”向“精准靶向”迈进。 未来,随着对IL-2信号网络与免疫细胞互作机制的进一步探索,有望开发出更高效、更安全的IL-2疗法:例如,结合免疫检查点抑制剂(如PD-1抗体),增强效应T细胞的肿瘤浸润;或通过时序调控IL-2浓度,实现“先激活效应细胞、后抑制Treg”的动态治疗。这些创新将推动IL-2在肿瘤、自身免疫病、感染性疾病等领域的应用,为免疫治疗的发展注入新动力。
LabEx多款现货Panel支持IL-2因子检测服务,欢迎咨询~
| Panel | 乐备实官网货号 | 技术平台 | 检测指标 |
| 人炎症10因子Panel | LXMH10-1 | MSD | IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-8,IL-10,IL-12p70,IL-13,TNF-α |
| 人炎症10因子Panel | LXLBH10-1 | Luminex | IL-1 β/IL-1F2,IL-2,IL-4,IL-6 ,IL-8/CXCL8,IL-10,IL-12 p70,IL-13,TNF-α,IFN-γ |
| 小鼠炎症10因子Panel | LXMM10-1 | MSD | IFN-γ,IL-1β,IL-2,IL-4,IL-5,IL-6,IL-10,IL-12p70,KC/GRO,TNF-α |
| 小鼠炎症10因子Panel | LXLBM10-1 | Luminex | IL-1 β/IL-1F2,IL-2,IL-4,IL-5,IL-6 ,IL-10,IL-12p70,CXCL1/GRO/α/KC/CINC-1,IFN-γ,TNF-α |
| 大鼠炎症10因子Panel | LXLBR10-1 | Luminex | IL-1 β/IL-1F2,IL-2,IL-4,IL-5,IL-6 ,IL-10,IL-12p70,CXCL1/GRO/α/KC/CINC-1,IFN-γ,TNF-α |
| 小鼠细胞因子-23因子Panel | LXLBM23-1 | Luminex | Eotaxin/CCL11,G-CSF,GM-CSF,IFN-γ,IL-10,IL-12(p40),IL-12(p70),IL-13,IL-17A,IL-1α,IL-1β,IL-2,IL-3,IL-4,IL-5,IL-6,IL-9,GRO-α (Gro-a/KC/CXCL1),MCP-1/CCL2,MIP-1α/CCL3,MIP-1β,RANTES,TNF-α |
| 大鼠细胞因子-23因子Panel | LXLBR23-1 | Luminex | G-CSF,GM-CSF,GRO/KC,IFN-γ,IL-1α,IL-1β,IL-2,IL-4,IL-5,IL-6,IL-7,IL-10,IL-12 (p70),IL-13,IL-17A,IL-18,M-CSF,MCP-1,MIP-1α,MIP-3α,RANTES,TNF-α,VEGF |
| 人细胞因子-27因子Panel | LXLBH27-1 | Luminex | G-CSF,GM-CSF,IFN-γ,IL-10,IL-12(p70),IL-13,IL-17A,IL-1β,IL-2,IL-4,IL-5,IL-6,IL-7,IL-8/CXCL8,MCP-1/CCL2,MIP-1β,TNF-α,IL-1Rα,IL-9,IL-15,FGF-basic,Eotaxin/CCL11,IP-10/CXCL10,MIP-1α/CCL3,PDGF-BB,RANTES,VEGF-A |
| 小鼠趋化因子-31因子Panel | LXLBM31-1 | Luminex | BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin/CCL11,Eotaxin-2/CCL24,Fractalkine/CX3CL1,GM-CSF,I-309/CCL1,IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-10,IL-16,IP-10/CXCL10,I-TAC/CXCL11,KC/CXCL1,MCP-1/CCL2,MCP-3/CCL7,MCP-5/CCL12,MDC/CCL22,MIP-1α/CCL3,MIP-1β/CCL4,MIP-3α/CCL20,MIP-3β/CCL19,RANTES/CCL5,SCYB16/CXCL16,SDF-1α/CXCL12,TARC/CCL17,TNF-α |
| 人炎症37因子Panel | LXLBH37-1 | Luminex | APRIL/TNFSF13,BAFF/TNFSF13B,sCD30/TNFRSF8,sCD163,Chitinase 3-like 1,gp130/sIL-6Rβ,IFN-α2,IFN-β,IFN-γ,IL-2,sIL-6Rα,IL-8/CXCL8,IL-10,IL-11,IL-12(p40),IL-12(p70),IL-19,IL-20,IL-22,IL-26,IL-27(p28),IL-28A/IFN-λ2,IL-29/IFN-λ1,IL-32,IL-34,IL-35,LIGHT/TNFSF14,MMP-1,MMP-2,MMP-3,Osteocalcin,Osteopontin,Pentraxin-3,TNF-R1,TNF-R2,TSLP,TWEAK/TNFSF12 |
| 人趋化因子/细胞因子-40因子Panel | LXLBH40-1 | Luminex | 6Ckine/CCL21,BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin/CCL11,Eotaxin-2/CCL24,Eotaxin-3/CCL26,Fractalkine/CX3CL1,GCP-2/CXCL6,GM-CSF,GRO-α (Gro-a/KC/CXCL1),Gro-β/CXCL2,I-309/CCL1,IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-8/CXCL8,IL-10,IL-16,IP-10/CXCL10,I-TAC/CXCL11,MCP-1/CCL2,MCP-2/CCL8,MCP-3/CCL7,MCP-4/CCL13,MDC/CCL22,MIF,MIG/CXCL9,MIP-1α/CCL3,MIP-1δ/CCL15,MIP-3α/CCL20,MIP-3β/CCL19,MPIF-1/CCL23,SCYB16/CXCL16,SDF-1α+β/CXCL12,TARC/CCL17,TECK/CCL25,TNF-α |
| 人细胞因子-46因子Panel | LXLRH46-1 | Luminex | CCL2/JE/MCP-1,CCL3/MIP-1 alpha,CCL4/MIP-1 beta,CCL5/RANTES,CCL11/Eotaxin,CCL19/MIP-3 beta,CCL20/MIP-3 alpha,CD40 Ligand/TNFSF5,CXCL1/GRO alpha/KC/CINC-1,CXCL2/GRO beta/MIP-2/CINC-3,CXCL10/IP-10/CRG-2,EGF,FGF basic/FGF2/bFGF,Flt-3 Ligand/FLT3L,G-CSF,GM-CSF,Granzyme B,IFN-alpha 2/IFNA2,IFN-beta,IFN-gamma,IL-1 alpha/IL-1F1,IL-1 beta/IL-1F2,IL-1ra/IL-1F3,IL-2,IL-3,IL-4,IL-5,IL-6,IL-7,IL-8/CXCL8,IL-9,IL-10,IL-12 p70,IL-13,IL-15,IL-17/IL-17A,IL-17E/IL-25,IL-33,Lymphotoxin-alpha/TNF-beta,PD-L1/B7-H1,PDGF-AA,PDGF-AB/BB,TGF-alpha,TNF-alpha,TRAIL/TNFSF10,VEGF |
| 人细胞因子-48因子Panel | LXLBH48-1 | Luminex | β-NGF,CTACK/CCL27,Eotaxin/CCL11,FGF-basic,G-CSF,GM-CSF,GRO-α (Gro-a/KC/CXCL1),HGF,IFN-α2,IFN-γ,IL-1α,IL-1Rα,IL-2Rα,IL-1β,IL-2,IL-3,IL-4,IL-5,IL-6,IL-7,IL-8/CXCL8,IL-9,IL-10,IL-12(p40),IL-12(p70),IL-13,IL-15,IL-16,IL-17A,IL-18,IP-10/CXCL10,LIF,M-CSF,MCP-1/CCL2,MCP-3/CCL7,MIG,MIP-1α/CCL3,MIP-1β,MIF,PDGF-BB,RANTES,SCF,SCGF-β,SDF-1α,TRAIL,TNF-α,TNF-β,VEGF-A |
| 人炎症9因子超灵敏Panel | LXMH09-2 | MSD | IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-10,IL-12p70,IL-17A,TNF-α |












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


