肿瘤的发生发展不仅与肿瘤细胞自身的异常增殖、分化相关,还高度依赖肿瘤微环境(Tumor Microenvironment, TME)中免疫细胞、细胞因子等多种成分的相互作用。趋化因子作为一类具有化学趋化活性的细胞因子,通过与靶细胞表面的趋化因子受体结合,形成特异性信号轴,精准调控免疫细胞和肿瘤细胞的迁移、定位及功能活化,在肿瘤免疫逃逸、血管生成、侵袭转移等关键过程中发挥核心调控作用。 由于肿瘤微环境的异质性及趋化因子受体表达的细胞特异性,趋化因子的生物学效应呈现出显著的复杂性。同一趋化因子作用于不同细胞亚群可能产生完全相反的功能,而不同趋化因子也可能通过协同或拮抗作用共同调控肿瘤进展。深入解析趋化因子系统的作用机制,对于开发新型肿瘤治疗策略具有重要意义。
一、趋化因子的分类及核心作用机制
根据功能差异,趋化因子可分为促瘤趋化因子、抗瘤趋化因子及双效趋化因子三大类,各类趋化因子通过特异性信号轴调控肿瘤发展进程。
(一)促瘤趋化因子
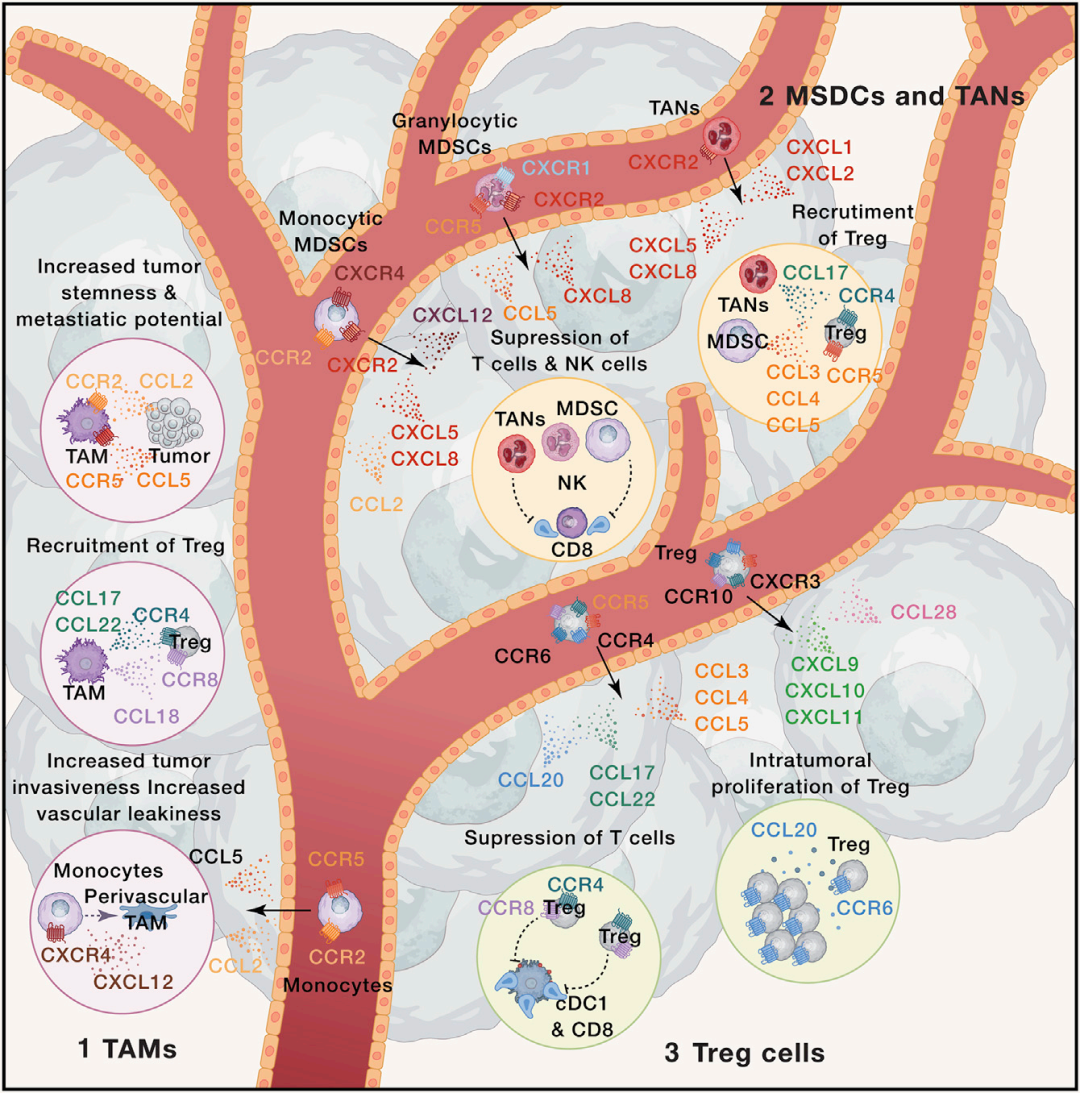
Kohli K, Pillarisetty VG, Kim TS. Key chemokines direct migration of immune cells in solid tumors. Cancer Gene Ther. 2022 Jan;29(1):10-21.
促瘤趋化因子主要通过募集免疫抑制细胞、促进肿瘤血管生成、增强肿瘤细胞干细胞特性及转移能力、介导治疗抵抗等机制加速肿瘤进展,核心成员及作用机制如下:
1. CCL2-CCR2轴:CCL2通过该信号轴特异性募集肿瘤相关免疫抑制细胞,同时介导肿瘤细胞与肿瘤相关巨噬细胞(Tumor-Associated Macrophages, TAM)的相互作用,显著提升肿瘤干细胞特性、转移潜能及对治疗的抵抗能力。
2. CXCL1/CXCL8-CXCR2轴:两类趋化因子共同通过与CXCR2结合,高效募集肿瘤相关免疫抑制细胞,构建免疫抑制性肿瘤微环境,削弱机体抗肿瘤免疫应答。
3. CXCL12-CXCR4轴:该信号轴具有多重促瘤功能:一方面促进TAM分化为血管周围TAM细胞,增加血管通透性,利于肿瘤细胞向血管内浸润;另一方面,实体瘤中骨髓基质细胞高表达CXCL12,导致表达CXCR4的髓样细胞积聚,阻碍免疫细胞发育成熟,同时参与调节性T细胞(Regulatory T cells, Treg)向骨髓的迁移,进一步增强免疫抑制。
4. CCR4、CCR6、CCR8介导的Treg募集与活化:CCR4在肿瘤微环境中特异性募集Treg细胞;CCR6可促进Treg在TME内原位增殖;CCR8则在DC细胞附近募集Treg,并通过CCR8-CCL1轴上调Foxp3表达,维持Treg的免疫抑制功能。此外,CCR4+ Th2、CCR6+ Th17、CXCR3+ Th1、CXCR5+ Tfh等趋化因子受体的表达,也与Treg的抑制功能存在相关性。
5. 其他促瘤趋化因子:CCL17、CCL22通过与CCR4结合进一步募集Treg;CCL18、CCL20等则通过调控肿瘤细胞侵袭性、血管渗漏性等促进肿瘤进展。
(二)抗瘤趋化因子
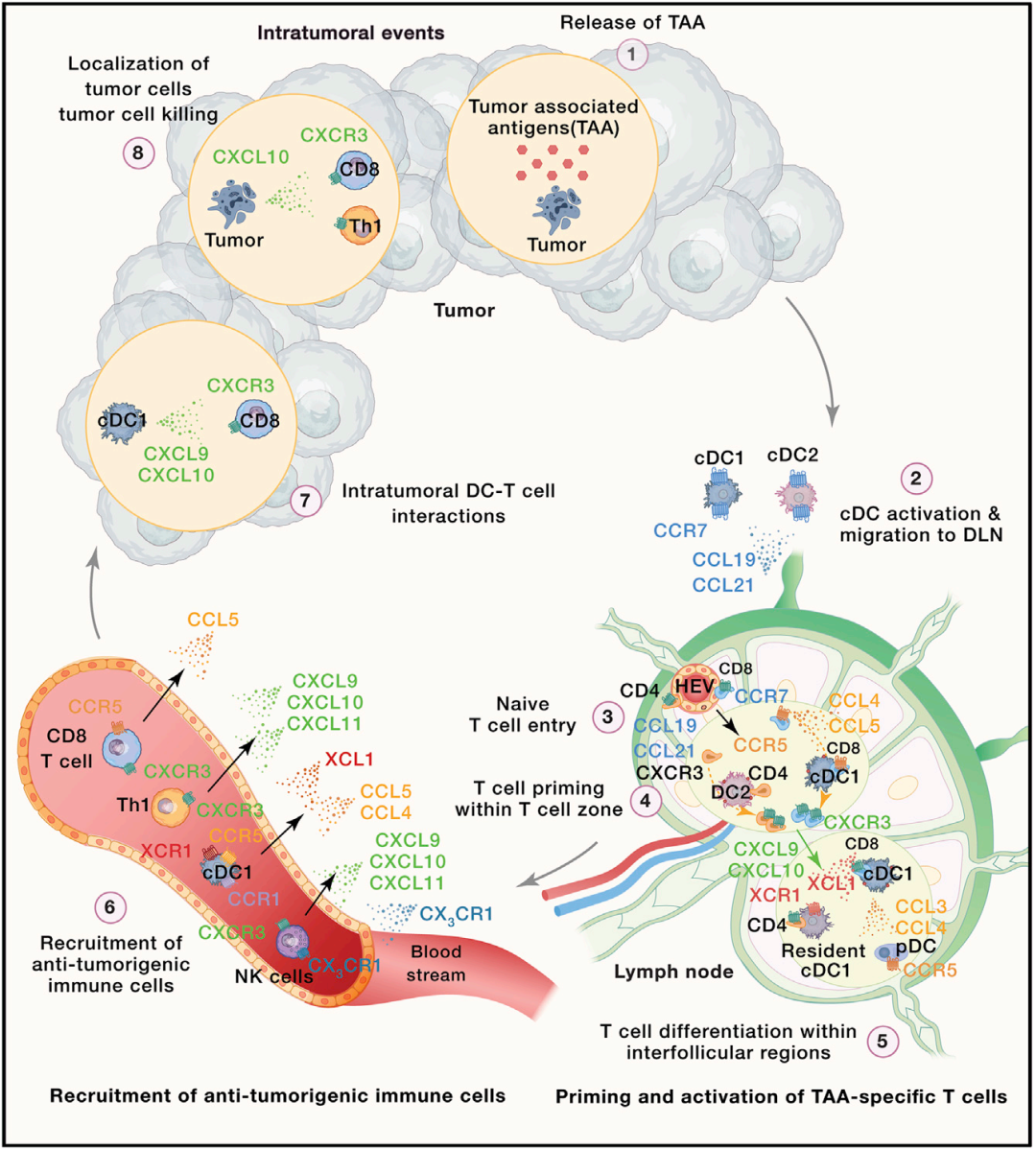
Kohli K, Pillarisetty VG, Kim TS. Key chemokines direct migration of immune cells in solid tumors. Cancer Gene Ther. 2022 Jan;29(1):10-21.
抗瘤趋化因子主要通过募集抗肿瘤免疫细胞、促进免疫细胞活化及效应功能获得、增强肿瘤免疫原性等机制抑制肿瘤发展,核心成员及作用机制如下:
1. XCL1-XCR1轴:XCL1通过该信号轴介导常规树突状细胞1(conventional Dendritic Cell 1, cDC1)向肿瘤组织募集,促进cDC1与CD8+ T细胞的相互作用,驱动T细胞增殖扩增并获得效应器功能,增强抗肿瘤免疫应答。
2. CXCL11:其表达水平与髓源性抑制细胞(Myeloid-Derived Suppressor Cells, MDSCs)的丰度呈负相关,与CD8+ T细胞的浸润程度也呈负相关,通过调控免疫细胞浸润格局发挥抗肿瘤作用。
3. CCR7介导的免疫启动:CCR7可介导cDC1和cDC2细胞从肿瘤组织向肿瘤引流淋巴结(Tumor-Draining Lymph Nodes, TDLN)迁移,启动T细胞的活化和效应功能,是连接肿瘤局部免疫与全身性免疫应答的关键分子。
4. CCL21:介导T细胞和DC细胞向TDLN募集,其表达下调会导致免疫细胞群定位异常,最终降低T细胞活性,而维持其正常表达则有助于增强抗肿瘤免疫。
5. CX3CR1:CD8+ T细胞需接收CX3CR1信号才能有效发挥肿瘤杀伤作用,该受体的表达是CD8+ T细胞获得抗肿瘤功能的必要条件。
(三)双效趋化因子
部分趋化因子因作用靶点的多样性,同时具备促瘤和抗肿瘤双重功能,核心代表如下:
1. CCR5:CCR5-CCL5轴具有双向调控作用:一方面介导cDC1向肿瘤募集,同时募集CD8+ T细胞发挥抗肿瘤效应;另一方面可募集Treg细胞,调控TAM的表型和功能,介导肿瘤与TAM的相互作用,提升肿瘤干细胞特性、转移能力及治疗抵抗,最终表现为促瘤效应。
2. CXCR3:CXCR3-CXCL9/CXCL10轴同样兼具双重功能:既能同时募集Treg和CD8+ T细胞,又能促进干细胞样TCF-1+细胞向cDC1细胞募集,使其在TME中重激活并通过接触IL-2获得效应器功能,同时调控免疫效应细胞在肿瘤附近的定位,其最终效应取决于肿瘤微环境中各类细胞的平衡状态。
二、趋化因子检测服务哪个公司有?
上海乐备实(U-Labex)作为国内领先的实验服务专家,主要专注于提供多组学/多因子相关检测分析,依托多技术平台打造了标准化、高性价比的检测服务体系。
趋化因子检测现货Panel
| 乐备实官网货号 | Panel | 技术平台 | 检测指标 |
| LXLBM23-1 | 小鼠细胞因子-23因子Panel | Luminex | Eotaxin/CCL11,G-CSF,GM-CSF,IFN-γ,IL-10,IL-12(p40),IL-12(p70),IL-13,IL-17A,IL-1α,IL-1β,IL-2,IL-3,IL-4,IL-5,IL-6,IL-9,GRO-α (Gro-a/KC/CXCL1),MCP-1/CCL2,MIP-1α/CCL3,MIP-1β,RANTES,TNF-α |
| LXLBR23-1 | 大鼠细胞因子-23因子Panel | Luminex | G-CSF,GM-CSF,GRO/KC,IFN-γ,IL-1α,IL-1β,IL-2,IL-4,IL-5,IL-6,IL-7,IL-10,IL-12 (p70),IL-13,IL-17A,IL-18,M-CSF,MCP-1,MIP-1α,MIP-3α,RANTES,TNF-α,VEGF |
| LXLBH27-1 | 人细胞因子-27因子Panel | Luminex | G-CSF,GM-CSF,IFN-γ,IL-10,IL-12(p70),IL-13,IL-17A,IL-1β,IL-2,IL-4,IL-5,IL-6,IL-7,IL-8/CXCL8,MCP-1/CCL2,MIP-1β,TNF-α,IL-1Rα,IL-9,IL-15,FGF-basic,Eotaxin/CCL11,IP-10/CXCL10,MIP-1α/CCL3,PDGF-BB,RANTES,VEGF-A |
| LXLBM31-1 | 小鼠趋化因子-31因子Panel | Luminex | BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin/CCL11,Eotaxin-2/CCL24,Fractalkine/CX3CL1,GM-CSF,I-309/CCL1,IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-10,IL-16,IP-10/CXCL10,I-TAC/CXCL11,KC/CXCL1,MCP-1/CCL2,MCP-3/CCL7,MCP-5/CCL12,MDC/CCL22,MIP-1α/CCL3,MIP-1β/CCL4,MIP-3α/CCL20,MIP-3β/CCL19,RANTES/CCL5,SCYB16/CXCL16,SDF-1α/CXCL12,TARC/CCL17,TNF-α |
| LXLBH40-1 |
人趋化因子/细胞因子- 40因子Panel |
Luminex | 6Ckine/CCL21,BCA-1/CXCL13,CTACK/CCL27,ENA-78/CXCL5,Eotaxin/CCL11,Eotaxin-2/CCL24,Eotaxin-3/CCL26,Fractalkine/CX3CL1,GCP-2/CXCL6,GM-CSF,GRO-α (Gro-a/KC/CXCL1),Gro-β/CXCL2,I-309/CCL1,IFN-γ,IL-1β,IL-2,IL-4,IL-6,IL-8/CXCL8,IL-10,IL-16,IP-10/CXCL10,I-TAC/CXCL11,MCP-1/CCL2,MCP-2/CCL8,MCP-3/CCL7,MCP-4/CCL13,MDC/CCL22,MIF,MIG/CXCL9,MIP-1α/CCL3,MIP-1δ/CCL15,MIP-3α/CCL20,MIP-3β/CCL19,MPIF-1/CCL23,SCYB16/CXCL16,SDF-1α+β/CXCL12,TARC/CCL17,TECK/CCL25,TNF-α |
| LXLRH46-1 | 人细胞因子-46因子Panel | Luminex | CCL2/JE/MCP-1,CCL3/MIP-1 alpha,CCL4/MIP-1 beta,CCL5/RANTES,CCL11/Eotaxin,CCL19/MIP-3 beta,CCL20/MIP-3 alpha,CD40 Ligand/TNFSF5,CXCL1/GRO alpha/KC/CINC-1,CXCL2/GRO beta/MIP-2/CINC-3,CXCL10/IP-10/CRG-2,EGF,FGF basic/FGF2/bFGF,Flt-3 Ligand/FLT3L,G-CSF,GM-CSF,Granzyme B,IFN-alpha 2/IFNA2,IFN-beta,IFN-gamma,IL-1 alpha/IL-1F1,IL-1 beta/IL-1F2,IL-1ra/IL-1F3,IL-2,IL-3,IL-4,IL-5,IL-6,IL-7,IL-8/CXCL8,IL-9,IL-10,IL-12 p70,IL-13,IL-15,IL-17/IL-17A,IL-17E/IL-25,IL-33,Lymphotoxin-alpha/TNF-beta,PD-L1/B7-H1,PDGF-AA,PDGF-AB/BB,TGF-alpha,TNF-alpha,TRAIL/TNFSF10,VEGF |
| LXLBH48-1 | 人细胞因子-48因子Panel | Luminex | β-NGF,CTACK/CCL27,Eotaxin/CCL11,FGF-basic,G-CSF,GM-CSF,GRO-α (Gro-a/KC/CXCL1),HGF,IFN-α2,IFN-γ,IL-1α,IL-1Rα,IL-2Rα,IL-1β,IL-2,IL-3,IL-4,IL-5,IL-6,IL-7,IL-8/CXCL8,IL-9,IL-10,IL-12(p40),IL-12(p70),IL-13,IL-15,IL-16,IL-17A,IL-18,IP-10/CXCL10,LIF,M-CSF,MCP-1/CCL2,MCP-3/CCL7,MIG,MIP-1α/CCL3,MIP-1β,MIF,PDGF-BB,RANTES,SCF,SCGF-β,SDF-1α,TRAIL,TNF-α,TNF-β,VEGF-A |
三、结语
趋化因子和趋化因子受体虽难以作为治疗靶点进行开发,但它们为解析诱导和维持促瘤及抗肿瘤免疫细胞状态的关键细胞成分提供了重要线索。未来研究需进一步深入探索趋化因子网络的调控机制,明确不同肿瘤类型中趋化因子的表达特征,开发多靶点联合治疗策略,并通过生物标志物筛选精准定位获益人群,从而提升基于趋化因子系统的肿瘤治疗效果。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


