一、引言
核糖核酸(RNA)提取是分子生物学研究的基础性技术环节,其质量直接影响后续逆转录定量聚合酶链式反应、转录组测序及基因表达分析等实验结果的可靠性与可重复性。核糖核酸酶(RNase)广泛存在于环境、实验器材及人体皮肤表面,具有极高的稳定性和催化活性,且无需辅助因子即可降解RNA分子。因此,在RNA提取全流程中建立系统性的RNase污染防控体系,是保障RNA完整性与纯度的关键前提。本文从污染来源识别、实验环境控制、耗材处理、试剂配制及操作规范五个维度,系统阐述RNase污染防控的技术策略。
二、RNase污染来源的系统性识别
2.1 外源性污染来源
外源性RNase主要来源于实验操作者、实验室空气、共用设备及非专用耗材。人体皮肤、唾液、毛发等均含有高浓度RNase,操作过程中未佩戴手套或口罩、手套接触非无菌表面后未及时更换,均可导致污染转移。此外,公共实验台面、移液器、离心机转子、制冰机等设备表面若未经过RNase清除处理,亦构成潜在污染源。
2.2 内源性污染来源
内源性RNase主要来源于所处理样本本身。富含RNase的组织类型,如胰腺、脾脏、肝脏及某些植物组织,在裂解释放RNA的同时亦释放大量内源性RNase。若裂解缓冲液未能及时抑制RNase活性,或样本裂解不完全、操作时间过长,RNA将迅速被降解。
三、实验环境与耗材的RNase清除处理
3.1 工作区域的物理隔离与清洁
应设立专用的RNA操作区域,该区域需与常规分子生物学实验室、尤其是聚合酶链式反应区域及微生物操作区域物理隔离。操作台面在使用前应以0.1%焦碳酸二乙酯(DEPC)处理水或商品化RNase清除剂擦拭,并辅以紫外灯照射至少30分钟。紫外辐射可使RNA分子发生交联,亦能使RNase蛋白结构变性,从而降低其活性。
3.2 耗材的预处理与选用
所有接触样本或试剂的耗材,包括微量离心管、移液器吸头、研钵、匀浆器等,均应选用经认证无核酸酶(RNase-free)的商品化产品。若需自行处理,可采用下述方法:玻璃器皿需经180℃干热灭菌4小时以上;塑料耗材可采用0.1% DEPC水浸泡过夜后高压灭菌,以分解残留DEPC;电泳槽等设备需以3%过氧化氢或0.5%十二烷基硫酸钠溶液浸泡处理,并以DEPC处理水充分冲洗。
四、试剂配制与储存中的RNase控制
4.1 溶剂与缓冲液的RNase去除
配制RNA相关试剂所需的水相溶剂,必须使用经DEPC处理并高压灭菌的超纯水。DEPC可通过修饰RNase活性中心组氨酸残基的咪唑环而使其失活,常用终浓度为0.1%,处理时间不少于12小时。需注意的是,Tris缓冲液可与DEPC发生反应,因此Tris溶液不适宜采用DEPC处理,应直接使用经认证无核酸酶的商业化产品。
4.2 试剂的分装与储存策略
频繁冻融可导致RNA稳定性下降,亦可能引入反复取用过程中的污染。所有RNA相关试剂,包括裂解液、洗涤液、洗脱液等,应在首次使用前按单次实验用量进行小规格分装,储存于-20℃或-80℃备用。分装过程应在超净工作台内完成,并严格使用无核酸酶耗材。
五、样本处理与RNA提取过程中的操作规范
5.1 样本采集与保存
新鲜组织离体后应尽快进行裂解处理,或立即投入液氮速冻,随后转移至-80℃长期保存。速冻过程可瞬时终止细胞内源性RNase的活性,防止RNA降解。冷冻样本在匀浆前不宜反复冻融,且应直接在冷冻状态下加入裂解液进行匀浆。
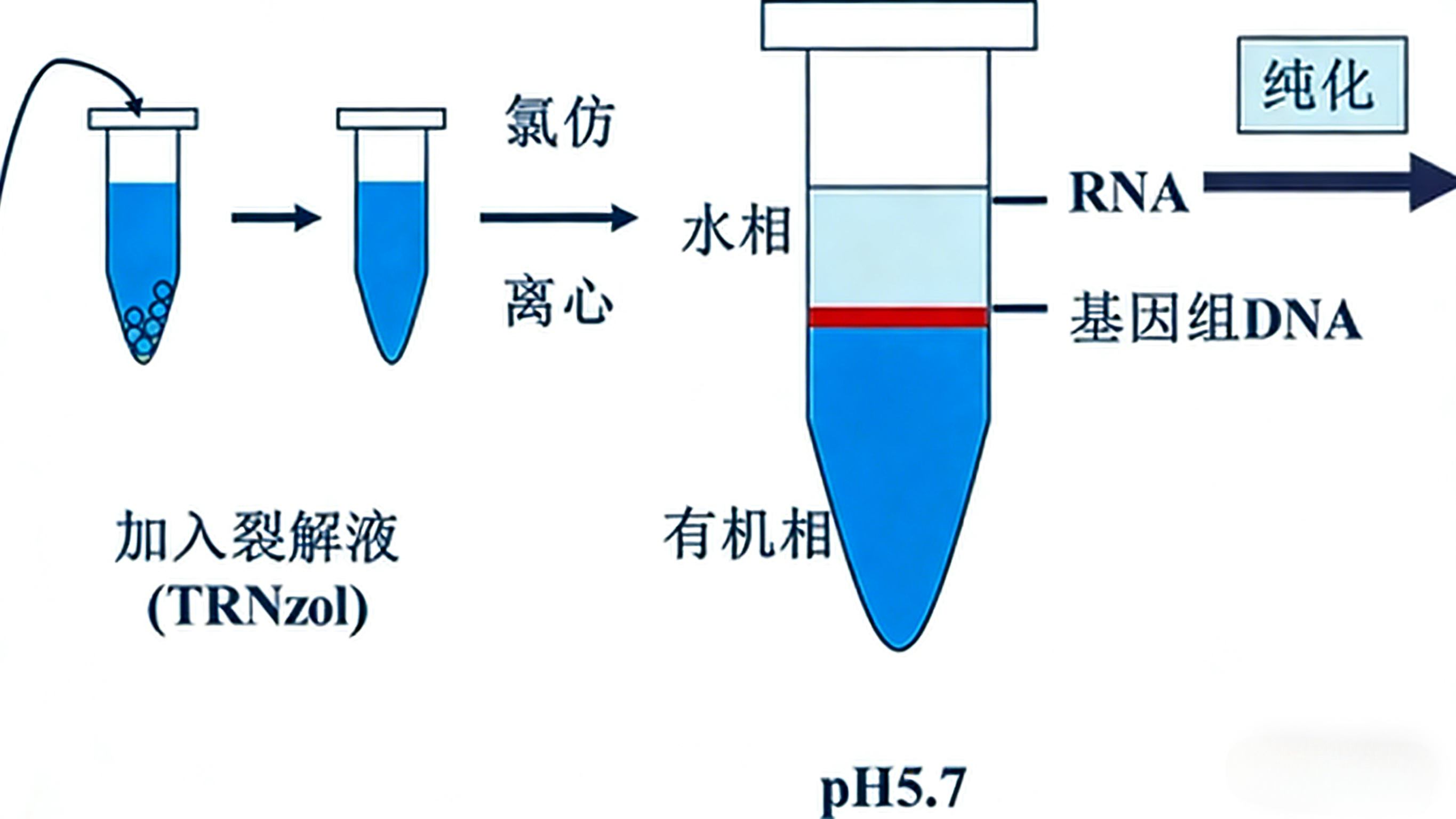
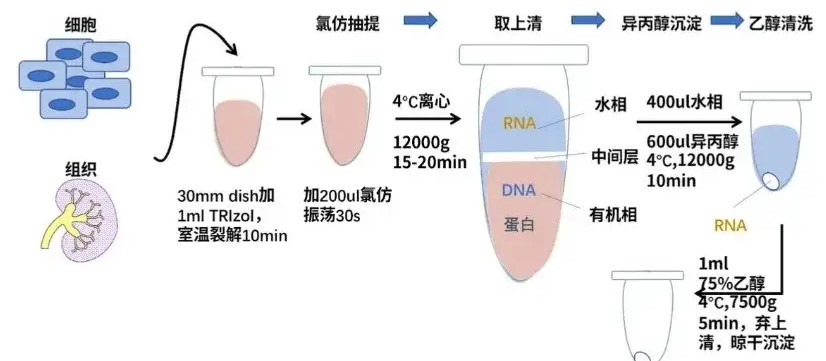
5.2 裂解与匀浆环节的控制
当前广泛应用的异硫氰酸胍-酚仿抽提法,其核心机制在于高浓度异硫氰酸胍可同时裂解细胞并强烈变性RNase。操作中应确保样本与裂解液充分接触,匀浆过程宜在冰浴条件下快速完成,以抑制局部升温引发的酶促反应。对于纤维组织或细胞壁较厚的植物样本,需延长匀浆时间或增加机械破碎强度,以确保RNase被充分变性失活。
5.3 相分离与沉淀步骤的优化
氯仿抽提后离心分离水相时,应避免吸取中间界面蛋白层及下层有机相,以免引入蛋白污染及残余RNase。异丙醇沉淀RNA时,温度不宜过低(通常推荐室温或-20℃),时间不宜过长,以避免盐类共沉淀。沉淀后的RNA应以75%乙醇洗涤两次,充分去除残留盐离子与有机溶剂,乙醇溶液应使用DEPC处理水新鲜配制。
六、RNase污染防控的质量控制与验证
6.1 实验系统的阴性对照设置
每批次RNA提取实验中,应设置无样本的空白裂解液对照,全程同步操作。该对照产物经后续逆转录及扩增后应无特异性条带或Ct值大于预设阈值,以此验证实验体系无RNase污染残留。
6.2 RNA完整性评估
RNA完整性可通过琼脂糖凝胶电泳或微流控芯片电泳进行评价。哺乳动物总RNA电泳图谱应呈现清晰的28S与18S核糖体RNA条带,且28S条带亮度约为18S的两倍。若出现弥散条带、小分子量片段增加或核糖体条带比例倒置,则提示提取过程中存在RNase污染或操作不当。
七、结语
RNA提取过程中的RNase污染防控是一项贯穿“人、机、料、法、环”各要素的系统性工程。通过建立专用操作区域、使用无核酸酶耗材、规范样本处理流程以及设置合理的质量控制节点,可有效抑制RNase活性,保障RNA的完整性与得率。当前,单细胞转录组学与微量样本RNA分析技术对RNA质量提出了更高要求,未来仍需在超微量样本的RNase瞬时抑制、自动化提取设备的洁净度维持等方面开展深入探索。












 沪公网安备31011502400759号
沪公网安备31011502400759号
 营业执照(三证合一)
营业执照(三证合一)


